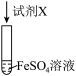
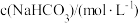1 . 利用下图装置可制备 沉淀,且能较长时间保存该物质而不变质。下列说法不正确的是
沉淀,且能较长时间保存该物质而不变质。下列说法不正确的是
 沉淀,且能较长时间保存该物质而不变质。下列说法不正确的是
沉淀,且能较长时间保存该物质而不变质。下列说法不正确的是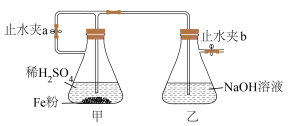
| A.实验开始时,打开止水夹a和止水夹b |
| B.关闭止水夹a,打开止水夹b,甲中溶液可流入乙中 |
C. 能较长时间保存是因 能较长时间保存是因 无氧化性 无氧化性 |
| D.抽滤瓶甲中的稀硫酸可以用稀硝酸代替 |
您最近半年使用:0次
2 . 下列说法不正确的是
| A.铁元素在自然界中以化合态和游离态形式存在 |
B. 中铁的化合价有 中铁的化合价有 和 和 价,是一种混合物 价,是一种混合物 |
C.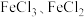 和 和 都可以通过化合反应制取 都可以通过化合反应制取 |
D. 铁与足量稀盐酸反应,转移电子数为 铁与足量稀盐酸反应,转移电子数为 |
您最近半年使用:0次
解题方法
3 . 回答下列问题。
(1)氢氧化亚铁与氧气、水的反应方程式为:___________ 。
(2)钠通常保存在___________ 中,加热时,钠可以在空气中燃烧发出___________ 火焰,生成___________ 色固体。
(3)写出氯气和水反应的化学方程式:___________ 。
(4)电离:电解质溶于水或受热熔化时,形成___________ 的过程。
(5) 、
、 、
、 、
、 、
、 、
、 中,
中,___________ 和___________ 互为同位素,___________ 和___________ 的中子数相等,但质子数不等,所以不是同一种元素。
(6)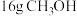 的物质的量是
的物质的量是___________ ,含H原子的数目为___________ 。
(1)氢氧化亚铁与氧气、水的反应方程式为:
(2)钠通常保存在
(3)写出氯气和水反应的化学方程式:
(4)电离:电解质溶于水或受热熔化时,形成
(5)
 、
、 、
、 、
、 、
、 、
、 中,
中,(6)
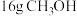 的物质的量是
的物质的量是
您最近半年使用:0次
4 . 铁及其化合物与生产、生活关系密切:
(1)下列铁化合物中,可以通过化合反应得到是_______(填字母序号)。
(2) 可作为铜电路板的腐蚀液,该反应的化学方程式
可作为铜电路板的腐蚀液,该反应的化学方程式_______ 。向反应后的溶液加入_______ (填名称),可回收Cu,并得到 溶液。
溶液。
(3)用废铁皮制取( )的部分流程示意图如下:
)的部分流程示意图如下:_______ 。
(4) 可制取新型、高效水处理剂高铁酸钾,反应原理为
可制取新型、高效水处理剂高铁酸钾,反应原理为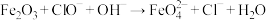 (未配平),该反应中氧化剂与还原剂的物质的量之比为
(未配平),该反应中氧化剂与还原剂的物质的量之比为_______ 。
(5) 可将氨氮废水中
可将氨氮废水中 的转化为
的转化为 除去。从价态角度分析,
除去。从价态角度分析, 能处理氨氮废水的原因是
能处理氨氮废水的原因是_______ 。当该反应转移1.2mol电子时,能产生_______ mol 。
。
(1)下列铁化合物中,可以通过化合反应得到是_______(填字母序号)。
A. | B. | C. | D. |
(2)
 可作为铜电路板的腐蚀液,该反应的化学方程式
可作为铜电路板的腐蚀液,该反应的化学方程式 溶液。
溶液。(3)用废铁皮制取(
 )的部分流程示意图如下:
)的部分流程示意图如下: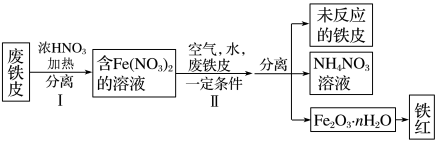
(4)
 可制取新型、高效水处理剂高铁酸钾,反应原理为
可制取新型、高效水处理剂高铁酸钾,反应原理为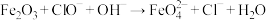 (未配平),该反应中氧化剂与还原剂的物质的量之比为
(未配平),该反应中氧化剂与还原剂的物质的量之比为(5)
 可将氨氮废水中
可将氨氮废水中 的转化为
的转化为 除去。从价态角度分析,
除去。从价态角度分析, 能处理氨氮废水的原因是
能处理氨氮废水的原因是 。
。
您最近半年使用:0次
2024-05-03更新
|
100次组卷
|
2卷引用:福建省晋江市养正中学2023-2024学年高一下学期3月第一次月考化学试题
名校
解题方法
5 .  具有较强的还原性,新制的白色
具有较强的还原性,新制的白色 会逐渐转变为灰绿色,使学生误认为氢氧化亚铁的颜色是灰绿色。为能较长时间观察到白色
会逐渐转变为灰绿色,使学生误认为氢氧化亚铁的颜色是灰绿色。为能较长时间观察到白色 ,某实验小组做了如下探究实验。
,某实验小组做了如下探究实验。
(1)配制实验所需一定物质的量浓度的溶液备用,配制溶液时所用蒸馏水的水分子空间结构为__________ ;使用的 晶体类型为
晶体类型为__________ 。
(2)实验时发现即使是用煮沸过的蒸馏水配制实验所用的溶液,新生成的 也仅能存在几分钟,其原因可能是
也仅能存在几分钟,其原因可能是__________ 。
(3)甲同学按如图a所示操作制备 (溶液均用煮沸过的蒸馏水配制)。挤入少量
(溶液均用煮沸过的蒸馏水配制)。挤入少量 溶液后,立即出现白色沉淀,但很快变成浅绿色,一会儿后变为灰绿色,最终变为红褐色。请分析固体变色的原因:
溶液后,立即出现白色沉淀,但很快变成浅绿色,一会儿后变为灰绿色,最终变为红褐色。请分析固体变色的原因:__________ 。
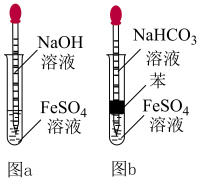
(4)乙同学经查阅资料后设计了如图 所示的装置(溶液均用煮沸过的蒸馏水配制),能较长时间观察到白色
所示的装置(溶液均用煮沸过的蒸馏水配制),能较长时间观察到白色 。
。
①该反应的原理为__________ (用离子方程式表示)。
②结合原理和装置特点分析能较长时间观察到白色 的原因:
的原因:__________ 。
(5)实验试剂最佳浓度探究:
采用不同浓度的试剂进行实验,记录如下。
(1)由以上实验可得到的规律是
①由以上实验可得到的规律是__________ 。
② 溶液的浓度为
溶液的浓度为 时,
时, 溶液的最佳浓度为
溶液的最佳浓度为__________ (填“1.0”“1.5”或“2.0”) 。
。
(6)实验创新:
延长 沉淀的稳定时间还可以采取的措施为
沉淀的稳定时间还可以采取的措施为__________ (任写一条)。
 具有较强的还原性,新制的白色
具有较强的还原性,新制的白色 会逐渐转变为灰绿色,使学生误认为氢氧化亚铁的颜色是灰绿色。为能较长时间观察到白色
会逐渐转变为灰绿色,使学生误认为氢氧化亚铁的颜色是灰绿色。为能较长时间观察到白色 ,某实验小组做了如下探究实验。
,某实验小组做了如下探究实验。(1)配制实验所需一定物质的量浓度的溶液备用,配制溶液时所用蒸馏水的水分子空间结构为
 晶体类型为
晶体类型为(2)实验时发现即使是用煮沸过的蒸馏水配制实验所用的溶液,新生成的
 也仅能存在几分钟,其原因可能是
也仅能存在几分钟,其原因可能是(3)甲同学按如图a所示操作制备
 (溶液均用煮沸过的蒸馏水配制)。挤入少量
(溶液均用煮沸过的蒸馏水配制)。挤入少量 溶液后,立即出现白色沉淀,但很快变成浅绿色,一会儿后变为灰绿色,最终变为红褐色。请分析固体变色的原因:
溶液后,立即出现白色沉淀,但很快变成浅绿色,一会儿后变为灰绿色,最终变为红褐色。请分析固体变色的原因:
(4)乙同学经查阅资料后设计了如图
 所示的装置(溶液均用煮沸过的蒸馏水配制),能较长时间观察到白色
所示的装置(溶液均用煮沸过的蒸馏水配制),能较长时间观察到白色 。
。①该反应的原理为
②结合原理和装置特点分析能较长时间观察到白色
 的原因:
的原因:(5)实验试剂最佳浓度探究:
采用不同浓度的试剂进行实验,记录如下。
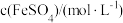 | 1.0 | 1.5 | 2.0 | |
| 1.0 | 现象 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡增多 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率较快 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率迅速 |
| 稳定时间 | 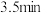 | 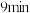 | 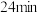 | |
| 1.5 | 现象 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡增多 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率较快 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率迅速 |
| 稳定时间 | 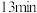 |  | 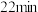 | |
| 2.0 | 现象 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡增多 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率加快 | 常温下无现象,加热后产生白色沉淀 |
| 稳定时间 |  |  |  | |
①由以上实验可得到的规律是
②
 溶液的浓度为
溶液的浓度为 时,
时, 溶液的最佳浓度为
溶液的最佳浓度为 。
。(6)实验创新:
延长
 沉淀的稳定时间还可以采取的措施为
沉淀的稳定时间还可以采取的措施为
您最近半年使用:0次
名校
解题方法
6 . 验证FeSO4的性质,进行如下实验。
实验序号 | 验证性质 | 实验装置 | 试剂X | 实验现象 |
① | 能与某些盐反应 |
| BaCl2溶液 | 产生白色沉淀 |
② | 能与碱反应 | NaOH溶液 | 产生白色絮状沉淀,迅速变为灰绿色,一段时间后变成红褐色 | |
③ | 具有氧化性 | 锌粒 | 锌粒表面变黑,溶液浅绿色褪去 | |
④ | 具有还原性 | KSCN溶液氯水 | 滴加KSCN溶液,无明显现象,再滴加氯水,溶液变为红色 |
下列关于该实验的说法不正确的是
A.①中产生白色沉淀的原因: |
B.②中沉淀变成红褐色的原因: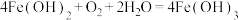 |
| C.③中用镁条(已打磨)替换锌粒,也可以证明FeSO4具有氧化性 |
| D.④中调换试剂的加入顺序,也可以证明FeSO4具有还原性 |
您最近半年使用:0次
名校
解题方法
7 . 构建知识网络是一种有效的学习方法,化学学习中的“价-类”二维图就是其中一种,如图所示是铁及其化合物的“价-类”二维图,请回答下列问题:

(1)在空气中C→B的现象是_____ 。
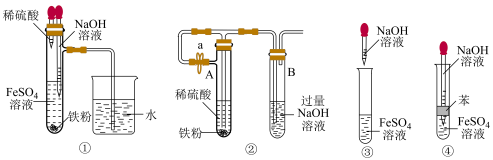
(2)下列各图示中能较长时间观察到 的是
的是_____ 。
(3)铁单质可与水蒸气在高温下发生反应,写出反应的方程式_____ ,当生成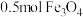 时,转移电子数为
时,转移电子数为_____ 。
(4)将 溶于盐酸后再加入1滴
溶于盐酸后再加入1滴 溶液,则溶液变红时发生反应的离子方程式为
溶液,则溶液变红时发生反应的离子方程式为_____ 。
(5)绿矾 是补血剂的原料,易变质。将硫酸亚铁溶液加热浓缩,冷却结晶,之后
是补血剂的原料,易变质。将硫酸亚铁溶液加热浓缩,冷却结晶,之后_____ 可获得绿矾晶体,如何检验绿矾是否完全变质_____ 。
(6)将硫酸亚铁固体隔绝空气煅烧,可发生以下反应,请将方程式配平:_____ 。
_____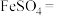 _____
_____ _____
_____ _____
_____

(1)在空气中C→B的现象是
(2)下列各图示中能较长时间观察到
 的是
的是
(3)铁单质可与水蒸气在高温下发生反应,写出反应的方程式
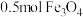 时,转移电子数为
时,转移电子数为(4)将
 溶于盐酸后再加入1滴
溶于盐酸后再加入1滴 溶液,则溶液变红时发生反应的离子方程式为
溶液,则溶液变红时发生反应的离子方程式为(5)绿矾
 是补血剂的原料,易变质。将硫酸亚铁溶液加热浓缩,冷却结晶,之后
是补血剂的原料,易变质。将硫酸亚铁溶液加热浓缩,冷却结晶,之后(6)将硫酸亚铁固体隔绝空气煅烧,可发生以下反应,请将方程式配平:
_____
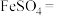 _____
_____ _____
_____ _____
_____
您最近半年使用:0次
解题方法
8 . 请回答下列问题:
(1)氯原子的最外层电子数为___________ ;其最高价氧化物的化学式是___________ 。
(2)维生素 又称“抗坏血酸”,能将
又称“抗坏血酸”,能将 转化为
转化为 ,说明维生素
,说明维生素 具有
具有___________ 性(填“还原”或“氧化”)。
(3)写出白色的氢氧化亚铁沉淀在空气中变色的化学反应方程式___________ 。
(1)氯原子的最外层电子数为
(2)维生素
 又称“抗坏血酸”,能将
又称“抗坏血酸”,能将 转化为
转化为 ,说明维生素
,说明维生素 具有
具有(3)写出白色的氢氧化亚铁沉淀在空气中变色的化学反应方程式
您最近半年使用:0次
2024高三·全国·专题练习
解题方法
9 . 在两支试管里分别加入少量的FeCl3溶液和新制FeSO4溶液,然后各滴入NaOH溶液,观察并记录现象。

(1)FeCl3溶液呈_______ 色,向FeCl3溶液中滴加NaOH溶液,现象为_______ ,反应的离子方程式为_______ 。
(2)FeSO4溶液呈_______ 色,向FeSO4溶液中滴加NaOH溶液,立即_______ ,离子方程式为_______________ ,然后生成的白色絮状沉淀迅速变成_______ 色,过一段时间后,最终变成了___________ 。变成红褐色的原因是_______ ,化学方程式为_______ 。
(3)将甲、乙两试管中的固体分别取出放入烧杯中,分别加入足量的稀盐酸,观察到的现象均为固体_______ ,烧杯中得到_________ 色溶液,离子方程式为_______ 。
(4)白色的Fe(OH)2会被溶解在溶液中的O2氧化,那么在实验室里制取纯净氢氧化亚铁前应该:_____________ 。

(1)FeCl3溶液呈
(2)FeSO4溶液呈
(3)将甲、乙两试管中的固体分别取出放入烧杯中,分别加入足量的稀盐酸,观察到的现象均为固体
(4)白色的Fe(OH)2会被溶解在溶液中的O2氧化,那么在实验室里制取纯净氢氧化亚铁前应该:
您最近半年使用:0次