解题方法
1 . 化学与生活关系密切,解释下列应用的离子方程式正确的是
| 选项 | 应用 | 解释(离子方程式) |
| A | 淀粉—KI溶液(稀硫酸酸化)检验碘盐中含KIO3 | 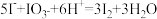 |
| B | 电解饱和食盐水制氢气和氯气 | 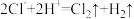 |
| C | 醋酸用于除去水垢 | 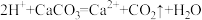 |
| D | 氯化铁用于蚀刻铜板 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021·广东·模拟预测
解题方法
2 . 下列有关离子共存或离子方程式的叙述正确的是
A.Na+、K+、ClO-、 不能大量共存 不能大量共存 |
| B.K+、Fe3+、SCN−、Cl−能大量共存 |
| C.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
D.向碳酸氢铵稀溶液中加入过量烧碱溶液: +OH−=NH3·H2O +OH−=NH3·H2O |
您最近一年使用:0次
名校
3 . 利用如下实验研究 与
与 的反应。
的反应。
步骤1:向烧杯中加入10mL 0.1 的KI溶液,再滴加2mL 0.1
的KI溶液,再滴加2mL 0.1 的
的 溶液,振荡,把溶液分为四等份于编号为①②③④的四支试管中。
溶液,振荡,把溶液分为四等份于编号为①②③④的四支试管中。
步骤2:向试管①中加入淀粉溶液,观察到溶液变蓝。
步骤3:向试管②中滴加15% KSCN溶液5~6滴,观察到溶液变红。
步骤4:向试管③、试管④中分别加入1mL 2.0 的
的 溶液和1mL的蒸馏水,振荡,观察到试管③中溶液颜色比试管④中溶液颜色浅。
溶液和1mL的蒸馏水,振荡,观察到试管③中溶液颜色比试管④中溶液颜色浅。
下列说法不正确的是
 与
与 的反应。
的反应。步骤1:向烧杯中加入10mL 0.1
 的KI溶液,再滴加2mL 0.1
的KI溶液,再滴加2mL 0.1 的
的 溶液,振荡,把溶液分为四等份于编号为①②③④的四支试管中。
溶液,振荡,把溶液分为四等份于编号为①②③④的四支试管中。步骤2:向试管①中加入淀粉溶液,观察到溶液变蓝。
步骤3:向试管②中滴加15% KSCN溶液5~6滴,观察到溶液变红。
步骤4:向试管③、试管④中分别加入1mL 2.0
 的
的 溶液和1mL的蒸馏水,振荡,观察到试管③中溶液颜色比试管④中溶液颜色浅。
溶液和1mL的蒸馏水,振荡,观察到试管③中溶液颜色比试管④中溶液颜色浅。下列说法不正确的是
A.试管①中的现象说明此条件下 的氧化性大于 的氧化性大于 |
B.试管②中的现象说明 与 与 的反应为可逆反应 的反应为可逆反应 |
C.试管②中红色物质的组成为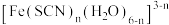 ,此微粒中心离子的配位数为6 ,此微粒中心离子的配位数为6 |
D.步骤4的现象不能说明此条件下 能将 能将 氧化成 氧化成 |
您最近一年使用:0次
2021-05-06更新
|
488次组卷
|
3卷引用:第09讲 铁及其重要化合物(精讲)-2022年一轮复习讲练测
解题方法
4 . 下列离子方程式正确的是
A.金属铜与稀硝酸反应:3Cu+8H++2NO =3Cu2++2NO↑+4H2O =3Cu2++2NO↑+4H2O |
| B.氯化铁和铜反应:Fe3++Cu=Fe2++Cu2+ |
| C.硫酸亚铁溶液与稀硫酸、双氧水混合:2Fe2++2H2O2+4H+=2Fe3++4H2O |
D.过量SO2通入NaClO溶液中:SO2+H2O+ClO-=HClO+HSO |
您最近一年使用:0次
解题方法
5 . 下列反应的方程式正确的是
A.向Fe(NO3)3溶液中加入过量的HI溶液:2NO +8H++6I−=3I2+2NO↑+4H2O +8H++6I−=3I2+2NO↑+4H2O |
| B.苯酚钠溶液中通入少量CO2:2C6H5ONa+CO2+H2O=2C6H5OH+Na2CO3 |
C.向煤中加石灰石可减少煤燃烧时SO2的排放:2CaCO3+O2+2SO2 2CO2+2CaSO4 2CO2+2CaSO4 |
D.氨水中滴加少量CuSO4溶液:Cu2++2NH3·H2O=Cu(OH)2↓+2NH |
您最近一年使用:0次
2021-04-09更新
|
461次组卷
|
6卷引用:课时06 与量有关的离子方程式书写-2022年高考化学一轮复习小题多维练(全国通用)
(已下线)课时06 与量有关的离子方程式书写-2022年高考化学一轮复习小题多维练(全国通用)(已下线)课时05 电解质与离子方程式-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点04 离子反应-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点04 离子反应-备战2022年高考化学一轮复习考点帮(浙江专用)浙江省丽水、湖州、衢州三地市2021届高三4月教学质量检测化学试题(已下线)【浙江新东方】高中化学20210513-015【2021】【高三下】
名校
6 . 氯及其化合物在生产、生活中有广泛应用。下列物质的性质与用途具有对应关系的是
| A.Cl2能溶于水,可用于工业制盐酸 |
| B.ClO2有强氧化性,可用于自来水消毒 |
| C.HClO不稳定,可用作棉、麻的漂白剂 |
| D.FeCl3溶液呈酸性,可用于蚀刻印刷电路板 |
您最近一年使用:0次
2021-03-27更新
|
689次组卷
|
10卷引用:第12讲 富集在海水中的元素——卤素(精练)-2022年高考化学一轮复习讲练测
(已下线)第12讲 富集在海水中的元素——卤素(精练)-2022年高考化学一轮复习讲练测江苏省南京市盐城市2021届高三第二次模拟考试化学试题江苏省常熟市2021-2022学年高三上学期阶段性抽测一化学试题江苏省连云港市赣榆智贤中学2021-2022学年高二上学期第一次月考化学试题(已下线)押新高考卷01题 化学与STSE、传统文化-备战2022年高考化学临考题号押题(新高考通版)江苏省淮安市涟水县第一中学2021-2022学年高三12月份阶段检测化学试题江苏省海安市实验中学2021-2022学年高三上学期11月月考化学试题江苏省扬州中学2021-2022学年高三下学期3月月考化学试题(已下线)一轮巩固卷2-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(全国卷专用)江苏省苏州市吴县中学2023-2024学年高二上学期10月月考化学试题
名校
解题方法
7 . 向一定量的Fe、Fe2O3和CuO混合物投入100mL 0.9mol/L的硫酸溶液中,充分反应后生成448mL标准状况下的气体,得不溶物0.03mol。向滤液中加入2mol/L的NaOH溶液,加至10mL时开始出现沉淀。忽略溶液的体积变化,下列说法不正确的
| A.0.03mol不溶物全为Cu | B.混合物中氧原子的物质的量为0.05mol |
| C.滤液中的阳离子只有两种 | D.滤液中的Fe2+的物质的量浓度为0.8mol/L |
您最近一年使用:0次
2021-02-02更新
|
1407次组卷
|
8卷引用:专题讲座(一) 化学计算的常用方法(精练)-2022年高考化学一轮复习讲练测
(已下线)专题讲座(一) 化学计算的常用方法(精练)-2022年高考化学一轮复习讲练测湖北省沙市中学2020-2021学年高一上学期期末考试化学试题(已下线)3.1.2 不同价态铁元素之间的转化-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)湖北省武汉市第六中学2021-2022学年高一上学期12月月考化学试题江西省景德镇一中2022-2023学年高一上学期期中考试(19班)化学试题重庆市南开中学2022-2023学年高一上学期12月定时练习化学试题湖南省邵阳市第二中学2023-2024学年高一下学期第一次月考化学试题福建师范大学附属中学2021-2022学年高一下学期期末考试化学试题
解题方法
8 . 某兴趣小组用Fe3+与I-间的反应探究氧化还原反应规律与平衡移动原理的关系,回答下列问题:
(1)用Fe2(SO4)3晶体配制100 mL 0.05 mol/L的溶液,配制时需先把Fe2(SO4)3晶体溶解在较浓的硫酸中,再用水稀释,加入硫酸的目的是_____ (结合化学方程式回答)。
(2)甲组同学将0.10 mol/L的KI溶液和0.05 mol/L的Fe2(SO4)3溶液各5 mL混合充分反应后,溶液变为棕黄色,现进行如下实验①②。
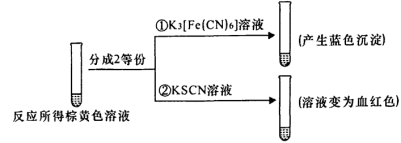
实验①中产生蓝色沉淀的离子方程式为_______ ,根据以上反应现象写出甲组同学实验中的离子方程式:_______ ,在甲组同学的反应中,I2和Fe3+的氧化性强弱顺序为_______ 。
(1)用Fe2(SO4)3晶体配制100 mL 0.05 mol/L的溶液,配制时需先把Fe2(SO4)3晶体溶解在较浓的硫酸中,再用水稀释,加入硫酸的目的是
(2)甲组同学将0.10 mol/L的KI溶液和0.05 mol/L的Fe2(SO4)3溶液各5 mL混合充分反应后,溶液变为棕黄色,现进行如下实验①②。

实验①中产生蓝色沉淀的离子方程式为
您最近一年使用:0次
9 . 硫化镍矿的主要成分是 ,还含有
,还含有 、
、 、一些不溶性物质等,工业上用硫化镍矿制备金属镍的工艺流程如图所示:
、一些不溶性物质等,工业上用硫化镍矿制备金属镍的工艺流程如图所示:
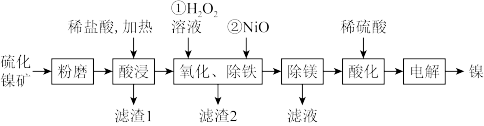
(1)硫化镍矿粉磨的目的是_______ ,“酸浸”时,硫化镍与稀盐酸反应的化学方程式为_______ 。
(2)“氧化、除铁”过程中加入 溶液时,发生反应的离子方程式为
溶液时,发生反应的离子方程式为_______ ;加入氧化镍的目的是除去铁元素,用化学平衡移动原理解释除去铁元素的原因_______ 。
(3)已知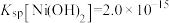 ,
,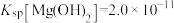 ,若“除镁”后的滤液中
,若“除镁”后的滤液中 的浓度不大于
的浓度不大于 ,则滤液中
,则滤液中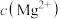 ≤
≤_______ 。
(4)电解硫酸镍溶液时,在_______ 极得到镍单质,电解产物_______ (填化学式)可以循环使用。
 ,还含有
,还含有 、
、 、一些不溶性物质等,工业上用硫化镍矿制备金属镍的工艺流程如图所示:
、一些不溶性物质等,工业上用硫化镍矿制备金属镍的工艺流程如图所示:
(1)硫化镍矿粉磨的目的是
(2)“氧化、除铁”过程中加入
 溶液时,发生反应的离子方程式为
溶液时,发生反应的离子方程式为(3)已知
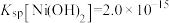 ,
,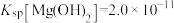 ,若“除镁”后的滤液中
,若“除镁”后的滤液中 的浓度不大于
的浓度不大于 ,则滤液中
,则滤液中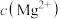 ≤
≤(4)电解硫酸镍溶液时,在
您最近一年使用:0次
解题方法
10 . 下列物质反应后一定有+3价铁生成的是
①过量的Fe与Cl2反应;②Fe与过量稀硫酸反应;③FeCl2溶液中通入少量Cl2;④Fe和Fe2O3的混合物溶于盐酸中
①过量的Fe与Cl2反应;②Fe与过量稀硫酸反应;③FeCl2溶液中通入少量Cl2;④Fe和Fe2O3的混合物溶于盐酸中
| A.只有① | B.①③ |
| C.①②③ | D.①③④ |
您最近一年使用:0次



