1 . 南阳古称“宛”,文化源远流长,博大精深。南阳在汉代是全国的冶铁中心,汉冶遗址公园和汉冶路是南阳人对这段历史的纪念。下列有关叙述中蕴含的化学知识错误的是
| A.曹植的“磁石引铁,于金不连”——“磁石”为四氧化三铁,能吸引铁,不能吸引金 |
| B.杜牧的“折戟沉沙铁未销”——铁生锈的条件是与水和氧气同时接触 |
| C.杨万里的“庐山山南刷铜绿”——“铜绿”主要成分为铜的氧化物 |
| D.沈括的“以剂钢为刃,柔铁为茎干,不尔则多断折”——“剂钢”是指铁的合金 |
您最近一年使用:0次
名校
解题方法
2 . 下列反应,其产物的颜色按红色、红褐色、淡黄色、蓝色顺序排列的是
①金属钠在纯氧中燃烧
②FeSO4溶液中滴入NaOH溶液,并在空气中放置一段时间
③FeCl3溶液中滴入KSCN溶液
④无水硫酸铜放入医用酒精中
①金属钠在纯氧中燃烧
②FeSO4溶液中滴入NaOH溶液,并在空气中放置一段时间
③FeCl3溶液中滴入KSCN溶液
④无水硫酸铜放入医用酒精中
| A.②③①④ | B.③②①④ | C.③①②④ | D.①②③④ |
您最近一年使用:0次
2022-01-13更新
|
1233次组卷
|
83卷引用:2016-2017学年河南省南阳一中高一上月考二化学卷
2016-2017学年河南省南阳一中高一上月考二化学卷2016-2017学年河南省南阳一中高一月考二化学卷(已下线)2010年广东省湛江二中高二第二学期期中考试化学(文)试题(已下线)2010年湖南省浏阳一中高一上学期第三次阶段性测试化学卷(已下线)2010—2011学年湖北省沙市中学高一上学期期末考试化学试卷(已下线)2011-2012学年黑龙江省庆安三中高一上学期期末考试化学试卷(已下线)2012-2013学年山东省济宁市汶上一中高一3月质量检测化学试卷(已下线)2012-2013学年广东省佛山市佛山一中高一下学期期中考试化学试卷(已下线)2012-2013学年广东省佛山市佛山一中高一下学期期中考试化学试卷(已下线)2012-2013学年山西省晋中市昔阳中学高二下学期期末考试化学试卷(已下线)2012-2013学年辽宁省铁岭市六校第一次联合考试化学试卷(已下线)2013-2014学年江苏省宿迁市高一上学期第二次月考化学试卷(已下线)2015届甘肃省天水市秦安县二中高三上学期期中考试化学试卷2014-2015黑龙江省哈尔滨六中高一12月月考化学试卷2014-2015湖南省浏阳一中等三校高一12月联考化学试卷2014-2015黑龙江省绥化市三校高一上学期期末联考化学试卷14-15内蒙古北方重工业集团三中高一上学期期末化学试卷2014-2015广东省深圳市南山区上学期高一化学期末试卷陕西省咸阳市西藏民族学院附属中学2015-2016学年高一上期末化学卷2015-2016学年广东省肇庆市高一上学期期末考试化学试卷2015-2016学年黑龙江省绥棱一中高二6月月考化学试卷2015-2016学年甘肃省甘谷一中高一上期末化学试卷2017届辽宁省铁岭市高三上学期第一次联考化学试卷2016-2017学年江西省南昌市第二中学高一上学期期末考试化学试卷2016-2017学年黑龙江省鸡西市第十九中学高一上学期期末考试化学试卷辽宁省大石桥市第二高级中学2016-2017学年高二学业水平模拟测试化学试题青海省西宁市第四高级中学2017-2018学年高一上学期第二次月考化学试题1湖北省荆州中学2017-2018学年高一12月月考化学试题湖南省醴陵市第一中学2017-2018学年高一上学期第二次月考(12月)化学试题湖北省宜昌市葛洲坝中学2017-2018学年高一12月月考化学试题湖北省宜昌市长阳县第一高级中学2017-2018学年高一12月月考化学试题安徽省淮南市第二中学2017-2018学年高一上学期第二次月考化学试题新疆昌吉市2017-2018学年高一上学期期末考试化学试题天津市红桥区2017-2018学年高一上学期期末考试化学试题宁夏银川一中2017-2018学年高一上学期期末考试化学试题湖北省宜昌市示范高中协作体2017-2018学年高一上学期期末化学试题湖南省师范大学附属中学2017-2018学年高一上学期期末考试化学试题黑龙江省伊春中学2017-2018学年高一化学上学期期末考试题【全国百强校】青海省平安县第一高级中学2017-2018学年高一下学期期中考试(A卷)化学试题人教版2017-2018学年高一化学必修1:3.2 几种重要的金属化合物 同步测试2【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高二(文)上学期10月月考化学试题河南省封丘县一中2018-2019学年高一上学期12月月考化学试题河南省信阳市第六高级中学2018-2019学年高一上学期第三次(1月)月考化学试题山西省晋中市平遥县第二中学2018-2019学年高一上学期12月月考化学试题陕西省黄陵中学2018-2019学年高一(普通班)上学期期末考试化学试题宁夏回族自治区青铜峡市高级中学2018-2019学年高一上学期期末考试化学试题新疆石河子第二中学2018-2019学年高一上学期期末考试化学试题内蒙古开来中学2018-2019学年高二下学期期末考试化学试题辽宁省实验中学东戴河分校2020届高三上学期期初摸底考试化学试题黑龙江省佳木斯市汤原高级中学2018-2019学年高二下学期期末考试化学试题江西省赣州市会昌中学2019-2020学年高一上学期第二次月考化学试题河北省安平中学2019-2020学年高一上学期第四次月考化学试题山西省晋中市平遥县第二中学2019-2020学年高一12月月考化学试题北京市昌平区新学道临川学校2019-2020学年高一上学期期末考试化学试题福建省泉州第五中学苏教版高中化学必修1专题3 单元综合练习云南省大理市下关第一中学2019-2020学年高一上学期期末考试化学试题安徽省六安市第一中学2019-2020学年高一下学期疫情防控延期开学期间辅导测试(二)化学试题四川省南充市阆中中学2020届高三化学选择题专项训练(15)江西省上饶市2019-2020学年高一上学期期末考试 化学(自招班)试题天津市西青区2019-2020学年高一上学期期末考试化学试题(已下线)专题3.2 铁及其化合物 -巅峰冲刺山东省2020年高考化学一轮考点扫描《2020年新高考政策解读与配套资源》陕西省咸阳市实验中学2019-2020学年高一上学期第三次月考化学试题河北省衡水市桃城区第十四中学2019-2020学年高一下学期第六次综合测试化学试题人教版(2019)高一必修第一册 第三章 铁 金属材料 第一节 铁及其化合物河南省洛阳市第一高级中学2021届高三上学期10月月考化学试题黑龙江省鸡东县第二中学2020-2021学年高一上学期中考试化学试卷宁夏石嘴山市平罗中学2020-2021学年高一上学期第三次月考化学试题天津市东丽区2020-2021学年高一上学期期末考试化学试题吉林省长春市第二十中学2020-2021学年高一上学期第三次考试化学试题广西南宁市英华学校2020-2021学年高一上学期期末考试化学试题(已下线)专题3.1.3 铁盐与亚铁盐(备作业)-【上好课】2021-2022学年高一化学同步备课系列(人教版2019必修第一册)吉林省长春市农安县2021-2022学年高一上学期期末考试化学试题新疆哈密市第八中学2021-2022学年高一上学期期末考试化学试题陕西省西安市阎良区关山中学2021-2022学年高一上学期第三次质量检测化学(理科)试题安徽省宿州市北方中学2021-2022学年高一上学期期末测试化学试题2023年广东省普通高中学业水平合格性考试化学科模拟测试卷(四)2023年广东省普通高中学业水平合格性考试化学科模拟仿真卷(一)天津市新华中学2022-2023学年高一上学期期末考试化学试题 云南省玉溪第一中学2022-2023学年高一下学期期中考试化学试题(已下线)专题九 铁及其化合物(已下线)合格考真题汇编8金属元素及其化合物二云南省大理白族自治州实验中学2020-2021学年高一上学期12月月考化学试题天津北京师范大学静海附属学校2023-2024学年高一上学期第三次月考化学试题
3 . 有A、B、C、D、E、F六种化合物,它们之间的反应关系如下所示:
①A+B→C+E ②C + NaOH→蓝色沉淀D + F
③ D→A+E ④F + Ba(NO3)2 → 白色沉淀 + NaNO3
回答下列问题:
(1)写出它们的化学式:
A____________ ;B____________ ;C____________ ;
D____________ ;E____________ ;F____________ 。
(2)写出①④反应的离子方程式:
①_______ ;④_________ 。
①A+B→C+E ②C + NaOH→蓝色沉淀D + F
③ D→A+E ④F + Ba(NO3)2 → 白色沉淀 + NaNO3
回答下列问题:
(1)写出它们的化学式:
A
D
(2)写出①④反应的离子方程式:
①
您最近一年使用:0次
2020-09-23更新
|
1874次组卷
|
8卷引用:河南省南阳市鸭河工业南都实验中学2020-2021学年高一上学期10月月考化学试题
4 . 在给定条件下,下列选项所示的物质间转化均能实现的是( )
A.CH3CH2Br CH3CH2OH CH3CH2OH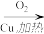 CH3CHO CH3CHO |
B.CuO Cu(OH)2 Cu(OH)2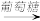 Cu2O Cu2O |
C.Mg2(OH)2CO3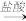 MgCl2(aq) MgCl2(aq)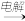 Mg Mg |
D.NaCl(aq) NaHCO3 NaHCO3 Na2CO3 Na2CO3 |
您最近一年使用:0次
名校
解题方法
5 . 绿色植物标本用醋酸铜[(CH3COO)2Cu]处理后颜色更鲜艳、稳定。某化学小组制备醋酸铜晶体并测定产品中铜的含量,实验如下。
Ⅰ.醋酸铜晶体的制备中

(1)用离子方程式表示过程①产物中OH-的来源:___________ ;
(2)过程②对应的化学方程式是:___________ 。
Ⅱ.测定产品中铜的含量
i.取ag醋酸铜产品放入带磨口塞子的锥形瓶中,用稀醋酸溶解,加入过量KI溶液,产Cul沉淀,溶液呈棕黄色;
ii.用b mol·L -1Na2S2O3标准溶液滴定i中的浊液至浅黄色时,加入几滴淀粉溶液,溶液变蓝,继续用Na2S2O3标准溶液滴定至蓝色近于消失;(已知:2 +I2=
+I2= +2I-)
+2I-)
iii.向ⅱ所得浊液中加入KSCN溶液,充分摇动,溶液蓝色加深;
iv.继续用Na2S2O3标准溶液滴定中浊液至终点,消耗标准溶液vmL。
已知:①Na2S2O3溶液和Na2S4O6溶液颜色均为无色;
②Cul易吸附I2,被吸附的I2不与淀粉发 CuSCN生显色反应。难溶于水且不吸附I2
(3)i中发生反应的离子方程式是_________ ;
(4)醋酸铜产品中铜元素的质量分数是_______ 。
Ⅰ.醋酸铜晶体的制备中

(1)用离子方程式表示过程①产物中OH-的来源:
(2)过程②对应的化学方程式是:
Ⅱ.测定产品中铜的含量
i.取ag醋酸铜产品放入带磨口塞子的锥形瓶中,用稀醋酸溶解,加入过量KI溶液,产Cul沉淀,溶液呈棕黄色;
ii.用b mol·L -1Na2S2O3标准溶液滴定i中的浊液至浅黄色时,加入几滴淀粉溶液,溶液变蓝,继续用Na2S2O3标准溶液滴定至蓝色近于消失;(已知:2
 +I2=
+I2= +2I-)
+2I-)iii.向ⅱ所得浊液中加入KSCN溶液,充分摇动,溶液蓝色加深;
iv.继续用Na2S2O3标准溶液滴定中浊液至终点,消耗标准溶液vmL。
已知:①Na2S2O3溶液和Na2S4O6溶液颜色均为无色;
②Cul易吸附I2,被吸附的I2不与淀粉发 CuSCN生显色反应。难溶于水且不吸附I2
(3)i中发生反应的离子方程式是
(4)醋酸铜产品中铜元素的质量分数是
您最近一年使用:0次
解题方法
6 . 下列说法中,不正确的是
| A.玻璃钢是复合材料 | B.铜在空气中会生成铜锈 |
| C.金属钠着火时可使用煤油灭火 | D.铝是活泼金属,但在空气中耐腐蚀 |
您最近一年使用:0次
解题方法
7 . 铜是生产和生活中用量较多的金属。
(1)下列有关铜元素的说法中,不正确的是__________ (填字母)
A.青铜、不锈钢、硬铝都是合金
B.铜表面易形成致密的氧化膜
C.铜与O2反应生成黑色的CuO
D.CuSO4·5H2O是一种混合物,加热后变为白色固体
(2)某化学小组为测定某铜铝混合物中铜的质量分数,设计了如下实验方案:
方案Ⅰ:铜铝混合物 测定生成气体的体积
测定生成气体的体积
方案Ⅱ:铜铝混合物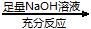 测定剩余固体的质量
测定剩余固体的质量
①请写出方案Ⅰ中铜与稀硝酸反应的离子方程式:___________ ,该方案中稀硝酸表现出来的性质是___________ (填字母)。
A.挥发性 B.酸性 C.氧化性 D.还原性
②方案Ⅱ比方案Ⅰ更易于实施,理由是________________ 。请写出方案Ⅱ中发生反应的化学方程式:____________ ,该反应产生气体在标准状况下的体积为________ (铜铝混合物质量是m1g,反应后剩余固体的质量m2g,用含m1、m2的代数式表示)。
(1)下列有关铜元素的说法中,不正确的是
A.青铜、不锈钢、硬铝都是合金
B.铜表面易形成致密的氧化膜
C.铜与O2反应生成黑色的CuO
D.CuSO4·5H2O是一种混合物,加热后变为白色固体
(2)某化学小组为测定某铜铝混合物中铜的质量分数,设计了如下实验方案:
方案Ⅰ:铜铝混合物
 测定生成气体的体积
测定生成气体的体积方案Ⅱ:铜铝混合物
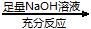 测定剩余固体的质量
测定剩余固体的质量①请写出方案Ⅰ中铜与稀硝酸反应的离子方程式:
A.挥发性 B.酸性 C.氧化性 D.还原性
②方案Ⅱ比方案Ⅰ更易于实施,理由是
您最近一年使用:0次
2020-01-02更新
|
126次组卷
|
2卷引用:河南省南阳市六校2019-2020学年高一下学期第一次联考试题 化学
名校
8 . 向Cu、Cu2O和CuO组成的混合物中,加入1L0.6 mol/L HNO3溶液恰好使其完全溶解,同时收集到2240 mL NO气体(标准状况)。下列说法中不正确的是
(已知:Cu2O+2H+=Cu+Cu2++H2O)
(已知:Cu2O+2H+=Cu+Cu2++H2O)
| A.上述体现酸性的硝酸与体现氧化性的硝酸其物质的量之比为5:1 |
| B.若混合物中含0.1molCu,使该混合物与稀硫酸充分反应,消耗硫酸的物质的量为0.1mol |
| C.Cu2O跟稀硝酸反应的离子方程式为:3Cu2O+14H++2NO3-=6Cu2++2NO↑+7H2O |
| D.若将上述混合物用足量的H2加热还原,所得到固体的质量为32g |
您最近一年使用:0次
2019-10-03更新
|
244次组卷
|
4卷引用:河南省南阳市第一中学2018届高三上学期第三次考试化学试题
名校
9 . 下列化学方程式中,不能正确表达反应颜色变化的原因的是
| A.铜久置空气中表面出现绿色固体:2Cu+O2+CO2+H2O═Cu2(OH)2CO3 |
B.某种火箭发射阶段有少量N2O4,逸出,产生红色气体:N2O4 2NO2 2NO2 |
C.FeSO4·7H2O在空气中久置变黄:2FeSO4·7H2O Fe2O3+SO2↑+SO3↑+14H2O Fe2O3+SO2↑+SO3↑+14H2O |
| D.SO2通入KMnO4溶液中,溶液紫色逐渐褪去:5SO2+2KMnO4+2H2O═K2SO4+2MnSO4十2H2SO4 |
您最近一年使用:0次
2019-09-09更新
|
400次组卷
|
5卷引用:河南省南阳市第一中学2020届高三上学期第二次开学考试化学试题
河南省南阳市第一中学2020届高三上学期第二次开学考试化学试题山东省临沂市第一中学2020届高三10月月考化学试题2019年湖北省黄冈市高三11月新高考备考监测联考化学试题山东省新高考备考监测2020届高三10月联考化学试题(已下线)《2020年新高考政策解读与配套资源》模拟试题10-2020年北京新高考化学模拟试题
10 . 狐刚子在“炼石胆取精华法”中作如下叙述:“以士擊(即砖坯)垒作两个方头炉,一炉中著铜盘,使定,即密泥之,一炉中以炭烧石胆(CuSO4·5H2O)使作烟,以物扇之,其精华尽入铜盘。炉中却火待冷……”。狐刚子所取“精华”为
| A.H2O | B.SO2 | C.稀硫酸 | D.CuSO4溶液 |
您最近一年使用:0次
2017-12-13更新
|
237次组卷
|
2卷引用:河南省南阳市2018届高三第三次联考化学试题



