1 . 氯化铜晶体(CuCl2·2H2O)常用作玻璃、陶瓷着色剂和饲料添加剂等。工业上用粗制氧化铜粉(含杂质FeO和SiO2)制备无水氯化铜,制取流程如下:

已知:氯化亚砜( 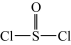 )熔点-101℃,沸点76℃,易水解。回答下列问题:
)熔点-101℃,沸点76℃,易水解。回答下列问题:
(1)为避免引入杂质,试剂x可选用___________ (填字母)
a.KMnO4溶液 b.Cl2水 c.Br2水 d.H2O2溶液
(2)溶液C中加入试剂y可以调节溶液pH,控制pH的取值范围为______~________________ ,从而除去Fe3+而不引入杂质。试剂y可选用下列物质中的___________ (填字母)
a.Cu b.CuO c.Cu2(OH)2CO3 d.NaOH
(3)SOCl2与水反应的化学方程式为___________ 。
(4)SOCl2与CuCl2·2H2O混合并加热,可得到无水CuCl2的原因是__________________ 。

| Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | |
| 开始沉淀的pH | 1.9 | 7.0 | 4.7 |
| 沉淀完全的pH | 3.2 | 9.0 | 6.7 |
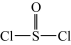 )熔点-101℃,沸点76℃,易水解。回答下列问题:
)熔点-101℃,沸点76℃,易水解。回答下列问题:(1)为避免引入杂质,试剂x可选用
a.KMnO4溶液 b.Cl2水 c.Br2水 d.H2O2溶液
(2)溶液C中加入试剂y可以调节溶液pH,控制pH的取值范围为______~_____
a.Cu b.CuO c.Cu2(OH)2CO3 d.NaOH
(3)SOCl2与水反应的化学方程式为
(4)SOCl2与CuCl2·2H2O混合并加热,可得到无水CuCl2的原因是
您最近一年使用:0次
解题方法
2 . 已知: ,氢氧化铜悬浊液受热易分解生成
,氢氧化铜悬浊液受热易分解生成 。蚀刻含铜电路板有多种方法,用蚀刻废液可制备
。蚀刻含铜电路板有多种方法,用蚀刻废液可制备 。
。
(1)酸性蚀刻液法(过氧化氢-盐酸法)。
①用过氧化氢和盐酸蚀刻含铜电路板时发生的离子反应方程式为_______ 。
②反应后有气泡产生,且反应一段时间后,随着溶液变蓝,产生气泡的速率加快,可能的原因是_______ 。
(2)碱性蚀刻液法。碱性含铜蚀刻液主要成分为 、氨水、氯化铵等。蚀刻过程中,
、氨水、氯化铵等。蚀刻过程中, 与电路板上的铜发生反应生成
与电路板上的铜发生反应生成 ,失去蚀刻能力,通入空气可恢复蚀刻能力。
,失去蚀刻能力,通入空气可恢复蚀刻能力。
①
 中
中 键的数目为
键的数目为_______ 。
②蚀刻能力恢复的化学方程式为_______ 。
(3)酸性蚀刻废液与碱性蚀刻废液混和可析出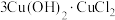 沉淀,pH在4~5之间易生成氢氧化铜胶体。酸性蚀刻废液与碱性蚀刻废液混和反应装置如图1所示。不同pH时,铜元素回收率如图2所示。
沉淀,pH在4~5之间易生成氢氧化铜胶体。酸性蚀刻废液与碱性蚀刻废液混和反应装置如图1所示。不同pH时,铜元素回收率如图2所示。
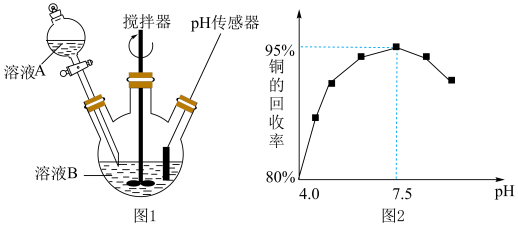
①为减少 胶体形成而影响后续操作,溶液A为
胶体形成而影响后续操作,溶液A为_______ (选填“酸性”或“碱性”)蚀刻废液。
② 时,铜元素回收率下降的原因为
时,铜元素回收率下降的原因为_______ 。
(4)设计从酸性蚀刻废液中制备氧化铜的实验方案。向一定质量的酸性蚀刻废液中_______ 。(实验中必须 使用的试剂:20% 溶液、硝酸银溶液、稀硝酸、蒸馏水)
溶液、硝酸银溶液、稀硝酸、蒸馏水)
 ,氢氧化铜悬浊液受热易分解生成
,氢氧化铜悬浊液受热易分解生成 。蚀刻含铜电路板有多种方法,用蚀刻废液可制备
。蚀刻含铜电路板有多种方法,用蚀刻废液可制备 。
。(1)酸性蚀刻液法(过氧化氢-盐酸法)。
①用过氧化氢和盐酸蚀刻含铜电路板时发生的离子反应方程式为
②反应后有气泡产生,且反应一段时间后,随着溶液变蓝,产生气泡的速率加快,可能的原因是
(2)碱性蚀刻液法。碱性含铜蚀刻液主要成分为
 、氨水、氯化铵等。蚀刻过程中,
、氨水、氯化铵等。蚀刻过程中, 与电路板上的铜发生反应生成
与电路板上的铜发生反应生成 ,失去蚀刻能力,通入空气可恢复蚀刻能力。
,失去蚀刻能力,通入空气可恢复蚀刻能力。①

 中
中 键的数目为
键的数目为②蚀刻能力恢复的化学方程式为
(3)酸性蚀刻废液与碱性蚀刻废液混和可析出
 沉淀,pH在4~5之间易生成氢氧化铜胶体。酸性蚀刻废液与碱性蚀刻废液混和反应装置如图1所示。不同pH时,铜元素回收率如图2所示。
沉淀,pH在4~5之间易生成氢氧化铜胶体。酸性蚀刻废液与碱性蚀刻废液混和反应装置如图1所示。不同pH时,铜元素回收率如图2所示。
①为减少
 胶体形成而影响后续操作,溶液A为
胶体形成而影响后续操作,溶液A为②
 时,铜元素回收率下降的原因为
时,铜元素回收率下降的原因为(4)设计从酸性蚀刻废液中制备氧化铜的实验方案。向一定质量的酸性蚀刻废液中
 溶液、硝酸银溶液、稀硝酸、蒸馏水)
溶液、硝酸银溶液、稀硝酸、蒸馏水)
您最近一年使用:0次
名校
解题方法
3 . 10℃时,分别向4支小试管中滴加8滴1mol/LCuSO4溶液,再分别向其中滴加2mol/LNaOH溶液,边滴加边振荡,实验数据及现象如下表:
取浅绿色沉淀用蒸馏水反复洗涤,加入稀盐酸完全溶解,再加入适量BaCl2溶液,产生大量白色沉淀。取蓝色沉淀重复上述实验,无白色沉淀。经检验,试管3、4中黑色沉淀中含有CuO。
下列说法不正确 的是
| 试管编号 | 1 | 2 | 3 | 4 |
| 滴加NaOH溶液的量 | 2滴 | 6滴 | 12滴 | 16滴 |
| 立即观察沉淀的颜色 | 浅绿色 | 浅绿色 | 蓝色 | 蓝色 |
| 酒精灯加热浊液后沉淀的颜色 | 浅绿色 | 浅绿色 | 黑色 | 黑色 |
下列说法
| A.由实验现象可知浅绿色沉淀中可能含有碱式硫酸铜 |
| B.CuSO4溶液与NaOH溶液反应时,其相对量不同可以得到不同的产物 |
C.试管3、4中的固体在加热过程中发生了反应:Cu(OH)2 CuO+H2O CuO+H2O |
| D.取浅绿色沉淀再滴加适量NaOH溶液后加热仍不会变黑 |
您最近一年使用:0次
2021-05-10更新
|
961次组卷
|
6卷引用:北京市第二十二中学2021-2022学年高三上学期期中考试化学试题
北京市第二十二中学2021-2022学年高三上学期期中考试化学试题北京市西城区2021届高三化学第二次模拟考试(已下线)第三章能力提升检测卷-2022年高考化学一轮复习讲练测2020年北京高考化学真题变式题11-19北京市房山区2022-2023学年高三上学期期末考试化学试题(已下线)北京市第四中学2022-2023学年高三下学期零模化学试题
名校
解题方法
4 . 某含结晶水的盐A是制备负载型活性铁催化剂的主要原料,由五种常见元素组成,M(A)<500 g·mol−1。某兴趣小组对盐A进行了实验探究,流程如下:
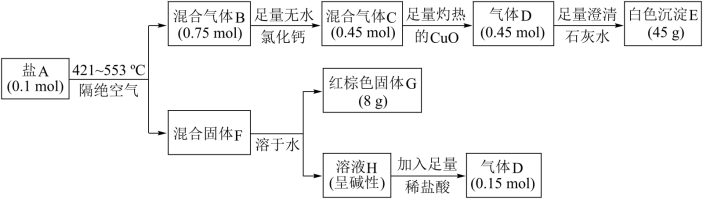
已知:①混合气体C转化为气体D时,质量增加了4.8 g;②溶液H为单一溶质,且不与氢氧化钾反应,焰色反应呈紫色。请回答:
(1)盐A除Fe、H、O以外的两种元素是_____ 。(填元素符号)
(2)混合气体C的组成成分_____ (填化学式)
(3)盐A在421~553℃下分解生成混合气体B和混合固体F的化学方程式:_____ 。
(4)盐A中加入足量稀硫酸,可得到一种二元弱酸,且该弱酸可以被酸性高锰酸钾溶液氧化生成气体D,试写出该弱酸被氧化的离子方程式:_______ 。
(5)某兴趣小组用混合气体C还原少量CuO粉末,使CuO完全反应得到红色产物。为确定红色产物的成分,请设计实验方案:_______ 。(已知:Cu2O+2H+=Cu2++Cu+H2O)

已知:①混合气体C转化为气体D时,质量增加了4.8 g;②溶液H为单一溶质,且不与氢氧化钾反应,焰色反应呈紫色。请回答:
(1)盐A除Fe、H、O以外的两种元素是
(2)混合气体C的组成成分
(3)盐A在421~553℃下分解生成混合气体B和混合固体F的化学方程式:
(4)盐A中加入足量稀硫酸,可得到一种二元弱酸,且该弱酸可以被酸性高锰酸钾溶液氧化生成气体D,试写出该弱酸被氧化的离子方程式:
(5)某兴趣小组用混合气体C还原少量CuO粉末,使CuO完全反应得到红色产物。为确定红色产物的成分,请设计实验方案:
您最近一年使用:0次
2021-05-08更新
|
321次组卷
|
3卷引用:江西省景德镇市第一中学2021-2022学年高一上学期期中18班化学试题
江西省景德镇市第一中学2021-2022学年高一上学期期中18班化学试题浙江省温州市2021届普通高中高考5月适应性测试(三模)化学试题(已下线)考点15 铁及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)



