名校
解题方法
1 . 硫酸铜是一种重要的盐,下列说法不正确 的是
| A.可用于泳池的消毒 | B.可以用来检验酒精中是否含少量水 |
| C.可以和石灰乳混合配制农药波尔多液 | D.可以通过Cu与稀硫酸反应制备 |
您最近一年使用:0次
名校
解题方法
2 . 碱式碳酸铜[ ,相对分子质量为222]可用作有机催化剂。工业上以辉铜矿(主要成分为
,相对分子质量为222]可用作有机催化剂。工业上以辉铜矿(主要成分为 ,含
,含 及少量
及少量 )为原料制备碱式碳酸铜,工业流程如下:
)为原料制备碱式碳酸铜,工业流程如下:
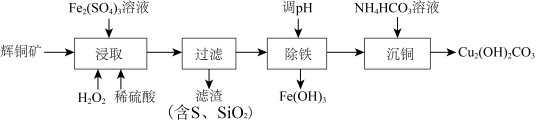
(1)“浸取”时能提高辉铜矿Cu浸取率的措施有___________ (填2条)
(2)某小组测得Cu浸取率随 浓度及温度影响的变化曲线如下:
浓度及温度影响的变化曲线如下:

①由图一可知 适宜的浓度范围为
适宜的浓度范围为___________ ;
②由图一中的a点分析,浸取时 也起到了氧化辉铜矿的作用,该反应的离子方程式为
也起到了氧化辉铜矿的作用,该反应的离子方程式为___________ 。
③图二中高于85℃时Cu浸取率下降的原因是___________ 。
(3)①“除铁”步骤调pH可加入试剂___________ (填选项字母);
a.HCl b.NaOH c.CuO d.
②常温下,“过滤”后的滤液中 ,则“除铁”步骤调pH应小于
,则“除铁”步骤调pH应小于___________ 。[常温下,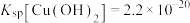 ]。
]。
(4)某实验小组为测定碱式碳酸铜的纯度,取制得的碱式碳酸铜产品5.0g,加适量硫酸,再加100mL水,加热溶解,冷却后配成250mL溶液。量取配成的25.00mL溶液于碘量瓶中,加入适量缓冲溶液控制溶液的pH在3~4之间,以及过量的碘化钾,摇匀,于暗处放置5分钟。用 的
的 溶液进行滴定,至临近滴定终点时再加入1mL淀粉溶液做指示剂,继续滴入
溶液进行滴定,至临近滴定终点时再加入1mL淀粉溶液做指示剂,继续滴入 溶液至滴定终点。平行测定3次,实验数据如下表所示。
溶液至滴定终点。平行测定3次,实验数据如下表所示。
已知: ,
,
①判断滴定到达终点的现象是___________ ;
②根据表中数据计算实验小组制得的碱式碳酸铜的纯度为___________ 。
(5)对下列几种假定情况进行讨论(填“偏高”、“偏低”或“无影响”);
①装 溶液的滴定管,滴定前尖嘴处有气泡,滴定后气泡消失,对测定结果的影响是
溶液的滴定管,滴定前尖嘴处有气泡,滴定后气泡消失,对测定结果的影响是___________ ;
②读 溶液体积时,若滴定前仰视,滴定后俯视,对测定结果的影响是
溶液体积时,若滴定前仰视,滴定后俯视,对测定结果的影响是___________ 。
 ,相对分子质量为222]可用作有机催化剂。工业上以辉铜矿(主要成分为
,相对分子质量为222]可用作有机催化剂。工业上以辉铜矿(主要成分为 ,含
,含 及少量
及少量 )为原料制备碱式碳酸铜,工业流程如下:
)为原料制备碱式碳酸铜,工业流程如下:
(1)“浸取”时能提高辉铜矿Cu浸取率的措施有
(2)某小组测得Cu浸取率随
 浓度及温度影响的变化曲线如下:
浓度及温度影响的变化曲线如下:
①由图一可知
 适宜的浓度范围为
适宜的浓度范围为②由图一中的a点分析,浸取时
 也起到了氧化辉铜矿的作用,该反应的离子方程式为
也起到了氧化辉铜矿的作用,该反应的离子方程式为③图二中高于85℃时Cu浸取率下降的原因是
(3)①“除铁”步骤调pH可加入试剂
a.HCl b.NaOH c.CuO d.

②常温下,“过滤”后的滤液中
 ,则“除铁”步骤调pH应小于
,则“除铁”步骤调pH应小于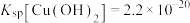 ]。
]。(4)某实验小组为测定碱式碳酸铜的纯度,取制得的碱式碳酸铜产品5.0g,加适量硫酸,再加100mL水,加热溶解,冷却后配成250mL溶液。量取配成的25.00mL溶液于碘量瓶中,加入适量缓冲溶液控制溶液的pH在3~4之间,以及过量的碘化钾,摇匀,于暗处放置5分钟。用
 的
的 溶液进行滴定,至临近滴定终点时再加入1mL淀粉溶液做指示剂,继续滴入
溶液进行滴定,至临近滴定终点时再加入1mL淀粉溶液做指示剂,继续滴入 溶液至滴定终点。平行测定3次,实验数据如下表所示。
溶液至滴定终点。平行测定3次,实验数据如下表所示。已知:
 ,
,
| 实验编号 | 滴定前 溶液的体积读数/mL 溶液的体积读数/mL | 滴定后 溶液的体积读数/mL 溶液的体积读数/mL |
| 1 | 0.10 | 20.12 |
| 2 | 1.20 | 23.21 |
| 3 | 1.50 | 21.48 |
②根据表中数据计算实验小组制得的碱式碳酸铜的纯度为
(5)对下列几种假定情况进行讨论(填“偏高”、“偏低”或“无影响”);
①装
 溶液的滴定管,滴定前尖嘴处有气泡,滴定后气泡消失,对测定结果的影响是
溶液的滴定管,滴定前尖嘴处有气泡,滴定后气泡消失,对测定结果的影响是②读
 溶液体积时,若滴定前仰视,滴定后俯视,对测定结果的影响是
溶液体积时,若滴定前仰视,滴定后俯视,对测定结果的影响是
您最近一年使用:0次
3 . 下列有关实验方案设计、现象和结论均正确的是
| 选项 | 实验方案 | 现象 | 结论 |
| A | 将滴有少量浓氨水的集气瓶倒扣在滴有少量浓硫酸的集气瓶上方 | 集气瓶内产生大量白烟 | 氨气和硫酸反应生成了硫酸铵 |
| B | 硫酸铜氨溶液中滴加少量硫酸 | 产生蓝色沉淀 | 硫酸根离子浓度增大,硫酸铜氨溶解度降低 |
| C | 将缠有锌条的铁钉置于装有少量食盐水的培养皿中,一段时间后,向铁钉附近滴加 溶液 溶液 | 未出现蓝色沉淀 | 锌条对铁钉起到保护作用 |
| D | 将5mL1-溴丁烷、15mL无水乙醇和2.0gNaOH混合,微热,并将产生气体通入 的 的 溶液 溶液 | 溴的四氯化碳溶液褪色 | 1-溴丁烷发生消去反应,生成1-丁烯 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 探究硫及其化合物的性质,下列方案设计、现象和结论都正确的是
| 选项 | 实验方案 | 现象 | 结论 |
| A | 往 固体中加入稀硫酸 固体中加入稀硫酸 | 产生蓝色溶液 | 不能说明稀硫酸具有强氧化性 |
| B | 往 溶液中通入 溶液中通入 ,再加入 ,再加入 溶液 溶液 | 产生白色沉淀 |  具有还原性 具有还原性 |
| C | 往 溶液中通入 溶液中通入 | 产生黑色沉淀 |  酸性强于 酸性强于 |
| D | 往紫色石蕊试液中通入 | 石蕊试液先变红后褪色 |  具有漂白性 具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 下列变化,能通过加盐酸一步反应实现的是
① Fe2O3→FeCl2 ②Cu→CuCl2 ③Cu(OH)2→CuCl2 ④Fe→FeCl3
① Fe2O3→FeCl2 ②Cu→CuCl2 ③Cu(OH)2→CuCl2 ④Fe→FeCl3
| A.① | B.② | C.③ | D.④ |
您最近一年使用:0次
2023-11-04更新
|
402次组卷
|
3卷引用:浙江省温州市瑞安十校联考2023-2024学年高一上学期期中化学试题
浙江省温州市瑞安十校联考2023-2024学年高一上学期期中化学试题浙江省温州市2023-2024学年瑞安市十校联考高一上学期化学期中试卷(已下线)专题03 铁 金属材料-【寒假自学课】2024年高一化学寒假提升学与练(人教版2019)
名校
6 . 下列物质对应的组成不正确 的是
A.干冰: | B.生石灰: |
C.胆矾: | D.小苏打: |
您最近一年使用:0次
2023-10-27更新
|
31次组卷
|
2卷引用:浙江省杭州市西湖高级中学2023-2024学年高一上学期10月月考化学试题
7 . 某研究小组探究白色难溶盐X(含五种元素,M<200 g•mol-1)的组成,进行如图实验:
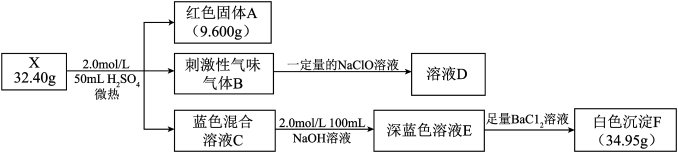
已知:固体A为常见单质:气体B能使品红褪色,实验测得气体体积为3.36L(标准状况),为防止污染环境,实验过程中用NaClO溶液吸收;溶液E中含有两种溶质,且阴离子相同。
请回答下列问题:
(1)X除含有H、O元素,还含有_________ 元素。
(2)混合溶液C中的溶质主要有_________ (填化学式)。
(3)可用气体B通入深蓝色溶液E制备X,写出相应的离子方程式________ 。
(4)设计实验方案证明吸收气体B的NaClO溶液已过量:_________ 。

已知:固体A为常见单质:气体B能使品红褪色,实验测得气体体积为3.36L(标准状况),为防止污染环境,实验过程中用NaClO溶液吸收;溶液E中含有两种溶质,且阴离子相同。
请回答下列问题:
(1)X除含有H、O元素,还含有
(2)混合溶液C中的溶质主要有
(3)可用气体B通入深蓝色溶液E制备X,写出相应的离子方程式
(4)设计实验方案证明吸收气体B的NaClO溶液已过量:
您最近一年使用:0次
名校
8 . 为探究固体化合物X(仅含两种元素,100 g/mol<M<200 g/mol)的组成和性质,设计并完成如下实验:
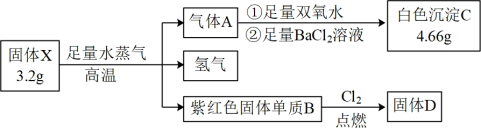
已知:气体A能使品红溶液褪色。请回答:
(1)固体D的化学式是___________ 。
(2)固体X的所含的元素是___________ 。(填元素符号)
(3)氢气是一种理想的绿色能源,点燃前须进行的操作是___________ 。
(4)写出气体A与双氧水反应的化学方程式___________ 。

已知:气体A能使品红溶液褪色。请回答:
(1)固体D的化学式是
(2)固体X的所含的元素是
(3)氢气是一种理想的绿色能源,点燃前须进行的操作是
(4)写出气体A与双氧水反应的化学方程式
您最近一年使用:0次
9 . 物质的性质决定用途,下列两者对应关系不正确 的是
A. 具有强氧化性,可用作消毒剂 具有强氧化性,可用作消毒剂 |
B. 固体具有氧化性,可作为黑火药的原料之一 固体具有氧化性,可作为黑火药的原料之一 |
| C.SiC中存在共价键,硬度大,可做砂纸和砂轮等磨料 |
D. 溶液呈蓝色,胆矾可以与石灰乳混合制备波尔多液 溶液呈蓝色,胆矾可以与石灰乳混合制备波尔多液 |
您最近一年使用:0次
解题方法
10 . 实验室以废铜屑为原料制取碱式碳酸铜[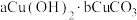 ]的流程如下:
]的流程如下:

已知:
①废铜屑的主要杂质有CuO、 、
、 、FeO和
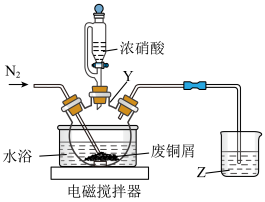
、FeO和 ,“酸浸”使用的装置如图;
,“酸浸”使用的装置如图;
②相关数据见下表:
请回答:
(1)仪器Y的名称是___________ ,溶液Z的作用是___________ 。
(2)流程中需要对滤液加热至70℃但又不宜过高,理由是___________ 。
(3)下列有关说法正确的是___________ 。
A.“酸浸”装置鼓入的 也可用空气代替
也可用空气代替
B.物质X可能是CuO、NaOH溶液或浓氨水
C.滤渣的主要成分是 、
、 、
、 和
和
D.流程中两次对溶液调pH,其调节范围和操作目的均不相同
E.“系列操作”包括了充分搅拌、趁热过滤、蒸馏水洗和灼烧等步骤
(4)可采用滴定法、热重分析法分别对碱式碳酸铜[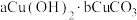 ]的组成进行分析。
]的组成进行分析。
①滴定法测定时需要用到酸式滴定管。其中,滴定步骤前可能需要的操作如下,请从中选出正确的操作并按序列出字母:______
向滴定管加蒸馏水并观察是否漏液______→______→______→______→______→______→在滴定管架上竖直放置,静置后读数
a.用蒸馏水洗涤滴定管,再用标准溶液润洗
b.将活塞旋转180°后静置观察
c.使滴定管略倾斜,捏住橡皮管内玻璃球赶走管尖气泡
d.向滴定管中加入标准液并高于“0”刻度
e.竖直滴定管,调整标准液液面低于“0”刻度
f.一手握住并倾斜滴定管,一手开关活塞赶走管尖气泡
②测得碱式碳酸铜[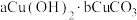 ]的热重分析结果如图所示,已知失重至65.7%时固体呈砖红色,则计算可知
]的热重分析结果如图所示,已知失重至65.7%时固体呈砖红色,则计算可知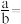
___________ (保留3位有效数字)。

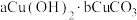 ]的流程如下:
]的流程如下:
已知:
①废铜屑的主要杂质有CuO、
 、
、 、FeO和
、FeO和 ,“酸浸”使用的装置如图;
,“酸浸”使用的装置如图;
②相关数据见下表:
| 物质 |  |  |  |  |
| 开始沉淀pH | 1.9 | 6.5 | 4.2 | 3.4 |
| 沉淀完全pH | 3.2 | 9.7 | 6.7 | 4.0 |
(1)仪器Y的名称是
(2)流程中需要对滤液加热至70℃但又不宜过高,理由是
(3)下列有关说法正确的是
A.“酸浸”装置鼓入的
 也可用空气代替
也可用空气代替B.物质X可能是CuO、NaOH溶液或浓氨水
C.滤渣的主要成分是
 、
、 、
、 和
和
D.流程中两次对溶液调pH,其调节范围和操作目的均不相同
E.“系列操作”包括了充分搅拌、趁热过滤、蒸馏水洗和灼烧等步骤
(4)可采用滴定法、热重分析法分别对碱式碳酸铜[
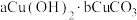 ]的组成进行分析。
]的组成进行分析。①滴定法测定时需要用到酸式滴定管。其中,滴定步骤前可能需要的操作如下,请从中选出正确的操作并按序列出字母:
向滴定管加蒸馏水并观察是否漏液______→______→______→______→______→______→在滴定管架上竖直放置,静置后读数
a.用蒸馏水洗涤滴定管,再用标准溶液润洗
b.将活塞旋转180°后静置观察
c.使滴定管略倾斜,捏住橡皮管内玻璃球赶走管尖气泡
d.向滴定管中加入标准液并高于“0”刻度
e.竖直滴定管,调整标准液液面低于“0”刻度
f.一手握住并倾斜滴定管,一手开关活塞赶走管尖气泡
②测得碱式碳酸铜[
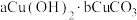 ]的热重分析结果如图所示,已知失重至65.7%时固体呈砖红色,则计算可知
]的热重分析结果如图所示,已知失重至65.7%时固体呈砖红色,则计算可知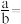

您最近一年使用:0次



