名校
解题方法
1 . Ⅰ.铁及铁的氧化物广泛应于生产、生活、航天、科研领域。
(1)铁的氧化物循环分解水制H2
已知:H2O(l)=H2(g)+1/2 O2(g) ΔH1=a kJ•mol-1
6FeO(s)+O2(g)=2Fe3O4(s) ΔH2=b kJ•mol-1
则:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH3=_______
(2)Fe2O3与CH4反应可制备“纳米级”金属铁。已知,恒温恒容时,加入Fe2O3与CH4发生反应:3CH4(g)+Fe2O3(s)⇌2Fe(s)+6H2(g)+3CO(g)
①此反应的化学平衡常数表达式为_______
②下列条件能判断该反应达到平衡状态的是_______
a.消耗1molFe2O3的同时,消耗3molCO
b.容器内气体的颜色不再改变
c.容器内压强不再改变
d.v正(CH4)=2v逆(H2)
Ⅱ.用CH4还原NO2的反应为CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g),向两个容积均为2L温度分别为T1、T2的恒温恒容密闭容器中分别加入1mol CH4和2mol NO2,测得各容器中n(NO2)随反应时间t的变化如图所示:
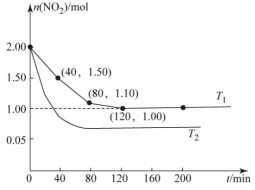
①T1_______ T2(填“>”或“<”)。
②T1时,40~80 min内,用N2的浓度变化表示的平均反应速率为v(N2)=_______
③T1下,200 min时,向容器中再加入CH4、NO2和H2O(g)各l mol,化学平衡_______ 移动(填“正向”“逆向”或“不”)。
Ⅲ.CaSO4微溶于水和酸,可加入氢氧化钠并通入CO2使其转化为CaCO3,然后加酸浸泡除去,反应的离子方程式为CaSO4+CO =CaCO3+SO
=CaCO3+SO ,室温下,该反应的化学平衡常数为
,室温下,该反应的化学平衡常数为_______ (室温下,Ksp(CaCO3)=3×10-9,Ksp(CaSO4)=9×10-6)。
(1)铁的氧化物循环分解水制H2
已知:H2O(l)=H2(g)+1/2 O2(g) ΔH1=a kJ•mol-1
6FeO(s)+O2(g)=2Fe3O4(s) ΔH2=b kJ•mol-1
则:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH3=
(2)Fe2O3与CH4反应可制备“纳米级”金属铁。已知,恒温恒容时,加入Fe2O3与CH4发生反应:3CH4(g)+Fe2O3(s)⇌2Fe(s)+6H2(g)+3CO(g)
①此反应的化学平衡常数表达式为
②下列条件能判断该反应达到平衡状态的是
a.消耗1molFe2O3的同时,消耗3molCO
b.容器内气体的颜色不再改变
c.容器内压强不再改变
d.v正(CH4)=2v逆(H2)
Ⅱ.用CH4还原NO2的反应为CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g),向两个容积均为2L温度分别为T1、T2的恒温恒容密闭容器中分别加入1mol CH4和2mol NO2,测得各容器中n(NO2)随反应时间t的变化如图所示:

①T1
②T1时,40~80 min内,用N2的浓度变化表示的平均反应速率为v(N2)=
③T1下,200 min时,向容器中再加入CH4、NO2和H2O(g)各l mol,化学平衡
Ⅲ.CaSO4微溶于水和酸,可加入氢氧化钠并通入CO2使其转化为CaCO3,然后加酸浸泡除去,反应的离子方程式为CaSO4+CO
 =CaCO3+SO
=CaCO3+SO ,室温下,该反应的化学平衡常数为
,室温下,该反应的化学平衡常数为
您最近一年使用:0次
2021-06-27更新
|
1003次组卷
|
8卷引用:四川省广安市2019-2020学年高二下学期期末(零诊)化学试题
四川省广安市2019-2020学年高二下学期期末(零诊)化学试题湖北省天门外国语学校2022-2023学年高二上学期12月月考化学试题(已下线)理综化学-2021年秋季高三开学摸底考试卷01(课标全国专用)2021年海南高考化学试题变式题11-19(已下线)备战2022年高考化学精准检测卷【全国卷】08广东省湛江市第二十一中学2021—2022学年高三上学期11月月考化学试题四川省资中县球溪高级中学2022-2023学年高三上学期10月月考化学试题四川省内江市威远中学校2022-2023学年高二下学期第二次阶段性考试理综化学试题
2 . 工业上除去电石渣浆 含
含 上清液中的
上清液中的 ,并制取石膏
,并制取石膏 的常用流程如下:
的常用流程如下:

下列说法正确的是
 含
含 上清液中的
上清液中的 ,并制取石膏
,并制取石膏 的常用流程如下:
的常用流程如下:
下列说法正确的是

A. 、 、 在过程Ⅰ、Ⅱ中均起催化剂作用 在过程Ⅰ、Ⅱ中均起催化剂作用 |
B.过程Ⅰ中,反应的离子方程式为 |
C.将10L上清液中的 转化为 转化为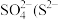 浓度为480 mg·L−1),理论上共需要0.03mol的 浓度为480 mg·L−1),理论上共需要0.03mol的 |
D.常温下,56gCaO溶于水配成1L溶液,溶液中 的数目为 的数目为 个 个 |
您最近一年使用:0次
2021-01-02更新
|
549次组卷
|
5卷引用:安徽省示范高中皖北协作区2020年第22届高三联考理科综合化学
安徽省示范高中皖北协作区2020年第22届高三联考理科综合化学(已下线)小题必刷08 氧化还原反应的规律及应用——2021年高考化学一轮复习小题必刷(通用版)江西省南昌市新建区第二中学2019-2020学年高二下学期期终考试化学试题湖北省龙泉中学、宜昌一中2021届高三下学期2月联合考试化学试题黑龙江省大庆实验中学实验一部2020-2021学年高一下学期开学考试化学试题
名校
解题方法
3 . 研究发现Pd2团簇可催化CO的氧化,在催化过程中路径不同可能生成不同的过渡态和中间产物(过渡态已标出),下图为路径1和路径2催化的能量变化。下列说法的不正确的是
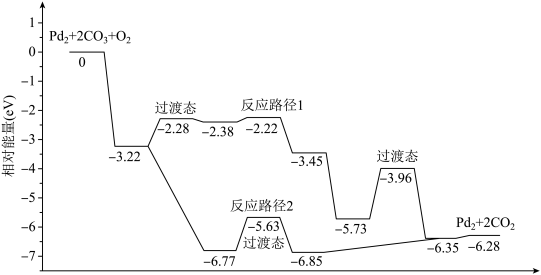

| A.该过程中有极性键和非极性键的断裂和生成 |
| B.反应路径2的催化效果更好 |
| C.催化剂不会改变整个反应的ΔH |
| D.路径1中最大能垒(活化能)E正=1.23eV |
您最近一年使用:0次
2020-12-08更新
|
1113次组卷
|
7卷引用:湖北省武汉市东西湖区华中师范大学第一附属中学2021届高三上学期期中考试化学试题
名校
4 . 某研究小组探究催化剂对CO、NO转化的影响。将含NO和CO的尾气以一定的流速通过两种不同的催化剂进行反应:2NO(g)+2CO(g)  N2(g)+2CO2(g),ΔH<0,相同时间内测量逸出气体中NO含量, 从而确定尾气脱氮率(脱氮率即NO的转化率),结果如下图所示。以下说法正确的是( )
N2(g)+2CO2(g),ΔH<0,相同时间内测量逸出气体中NO含量, 从而确定尾气脱氮率(脱氮率即NO的转化率),结果如下图所示。以下说法正确的是( )
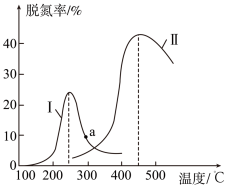
①两种催化剂均能降低活化能,但ΔH不变
②相同条件下,改变压强对脱氮率没有影响
③曲线Ⅱ中的催化剂适用于450 ℃左右脱氮
④曲线Ⅱ中催化剂脱氮率比曲线Ⅰ中的高
⑤ a 点是对应温度下的平衡脱氮率
⑥若低于200 ℃,图中曲线Ⅰ脱氮率随温度升高而变化不大的主要原因是催化剂的活性不高
 N2(g)+2CO2(g),ΔH<0,相同时间内测量逸出气体中NO含量, 从而确定尾气脱氮率(脱氮率即NO的转化率),结果如下图所示。以下说法正确的是( )
N2(g)+2CO2(g),ΔH<0,相同时间内测量逸出气体中NO含量, 从而确定尾气脱氮率(脱氮率即NO的转化率),结果如下图所示。以下说法正确的是( )
①两种催化剂均能降低活化能,但ΔH不变
②相同条件下,改变压强对脱氮率没有影响
③曲线Ⅱ中的催化剂适用于450 ℃左右脱氮
④曲线Ⅱ中催化剂脱氮率比曲线Ⅰ中的高
⑤ a 点是对应温度下的平衡脱氮率
⑥若低于200 ℃,图中曲线Ⅰ脱氮率随温度升高而变化不大的主要原因是催化剂的活性不高
| A.①③⑥ | B.①③④ | C.②③④ | D.①③⑤ |
您最近一年使用:0次
解题方法
5 . 据文献报道:Fe(CO)5催化某反应的一种反应机理如图所示。下列叙述正确的是( )
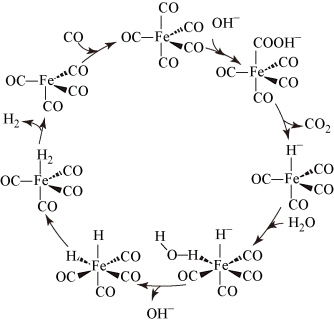

| A.该反应可消耗温室气体CO2 |
| B.OH- 作为中间产物参与了该催化循环 |
| C.该催化循环中Fe的成键数目发生了变化 |
| D.该反应可产生清洁燃料H2 |
您最近一年使用:0次
6 . “绿水青山就是金山银山”,研究碳、氮、硫等大气污染物和水污染物的处理对建设美丽中国具有重要意义。
(1)已知:①NO2(g)+CO(g) CO2(g)+NO(g) △H=-232.0 kJ·mol-1
CO2(g)+NO(g) △H=-232.0 kJ·mol-1
②N2(g)+O2(g) 2NO(g) △H=+180.0 kJ·mol-1
2NO(g) △H=+180.0 kJ·mol-1
③2NO(g)+O2(g) 2NO2(g) △H=-122.2 kJ·mol-1
2NO2(g) △H=-122.2 kJ·mol-1
则NO与CO反应生成无污染物气体的热化学方程式为__________ 。
(2)工业上用CO与H2制备甲醇可消除CO污染,其反应为:CO(g)+2H2(g) CH3OH(g)。某温度下,将1 mol CO与2 mol H2充入体积为1 L的恒容密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下:
CH3OH(g)。某温度下,将1 mol CO与2 mol H2充入体积为1 L的恒容密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下:
①若P前=9.00MPa,则该反应的平衡常数Kp=_____ MPa-2(用平衡分压代替平衡浓度计算,分压=总压×体积分数);
②若平衡后再向容器中充入1 mol CO与2 mol H2,则重新平衡后CO的体积分数与原平衡相比___ (填“增大”、“不变”、“减小”)。
(3)甲醇碱性燃料电池因性能优异而被人们青睐,请写出其负极的电极反应式:_____ 。
(4)工业上常用过量浓氨水吸收硫酸工业尾气SO2,请写出其离子方程式_____ 。
(1)已知:①NO2(g)+CO(g)
 CO2(g)+NO(g) △H=-232.0 kJ·mol-1
CO2(g)+NO(g) △H=-232.0 kJ·mol-1②N2(g)+O2(g)
 2NO(g) △H=+180.0 kJ·mol-1
2NO(g) △H=+180.0 kJ·mol-1③2NO(g)+O2(g)
 2NO2(g) △H=-122.2 kJ·mol-1
2NO2(g) △H=-122.2 kJ·mol-1则NO与CO反应生成无污染物气体的热化学方程式为
(2)工业上用CO与H2制备甲醇可消除CO污染,其反应为:CO(g)+2H2(g)
 CH3OH(g)。某温度下,将1 mol CO与2 mol H2充入体积为1 L的恒容密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下:
CH3OH(g)。某温度下,将1 mol CO与2 mol H2充入体积为1 L的恒容密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下:| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| P后/P前 | 0.75 | 0.62 | 0.52 | 0.44 | 0.40 | 0.40 |
①若P前=9.00MPa,则该反应的平衡常数Kp=
②若平衡后再向容器中充入1 mol CO与2 mol H2,则重新平衡后CO的体积分数与原平衡相比
(3)甲醇碱性燃料电池因性能优异而被人们青睐,请写出其负极的电极反应式:
(4)工业上常用过量浓氨水吸收硫酸工业尾气SO2,请写出其离子方程式
您最近一年使用:0次
解题方法
7 . 乙炔、乙烯均是重要的化工原料。回答下列问题:
(1)1902年,Sabatier首次发现,常压下过渡金属可以催化含有双键或叁键的气态烃的加氢反应。
①已知:C2H2(g)+H2(g)→C2H4ΔH1=—174.3kJ•mol-1 K1(300K)=3.37×1024
C2H2(g)+2H2(g)→C2H6ΔH2=—311.0kJ•mol-1 K2(300K)=1.19×1042
则反应C2H4(g)+H2(g)→C2H6的ΔH=____________ kJ•mol-1,K(300K)=____________ (保留三位有效数字)
②2010年Sheth等得出乙炔在Pd表面选择加氢的反应机理(如图)。其中吸附在Pd表面上的物种用*标注。

上述吸附反应为____________ (填“放热”或“吸热”)反应,该历程中最大能垒(活化能)为____________ kJ•mol-1,该步骤的化学方程式为____________ 。
(2)在恒容密闭容器中充入乙烯,一定条件下发生反应C2H4(g) C2H2(g)+H2(g)。
C2H2(g)+H2(g)。
①乙烯的离解率为α,平衡时容器内气体总压强为p总,则分压p(C2H4)=____________ (用p总和α表示)。
②在1000K时,该反应的Kp=2×10-3atm,平衡时容器内气体的总压强为10atm,则乙烯的离解率为____________ (精确到0.001,已知 ≈1.4)。
≈1.4)。
(3)用如图装置电解含CO2的某酸性废水溶液,阴极产物中含有乙烯。

该分离膜为____________ (填“阳”或“阴”)离子选择性交换膜;生成乙烯的电极反应式为____________ 。
(1)1902年,Sabatier首次发现,常压下过渡金属可以催化含有双键或叁键的气态烃的加氢反应。
①已知:C2H2(g)+H2(g)→C2H4ΔH1=—174.3kJ•mol-1 K1(300K)=3.37×1024
C2H2(g)+2H2(g)→C2H6ΔH2=—311.0kJ•mol-1 K2(300K)=1.19×1042
则反应C2H4(g)+H2(g)→C2H6的ΔH=
②2010年Sheth等得出乙炔在Pd表面选择加氢的反应机理(如图)。其中吸附在Pd表面上的物种用*标注。

上述吸附反应为
(2)在恒容密闭容器中充入乙烯,一定条件下发生反应C2H4(g)
 C2H2(g)+H2(g)。
C2H2(g)+H2(g)。①乙烯的离解率为α,平衡时容器内气体总压强为p总,则分压p(C2H4)=
②在1000K时,该反应的Kp=2×10-3atm,平衡时容器内气体的总压强为10atm,则乙烯的离解率为
 ≈1.4)。
≈1.4)。(3)用如图装置电解含CO2的某酸性废水溶液,阴极产物中含有乙烯。

该分离膜为
您最近一年使用:0次
名校
解题方法
8 . 将煤转化为水煤气的主要化学反应为C(s)+H2O(g) CO(g)+H2(g);C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为
CO(g)+H2(g);C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为
C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ•mol-1
H2(g)+ O2(g)=H2O(g) ΔH=-242.0 kJ•mol-1
CO(g)+ O2(g)=CO2(g) ΔH=-283.0 kJ•mol-1
(1)根据以上数据,写出C(s)与水蒸气反应的热化学方程式:_______ 。
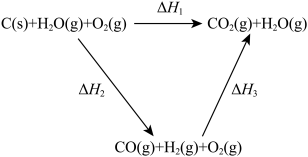
(2)比较反应热数据可知,1 mol CO(g)和1 mol H2(g)完全燃烧放出的热量之和比1 mol C(s)完全燃烧放出的热量多。甲同学据此认为“煤转化为水煤气可以使煤燃烧放出更多的热量”;乙同学根据盖斯定律做出下列循环图,并据此认为“煤转化为水煤气再燃烧放出的热量与煤直接燃烧放出的热量相等”。请分析:甲、乙两同学观点正确的是_____ (填“甲”或“乙”);判断的理由是________ 。
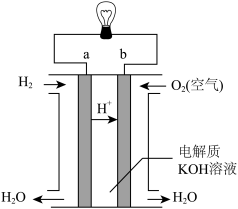
(3)CO、H2等可燃性气体可以设计成燃料电池,燃料电池是一种能量转化率较高的发电装置。如图是一种氢氧燃料电池示意图,则该电池a极的电极反应式为________ 。若将H2换成CH4,则该电池负极的电极反应式为 _______ 。
 CO(g)+H2(g);C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为
CO(g)+H2(g);C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为 C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ•mol-1
H2(g)+ O2(g)=H2O(g) ΔH=-242.0 kJ•mol-1
CO(g)+ O2(g)=CO2(g) ΔH=-283.0 kJ•mol-1
(1)根据以上数据,写出C(s)与水蒸气反应的热化学方程式:
(2)比较反应热数据可知,1 mol CO(g)和1 mol H2(g)完全燃烧放出的热量之和比1 mol C(s)完全燃烧放出的热量多。甲同学据此认为“煤转化为水煤气可以使煤燃烧放出更多的热量”;乙同学根据盖斯定律做出下列循环图,并据此认为“煤转化为水煤气再燃烧放出的热量与煤直接燃烧放出的热量相等”。请分析:甲、乙两同学观点正确的是

(3)CO、H2等可燃性气体可以设计成燃料电池,燃料电池是一种能量转化率较高的发电装置。如图是一种氢氧燃料电池示意图,则该电池a极的电极反应式为

您最近一年使用:0次
9 . 据文献报道:Fe(CO)5催化某反应的一种反应机理如下图所示。下列叙述错误的是


| A.OH-参与了该催化循环 | B.该反应可产生清洁燃料H2 |
| C.该反应可消耗温室气体CO2 | D.该催化循环中Fe的成键数目发生变化 |
您最近一年使用:0次
2020-07-08更新
|
13757次组卷
|
60卷引用:2020年全国统一考试化学试题(新课标Ⅱ)
2020年全国统一考试化学试题(新课标Ⅱ)(已下线)专题07 化学反应中的能量变化-2020年高考真题和模拟题化学分项汇编(已下线)第八单元 化学反应与能量测试题-2021年高考化学一轮复习名师精讲练黑龙江省大庆实验中学2021届高三8月开学考试化学试题北京二中2020-2021学年高二上学期10月月考化学试题北京首都师范大学附属中学2020-2021学年高二上学期期中考试化学试题山东省泰安市宁阳一中2021届高三上学期模块考试化学试题广东省惠州市惠州中学2021届高三12月月考化学试题湖北省华中师范大学第一附属中学2020-2021学年高一下学期期末考试化学试题2020年全国卷Ⅱ化学真题变式题(已下线)热点10 新信息反应机理分析-2021年高考化学专练【热点·重点·难点】(已下线)专题10 化学平衡(速率、影响因素、图像、标志、平衡压强及常数)-2021年高考化学必做热点专题(已下线)专题05 化学反应与能量——备战2021年高考化学纠错笔记北京市昌平区新学道临川学校2021届高三上学期期末考试化学试题(已下线)热点7 新信息反应机理分析-2021年高考化学【热点·重点·难点】专练(山东专用)黑龙江省大庆市实验中学实验一部2020-2021学年高一下学期4月阶段性教学质量检测化学试题安徽省阜阳市2020-2021学年高二下学期段考化学试题(已下线)押全国卷理综第13题 反应机理图分析、能垒图分析等创新题型及阿伏伽德罗常数-备战2021年高考化学临考题号押题(课标全国卷)山西省长治市第二中学校2020-2021学年高二下学期期中考试化学试题(已下线)押山东卷第13题 陌生反应机理选择题-备战2021年高考化学临考题号押题(山东卷)广西桂林市第十八中学2020-2021学年高一下学期期中考试化学试题江西省景德镇一中2020-2021学年高二下学期期末考试化学(2班)试题(已下线)课时27 微粒间作用力-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点01 物质的组成、性质和分类-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点01 物质的组成、性质和分类-备战2022年高考化学一轮复习考点帮(浙江专用)吉林省延边第二中学2020-2021学年高二下学期第二次考试月考化学试题甘肃省兰州市第二十七中学2020-2021学年高二下学期期末考试化学试题陕西省瑞泉中学2021-2022学年高三上学期第一次质量检测化学试题新疆生产建设兵团第九师龙珍高级中学2021-2022学年高三上学期第一次月考化学试题辽宁省大连市第一中学2021-2022学年高二上学期阶段性学情反馈(二)化学试题云南省峨山彝族自治县第一中学2021-2022学年高二上学期期中考试化学试题(已下线)专题09 反应机理—2022年高考化学二轮复习讲练测(全国版)-练习江苏省天一中学2021-2022学年高一上学期期末考试化学(强化班)试题(已下线)秘籍08 反应历程探究与催化原理图象分析-备战2022年高考化学抢分秘籍(全国通用)福建省南安市侨光中学、昌财实验中学2021-2022学年高二下学期第4次联考(期中)化学试题(已下线)押全国卷理综第13题 反应机理图分析、能垒图分析等创新题型及阿伏加德罗常数-备战2022年高考化学临考题号押题(全国卷)(已下线)查补易混易错点01 物质的组成、性质、分类及化学用语-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)回归教材重难点05 化学反应中的能量变化-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题07化学反应中的能量变化及反应机理-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题07化学反应中的能量变化及反应机理-五年(2018~2022)高考真题汇编(全国卷)浙江省宁波市2021-2022学年高二下学期九校联考化学试题(已下线)考点01 物质的分类和转化-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点17 化学反应的热效应-备战2023年高考化学一轮复习考点帮(全国通用)黑龙江省哈尔滨师范大学附属中学2022-2023学年高三9月月考化学试题(已下线)第18讲 化学反应速率(讲)-2023年高考化学一轮复习讲练测(新教材新高考)辽宁省锦州市锦州中学2023届高三上学期9月月考化学试题云南省临沧市民族中学2022-2023学年高二上学期第二次月考化学试题广东省广州天省实验学校2021-2022学年高二下学期6月月考化学试题黑龙江省双鸭山市饶河县高级中学2021-2022学年高二下学期期中考试化学试题新疆乌鲁木齐市第七十中学2022-2023学年高二上学期期中考试化学试题辽宁省兴城市高级中学2022-2023学年高二上学期期末线上质量检测化学试题(已下线)专题13 反应微观机理分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第一部分 二轮专题突破 题型专攻3 化学反应历程图像分析江苏省南通市海安高级中学2022-2023学年高一下学期第一次月考化学试题(已下线)专题10 物质的反应及转化广东省梅州市兴宁市齐昌中学2022-2023学年高三上学期第二次质检考试化学试题北京市中国人民大学附属中学2023-2024学年高三上学期11月统练三 化学试题河北省石家庄市第十七中学2023-2024高二上学期期末考试化学试题
10 . 甲酸被认为是理想的氢能载体,我国科技工作者运用DFT计算研究单分子HCOOH在催化剂表面分解产生H2的反应历程如图所示,其中吸附在催化剂表面的物种用*标注。

回答下列问题:
(1)该历程中决速步骤的能垒(活化能)E正=__________ eV,该步骤的反应方程式为__________ 。
(2)甲酸分解制氢气的热化学方程式为__________ 。
(3)在温度为383K、压强为p0时,将一定量的HCOOH气体充入一个盛有催化剂的刚性容器中,达到平衡时,H2的分压为0.55p0,则该反应α(HCOOH)=______________ ,该温度下的压强平衡常数Kp=__________ (计算结果保留2位有效数字)。
(4)HCOOH的分解存在副反应HCOOH(g) CO(g)+H2O(g)。
CO(g)+H2O(g)。
已知H2的选择性= 能够增大H2选择性的可能方法是
能够增大H2选择性的可能方法是____ 。
(5)甲酸作为直接燃料电池的燃料具有能量密度高的优点。若电解质溶液显酸性,甲酸直接燃料电池的负极反应式为__________ ,该电池的理论输出电压为1.48V,能量密度E=________ kW·h/kg(能量密度=电池输出电能/燃料质量,1kW·h=3.6×106J)。

回答下列问题:
(1)该历程中决速步骤的能垒(活化能)E正=
(2)甲酸分解制氢气的热化学方程式为
(3)在温度为383K、压强为p0时,将一定量的HCOOH气体充入一个盛有催化剂的刚性容器中,达到平衡时,H2的分压为0.55p0,则该反应α(HCOOH)=
(4)HCOOH的分解存在副反应HCOOH(g)
 CO(g)+H2O(g)。
CO(g)+H2O(g)。已知H2的选择性=
 能够增大H2选择性的可能方法是
能够增大H2选择性的可能方法是(5)甲酸作为直接燃料电池的燃料具有能量密度高的优点。若电解质溶液显酸性,甲酸直接燃料电池的负极反应式为
您最近一年使用:0次



