1 . 据文献报道:Fe(CO)5催化某反应的一种反应机理如下图所示。下列叙述错误的是


| A.OH-参与了该催化循环 | B.该反应可产生清洁燃料H2 |
| C.该反应可消耗温室气体CO2 | D.该催化循环中Fe的成键数目发生变化 |
您最近一年使用:0次
2020-07-08更新
|
13757次组卷
|
60卷引用:2020年全国统一考试化学试题(新课标Ⅱ)
2020年全国统一考试化学试题(新课标Ⅱ)(已下线)专题07 化学反应中的能量变化-2020年高考真题和模拟题化学分项汇编(已下线)第八单元 化学反应与能量测试题-2021年高考化学一轮复习名师精讲练北京二中2020-2021学年高二上学期10月月考化学试题北京首都师范大学附属中学2020-2021学年高二上学期期中考试化学试题广东省惠州市惠州中学2021届高三12月月考化学试题2020年全国卷Ⅱ化学真题变式题黑龙江省大庆实验中学2021届高三8月开学考试化学试题山东省泰安市宁阳一中2021届高三上学期模块考试化学试题(已下线)热点10 新信息反应机理分析-2021年高考化学专练【热点·重点·难点】(已下线)专题10 化学平衡(速率、影响因素、图像、标志、平衡压强及常数)-2021年高考化学必做热点专题(已下线)专题05 化学反应与能量——备战2021年高考化学纠错笔记北京市昌平区新学道临川学校2021届高三上学期期末考试化学试题安徽省阜阳市2020-2021学年高二下学期段考化学试题(已下线)押全国卷理综第13题 反应机理图分析、能垒图分析等创新题型及阿伏伽德罗常数-备战2021年高考化学临考题号押题(课标全国卷)山西省长治市第二中学校2020-2021学年高二下学期期中考试化学试题(已下线)课时27 微粒间作用力-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点01 物质的组成、性质和分类-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(全国通用)甘肃省兰州市第二十七中学2020-2021学年高二下学期期末考试化学试题陕西省瑞泉中学2021-2022学年高三上学期第一次质量检测化学试题辽宁省大连市第一中学2021-2022学年高二上学期阶段性学情反馈(二)化学试题湖北省华中师范大学第一附属中学2020-2021学年高一下学期期末考试化学试题(已下线)专题09 反应机理—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)秘籍08 反应历程探究与催化原理图象分析-备战2022年高考化学抢分秘籍(全国通用)(已下线)押全国卷理综第13题 反应机理图分析、能垒图分析等创新题型及阿伏加德罗常数-备战2022年高考化学临考题号押题(全国卷)(已下线)查补易混易错点01 物质的组成、性质、分类及化学用语-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)回归教材重难点05 化学反应中的能量变化-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题07化学反应中的能量变化及反应机理-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题07化学反应中的能量变化及反应机理-五年(2018~2022)高考真题汇编(全国卷)(已下线)考点01 物质的分类和转化-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点17 化学反应的热效应-备战2023年高考化学一轮复习考点帮(全国通用)黑龙江省哈尔滨师范大学附属中学2022-2023学年高三9月月考化学试题(已下线)第18讲 化学反应速率(讲)-2023年高考化学一轮复习讲练测(新教材新高考)辽宁省锦州市锦州中学2023届高三上学期9月月考化学试题广东省广州天省实验学校2021-2022学年高二下学期6月月考化学试题新疆乌鲁木齐市第七十中学2022-2023学年高二上学期期中考试化学试题辽宁省兴城市高级中学2022-2023学年高二上学期期末线上质量检测化学试题(已下线)专题13 反应微观机理分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第一部分 二轮专题突破 题型专攻3 化学反应历程图像分析(已下线)专题10 物质的反应及转化广东省梅州市兴宁市齐昌中学2022-2023学年高三上学期第二次质检考试化学试题北京市中国人民大学附属中学2023-2024学年高三上学期11月统练三 化学试题河北省石家庄市第十七中学2023-2024高二上学期期末考试化学试题(已下线)热点7 新信息反应机理分析-2021年高考化学【热点·重点·难点】专练(山东专用)黑龙江省大庆市实验中学实验一部2020-2021学年高一下学期4月阶段性教学质量检测化学试题(已下线)押山东卷第13题 陌生反应机理选择题-备战2021年高考化学临考题号押题(山东卷)广西桂林市第十八中学2020-2021学年高一下学期期中考试化学试题江西省景德镇一中2020-2021学年高二下学期期末考试化学(2班)试题(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点01 物质的组成、性质和分类-备战2022年高考化学一轮复习考点帮(浙江专用)吉林省延边第二中学2020-2021学年高二下学期第二次考试月考化学试题新疆生产建设兵团第九师龙珍高级中学2021-2022学年高三上学期第一次月考化学试题云南省峨山彝族自治县第一中学2021-2022学年高二上学期期中考试化学试题江苏省天一中学2021-2022学年高一上学期期末考试化学(强化班)试题福建省南安市侨光中学、昌财实验中学2021-2022学年高二下学期第4次联考(期中)化学试题浙江省宁波市2021-2022学年高二下学期九校联考化学试题云南省临沧市民族中学2022-2023学年高二上学期第二次月考化学试题黑龙江省双鸭山市饶河县高级中学2021-2022学年高二下学期期中考试化学试题江苏省南通市海安高级中学2022-2023学年高一下学期第一次月考化学试题
2 . 铑的配合物离子[Rh(CO)2I2]-可催化甲醇羰基化,反应过程如图所示。
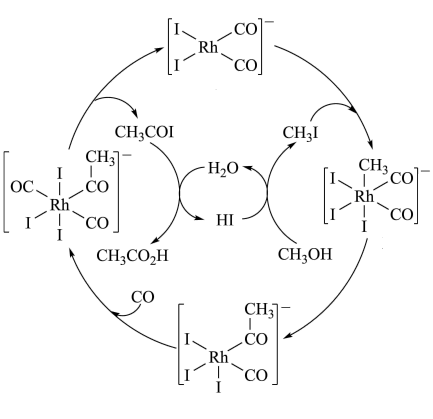
| A.CH3COI是反应中间体 |
| B.甲醇羰基化反应为CH3OH+CO=CH3CO2H |
| C.反应过程中Rh的成键数目保持不变 |
| D.存在反应CH3OH+HI=CH3I+H2O |
您最近一年使用:0次
2020-07-08更新
|
17480次组卷
|
48卷引用:2020年全国统一考试化学试题(新课标Ⅰ)
2020年全国统一考试化学试题(新课标Ⅰ)(已下线)专题07 化学反应中的能量变化-2020年高考真题和模拟题化学分项汇编(已下线)第13讲 原子结构和化学键-2021年高考化学一轮复习名师精讲练河南省郑州市巩义市第四高级中学2021届高三上学期期中考试化学试题(已下线)小题必刷21 原子结构与化学键——2021年高考化学一轮复习小题必刷(通用版)2020年全国卷Ⅰ理综化学高考真题变式题(已下线)热点10 新信息反应机理分析-2021年高考化学专练【热点·重点·难点】(已下线)专题10 化学平衡(速率、影响因素、图像、标志、平衡压强及常数)-2021年高考化学必做热点专题(已下线)专题05 化学反应与能量——备战2021年高考化学纠错笔记(已下线)押全国卷理综第13题 反应机理图分析、能垒图分析等创新题型及阿伏伽德罗常数-备战2021年高考化学临考题号押题(课标全国卷)天津市和平区2020-2021学年高二下学期期末考试化学试题(已下线)课时27 微粒间作用力-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点01 物质的组成、性质和分类-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点38 烃的含氧衍生物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)一轮巩固卷4-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(北京专用)(已下线)专题09 反应机理—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)卷08 元素周期律-【小题小卷】冲刺2022年高考化学小题限时集训(全国卷专用)(已下线)秘籍08 反应历程探究与催化原理图象分析-备战2022年高考化学抢分秘籍(全国通用)安徽省合肥市普通高中六校联盟2021-2022学年高二下学期期中联考化学试题(已下线)押全国卷理综第13题 反应机理图分析、能垒图分析等创新题型及阿伏加德罗常数-备战2022年高考化学临考题号押题(全国卷)(已下线)查补易混易错点01 物质的组成、性质、分类及化学用语-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题07化学反应中的能量变化及反应机理-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题07化学反应中的能量变化及反应机理-五年(2018~2022)高考真题汇编(全国卷)北京市中国人民大学附属中学2022届高三下学期第三次适应性练习化学试题(已下线)考点01 物质的分类和转化-备战2023年高考化学一轮复习考点帮(全国通用)专题1 揭示物质结构的奥秘 ★第一~三单元综合拔高练四川省内江市第六中学2021-2022学年高二下学期入学考试(创新班)化学试题新疆岳普湖县2021-2022学年高二下学期第一次学情调研测试化学试题(已下线)第18讲 化学反应速率(讲)-2023年高考化学一轮复习讲练测(新教材新高考)河南省洛阳市新安县第一高级中学2022-2023学年高三上学期入学测试(实验小班)化学试题北京市中国人民大学附属中学2022-2023学年高三上学期统练6化学试题(已下线)专题13 反应微观机理分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第一部分 二轮专题突破 题型专攻3 化学反应历程图像分析内蒙古赤峰二中2022-2023学年高二下学期第一次月考化学试题(已下线)专题10 物质的反应及转化(已下线)热点题型训练 催化剂与反应历程(机理)(已下线)T12-物质反应及转化江苏省南京市人民中学 海安实验中学 句容三中2023-2024学年高二下学期3月月考化学试题(已下线)热点7 新信息反应机理分析-2021年高考化学【热点·重点·难点】专练(山东专用)(已下线)考点01 物质的组成、性质和分类-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点38 卤代烃 醇 酚-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点39 醛 羧酸 酯-备战2022年高考化学一轮复习考点帮(浙江专用)黑龙江省大庆市东风中学2022-2023学年高三上学期第一次月考化学试题湖南省邵阳市洞口县第一中学2021-2022学年高三下学期第三次模拟考试化学试题(已下线)广东省深圳中学2023届高三年级上学期第二次阶段测试化学试题(A卷)黑龙江省哈尔滨市第一二二中学2021-2022学年高三假期检验性考试化学试题广东省2021届高三下学期模拟预热化学试题广东省汕头市金山中学2023-2024学年高二上学期10月阶段考试 化学 Word版含答案
3 . 水煤气变换[CO(g)+H2O(g)=CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。回答下列问题:
(1)Shibata曾做过下列实验:①使纯H2缓慢地通过处于721 ℃下的过量氧化钴CoO(s),氧化钴部分被还原为金属钴(Co),平衡后气体中H2的物质的量分数为0.0250。
②在同一温度下用CO还原CoO(s),平衡后气体中CO的物质的量分数为0.0192。
根据上述实验结果判断,还原CoO(s)为Co(s)的倾向是CO_________ H2(填“大于”或“小于”)。
(2)721 ℃时,在密闭容器中将等物质的量的CO(g)和H2O(g)混合,采用适当的催化剂进行反应,则平衡时体系中H2的物质的量分数为_________ (填标号)。
A.<0.25 B.0.25 C.0.25~0.50 D.0.50 E.>0.50
(3)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用 标注。
标注。
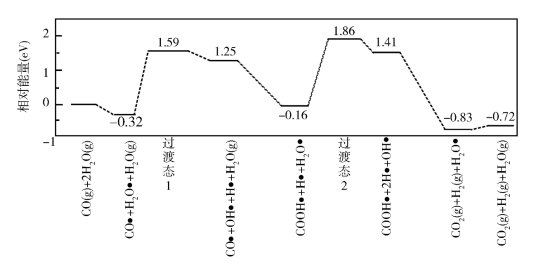
可知水煤气变换的ΔH________ 0(填“大于”“等于”或“小于”),该历程中最大能垒(活化能)E正=_________ eV,写出该步骤的化学方程式_______________________ 。
(4)Shoichi研究了467 ℃、489 ℃时水煤气变换中CO和H2分压随时间变化关系(如下图所示),催化剂为氧化铁,实验初始时体系中的PH2O和PCO相等、PCO2和PH2相等。
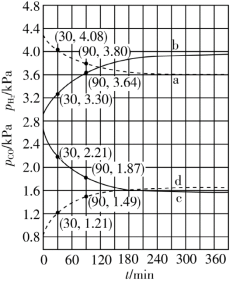
计算曲线a的反应在30~90 min内的平均速率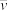 (a)=
(a)=___________ kPa·min−1。467 ℃时PH2和PCO随时间变化关系的曲线分别是___________ 、___________ 。489 ℃时PH2和PCO随时间变化关系的曲线分别是___________ 、___________ 。
(1)Shibata曾做过下列实验:①使纯H2缓慢地通过处于721 ℃下的过量氧化钴CoO(s),氧化钴部分被还原为金属钴(Co),平衡后气体中H2的物质的量分数为0.0250。
②在同一温度下用CO还原CoO(s),平衡后气体中CO的物质的量分数为0.0192。
根据上述实验结果判断,还原CoO(s)为Co(s)的倾向是CO
(2)721 ℃时,在密闭容器中将等物质的量的CO(g)和H2O(g)混合,采用适当的催化剂进行反应,则平衡时体系中H2的物质的量分数为
A.<0.25 B.0.25 C.0.25~0.50 D.0.50 E.>0.50
(3)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用
 标注。
标注。
可知水煤气变换的ΔH
(4)Shoichi研究了467 ℃、489 ℃时水煤气变换中CO和H2分压随时间变化关系(如下图所示),催化剂为氧化铁,实验初始时体系中的PH2O和PCO相等、PCO2和PH2相等。

计算曲线a的反应在30~90 min内的平均速率
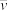 (a)=
(a)=
您最近一年使用:0次
2019-06-09更新
|
19228次组卷
|
20卷引用:2019年全国统一考试化学试题(新课标Ⅰ)
2019年全国统一考试化学试题(新课标Ⅰ)(已下线)专题09 反应速率、化学平衡——2019年高考真题和模拟题化学分项汇编安徽省阜阳市颍上二中等三校2020届高三上学期入学考试化学试题(已下线)专题7.1 化学反应速率(讲)-《2020年高考一轮复习讲练测》(已下线)专题7.1 化学反应速率(练)-《2020年高考一轮复习讲练测》专题2.2 化学反应速率和化学平衡(综合提升卷)——巅峰冲刺2020年高考化学二轮专项提升(已下线)专题6.3 化学原理题(必考)(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升鲁科版(2019)选择性必修1第2章 化学反应的方向、限度与速率 第2章 综合检测高中必刷题高二选择性必修1第二章 化学反应速率与化学平衡 第二章素养检测人教版(2019)高二化学选择性必修1第二章 化学反应速率与化学平衡 过高考 3年真题强化闯关鲁科版(2019)高二选择性必修第一册第2章 化学反应的方向、限度与速率 高考挑战区 过高考福建省泉州市泉港区第一中学2019-2020学年高二上学期第二次月考化学试题湖南省株洲市茶陵二中2020届高三上学期第二次月考化学试题(已下线)专题06 化学反应速率和化学平衡——备战2021年高考化学纠错笔记(已下线)专题12 化学反应原理综合题—2022年高考化学二轮复习讲练测(全国版)-讲义(已下线)专题15化学反应原理综合-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题17 原理综合题(已下线)T28-原理综合题2018-2019学年度耀华实验学校第二学期高二实验化学期末试卷江苏省盱眙中学2021-2022学年高二上学期第三次学情调研化学试题
真题
解题方法
4 . 下表列出了3种燃煤烟气脱硫方法的原理。
(1) 方法Ⅰ中氨水吸收燃煤烟气中 的化学反应为:
的化学反应为:

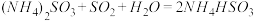
能提高燃煤烟气中 去除率的措施有
去除率的措施有__________ (填字母)。
A.增大氨水浓度 B.升高反应温度
C.使燃煤烟气与氨水充分接触 D. 通入空气使HSO3-转化为SO42-
采用方法Ⅰ脱硫,并不需要预先除去燃煤烟气中大量的 ,原因是
,原因是________ (用离子方程式表示)。
(2)方法Ⅱ重要发生了下列反应:
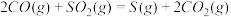 ∆H=8.0kJ/mol
∆H=8.0kJ/mol
 ∆H=90.4kJ/mol
∆H=90.4kJ/mol
 ∆H=-566.0kJ/mol
∆H=-566.0kJ/mol
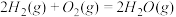 ∆H=-483.6kJ/mol
∆H=-483.6kJ/mol
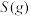 与
与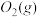 反应生成
反应生成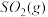 的热化学方程式为
的热化学方程式为_____________ 。
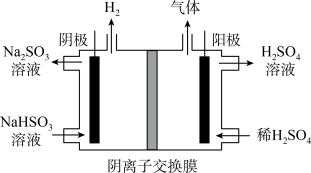
(3) 方法Ⅲ中用惰性电极电解 溶液的装置如上图所示。阳极区放出气体的成分为
溶液的装置如上图所示。阳极区放出气体的成分为______________ 。(填化学式)
| 方法I | 用氨水将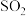 转化为 转化为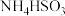 ,再氧化成( ,再氧化成(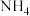 ) )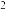 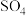 |
| 方法II | 用生物质热解气(主要成分CO、 、 、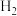 )将 )将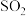 在高温下还原成单质硫 在高温下还原成单质硫 |
| 方法III | 用 溶液吸收 溶液吸收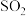 ,再经电解转化为 ,再经电解转化为 |
 的化学反应为:
的化学反应为:
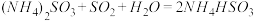
能提高燃煤烟气中
 去除率的措施有
去除率的措施有A.增大氨水浓度 B.升高反应温度
C.使燃煤烟气与氨水充分接触 D. 通入空气使HSO3-转化为SO42-
采用方法Ⅰ脱硫,并不需要预先除去燃煤烟气中大量的
 ,原因是
,原因是(2)方法Ⅱ重要发生了下列反应:
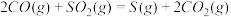 ∆H=8.0kJ/mol
∆H=8.0kJ/mol ∆H=90.4kJ/mol
∆H=90.4kJ/mol ∆H=-566.0kJ/mol
∆H=-566.0kJ/mol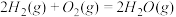 ∆H=-483.6kJ/mol
∆H=-483.6kJ/mol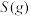 与
与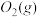 反应生成
反应生成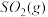 的热化学方程式为
的热化学方程式为
(3) 方法Ⅲ中用惰性电极电解
 溶液的装置如上图所示。阳极区放出气体的成分为
溶液的装置如上图所示。阳极区放出气体的成分为
您最近一年使用:0次
2019-01-30更新
|
204次组卷
|
4卷引用:2010年高考化学试题分项专题一 化学与STS
5 . 采用N2O5为硝化剂是一种新型的绿色硝化技术,在含能材料、医药等工业中得到广泛应用。回答下列问题
(1)1840年 Devil用干燥的氯气通过干燥的硝酸银,得到N2O5。该反应的氧化产物是一种气体,其分子式为___________ 。
(2)F.Daniels等曾利用测压法在刚性反应器中研究了25℃时N2O5(g)分解反应:
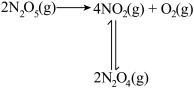
其中NO2二聚为N2O4的反应可以迅速达到平衡。体系的总压强p随时间t的变化如下表所示(t=∞时,N2O5(g)完全分解):
①已知:2N2O5(g)=2N2O4(g)+O2(g) ΔH1=−4.4 kJ·mol−1
2NO2(g)=N2O4(g) ΔH 2=−55.3 kJ·mol−1
则反应N2O5(g)=2NO2(g)+ O2(g)的ΔH=
O2(g)的ΔH=_______ kJ·mol−1。
②研究表明,N2O5(g)分解的反应速率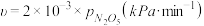 。t=62 min时,测得体系中pO2=2.9 kPa,则此时的
。t=62 min时,测得体系中pO2=2.9 kPa,则此时的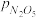 =
=________ kPa,v=_______ kPa·min−1。
③若提高反应温度至35℃,则N2O5(g)完全分解后体系压强p∞(35℃)____ 63.1 kPa(填“大于”“等于”或“小于”),原因是________ 。
④25℃时N2O4(g) 2NO2(g)反应的平衡常数Kp=
2NO2(g)反应的平衡常数Kp=_______ kPa(Kp为以分压表示的平衡常数,计算结果保留1位小数)。
(3)对于反应2N2O5(g)→4NO2(g)+O2(g),R.A.Ogg提出如下反应历程:
第一步 N2O5 NO2+NO3快速平衡
NO2+NO3快速平衡
第二步 NO2+NO3→NO+NO2+O2慢反应
第三步 NO+NO3→2NO2快反应
其中可近似认为第二步反应不影响第一步的平衡。下列表述正确的是_______ (填标号)。
A.v(第一步的逆反应)>v(第二步反应)
B.反应的中间产物只有NO3
C.第二步中NO2与NO3的碰撞仅部分有效
D.第三步反应活化能较高
(1)1840年 Devil用干燥的氯气通过干燥的硝酸银,得到N2O5。该反应的氧化产物是一种气体,其分子式为
(2)F.Daniels等曾利用测压法在刚性反应器中研究了25℃时N2O5(g)分解反应:

其中NO2二聚为N2O4的反应可以迅速达到平衡。体系的总压强p随时间t的变化如下表所示(t=∞时,N2O5(g)完全分解):
| t/min | 0 | 40 | 80 | 160 | 260 | 1300 | 1700 | ∞ |
| p/kPa | 35.8 | 40.3 | 42.5. | 45.9 | 49.2 | 61.2 | 62.3 | 63.1 |
2NO2(g)=N2O4(g) ΔH 2=−55.3 kJ·mol−1
则反应N2O5(g)=2NO2(g)+
 O2(g)的ΔH=
O2(g)的ΔH=②研究表明,N2O5(g)分解的反应速率
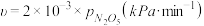 。t=62 min时,测得体系中pO2=2.9 kPa,则此时的
。t=62 min时,测得体系中pO2=2.9 kPa,则此时的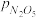 =
=③若提高反应温度至35℃,则N2O5(g)完全分解后体系压强p∞(35℃)
④25℃时N2O4(g)
 2NO2(g)反应的平衡常数Kp=
2NO2(g)反应的平衡常数Kp=(3)对于反应2N2O5(g)→4NO2(g)+O2(g),R.A.Ogg提出如下反应历程:
第一步 N2O5
 NO2+NO3快速平衡
NO2+NO3快速平衡第二步 NO2+NO3→NO+NO2+O2慢反应
第三步 NO+NO3→2NO2快反应
其中可近似认为第二步反应不影响第一步的平衡。下列表述正确的是
A.v(第一步的逆反应)>v(第二步反应)
B.反应的中间产物只有NO3
C.第二步中NO2与NO3的碰撞仅部分有效
D.第三步反应活化能较高
您最近一年使用:0次
2018-06-09更新
|
14023次组卷
|
12卷引用:2018年全国普通高等学校招生统一考试化学(新课标I卷)
2018年全国普通高等学校招生统一考试化学(新课标I卷)【全国百强校】四川省棠湖中学2017-2018学年高二下学期期末考试理综化学试题(已下线)2018年高考题及模拟题汇编 专题14 化学反应原理综合(已下线)高考母题题源13 基本概念、基本理论综合一(已下线)2019年高考总复习巅峰冲刺-专题06 化学反应速率、化学平衡问题应试策略【全国百强校】河南省南阳市第一中学2018-2019学年高二下学期第四次月考化学试题鲁科版(2019)选择性必修1 第2章 化学反应的方向、限度与速率 章末综合检测卷云南省元阳县第一中学2020届高三上学期开学考试化学试题(已下线)专题15化学反应原理综合-五年(2018~2022)高考真题汇编(全国卷)(已下线)先机卷 01 -【热题狂飙】2023年高考化学样卷(全国卷专用)四川省江油市太白中学2023-2024学年高二上学期12月考试化学试题江西省安福中学2021-2022学年高二上学期开学考试化学(理)试题
真题
名校
6 . 三氯氢硅(SiHCl3)是制备硅烷、多晶硅的重要原料。回答下列问题:
(1)SiHCl3在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成(HSiO)2O等,写出该反应的化学方程式__________ 。
(2)SiHCl3在催化剂作用下发生反应:
2SiHCl3(g) SiH2Cl2(g)+ SiCl4(g) ΔH1=48 kJ·mol−1
SiH2Cl2(g)+ SiCl4(g) ΔH1=48 kJ·mol−1
3SiH2Cl2(g) SiH4(g)+2SiHCl3 (g) ΔH2=−30 kJ·mol−1
SiH4(g)+2SiHCl3 (g) ΔH2=−30 kJ·mol−1
则反应4SiHCl3(g) SiH4(g)+ 3SiCl4(g)的ΔH=
SiH4(g)+ 3SiCl4(g)的ΔH=__________ kJ·mol−1。
(3)对于反应2SiHCl3(g) SiH2Cl2(g)+SiCl4(g),采用大孔弱碱性阴离子交换树脂催化剂,在323 K和343 K时SiHCl3的转化率随时间变化的结果如图所示。
SiH2Cl2(g)+SiCl4(g),采用大孔弱碱性阴离子交换树脂催化剂,在323 K和343 K时SiHCl3的转化率随时间变化的结果如图所示。
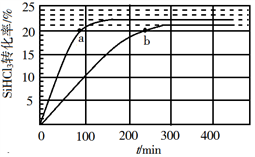
①343 K时反应的平衡转化率α=_________ %。平衡常数K343 K=__________ (保留2位小数)。
②在343 K下:要提高SiHCl3转化率,可采取的措施是___________ ;要缩短反应达到平衡的时间,可采取的措施有____________ 、___________ 。
③比较a、b处反应速率大小:υa________ υb(填“大于”“小于”或“等于”)。反应速率υ=υ正−υ逆=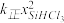 −
− ,k正、k逆分别为正、逆向反应速率常数,x为物质的量分数,计算a处
,k正、k逆分别为正、逆向反应速率常数,x为物质的量分数,计算a处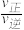 =
=__________ (保留1位小数)。
(1)SiHCl3在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成(HSiO)2O等,写出该反应的化学方程式
(2)SiHCl3在催化剂作用下发生反应:
2SiHCl3(g)
 SiH2Cl2(g)+ SiCl4(g) ΔH1=48 kJ·mol−1
SiH2Cl2(g)+ SiCl4(g) ΔH1=48 kJ·mol−13SiH2Cl2(g)
 SiH4(g)+2SiHCl3 (g) ΔH2=−30 kJ·mol−1
SiH4(g)+2SiHCl3 (g) ΔH2=−30 kJ·mol−1则反应4SiHCl3(g)
 SiH4(g)+ 3SiCl4(g)的ΔH=
SiH4(g)+ 3SiCl4(g)的ΔH=(3)对于反应2SiHCl3(g)
 SiH2Cl2(g)+SiCl4(g),采用大孔弱碱性阴离子交换树脂催化剂,在323 K和343 K时SiHCl3的转化率随时间变化的结果如图所示。
SiH2Cl2(g)+SiCl4(g),采用大孔弱碱性阴离子交换树脂催化剂,在323 K和343 K时SiHCl3的转化率随时间变化的结果如图所示。
①343 K时反应的平衡转化率α=
②在343 K下:要提高SiHCl3转化率,可采取的措施是
③比较a、b处反应速率大小:υa
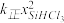 −
− ,k正、k逆分别为正、逆向反应速率常数,x为物质的量分数,计算a处
,k正、k逆分别为正、逆向反应速率常数,x为物质的量分数,计算a处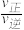 =
=
您最近一年使用:0次
2018-06-09更新
|
11969次组卷
|
8卷引用:2018年全国普通高等学校招生统一考试化学(新课标III卷)
真题
解题方法
7 . 接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:
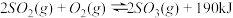
(1)该反应所用的催化剂是___ (填写化合物名称),该反应450℃时的平衡常数_____ 500℃时的平衡常数(填“大于”、“小于”或“等于”)。
(2)该热化学反应方程式的意义是____________ .
(3)下列描述中能表明该反应已达平衡状态的是________
A.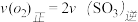 B.容器中气体的平均分子量不随时间而变化
B.容器中气体的平均分子量不随时间而变化
C.容器中气体的密度不随时间而变化D.容器中气体的分子总数不随时间而变化
(4)在一个固定容积为5L的密闭容器中充入0.20 mol 和0.10mol
和0.10mol ,半分钟后达到平衡,测得容器中含
,半分钟后达到平衡,测得容器中含 0.18mol,则
0.18mol,则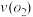 =
=______  :若继续通入0.20mol
:若继续通入0.20mol 和0.10mol
和0.10mol ,则平衡
,则平衡______ 移动(填“向正反应方向”、“向逆反应方向” 或“不”),再次达到平衡后,______ mol<n( )<
)<______ mol。
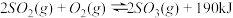
(1)该反应所用的催化剂是
(2)该热化学反应方程式的意义是
(3)下列描述中能表明该反应已达平衡状态的是
A.
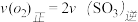 B.容器中气体的平均分子量不随时间而变化
B.容器中气体的平均分子量不随时间而变化C.容器中气体的密度不随时间而变化D.容器中气体的分子总数不随时间而变化
(4)在一个固定容积为5L的密闭容器中充入0.20 mol
 和0.10mol
和0.10mol ,半分钟后达到平衡,测得容器中含
,半分钟后达到平衡,测得容器中含 0.18mol,则
0.18mol,则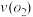 =
= :若继续通入0.20mol
:若继续通入0.20mol 和0.10mol
和0.10mol ,则平衡
,则平衡 )<
)<
您最近一年使用:0次
真题
8 . 工业上电解饱和食盐水能制取多种化工原料,其中部分原料可用于制备多晶硅。

(1)上图是离子交换膜法电解饱和食盐水示意图,电解槽阳极产生的气体是________ ;NaOH溶液的出口为________ (填字母);精制饱和食盐水的进口为________ (填字母);干燥塔中应使用的液体是________ 。
(2)多晶硅主要采用SiHCl3还原工艺生产,其副产物SiCl4的综合利用受到广泛关注。
①SiCl4可制气相白炭黑(与光导纤维主要原料相同),方法为高温下SiCl4与H2和O2反应,产物有两种,化学方程式为___________________________________ 。
②SiCl4可转化为SiHCl3而循环使用,一定条件下,在20 L恒容密闭容器中的反应:
3SiCl4(g)+2H2(g)+Si(s) 4SiHCl3(g)
4SiHCl3(g)
达平衡后,H2和SiHCl3物质的量浓度分别为0.140 mol/L和0.020 mol/L,若H2全部来源于离子交换膜法的电解产物,理论上需消耗纯NaCl的质量为________ kg。
(3)采用无膜电解槽电解饱和食盐水,可制取氯酸钠,同时生成氢气,现制得氯酸钠213.0 kg,则生成氢气________ m3(标准状况)。

(1)上图是离子交换膜法电解饱和食盐水示意图,电解槽阳极产生的气体是
(2)多晶硅主要采用SiHCl3还原工艺生产,其副产物SiCl4的综合利用受到广泛关注。
①SiCl4可制气相白炭黑(与光导纤维主要原料相同),方法为高温下SiCl4与H2和O2反应,产物有两种,化学方程式为
②SiCl4可转化为SiHCl3而循环使用,一定条件下,在20 L恒容密闭容器中的反应:
3SiCl4(g)+2H2(g)+Si(s)
 4SiHCl3(g)
4SiHCl3(g)达平衡后,H2和SiHCl3物质的量浓度分别为0.140 mol/L和0.020 mol/L,若H2全部来源于离子交换膜法的电解产物,理论上需消耗纯NaCl的质量为
(3)采用无膜电解槽电解饱和食盐水,可制取氯酸钠,同时生成氢气,现制得氯酸钠213.0 kg,则生成氢气
您最近一年使用:0次
2016-12-09更新
|
48次组卷
|
4卷引用:2009年高考真题汇编-卤 素



