1 . 下列说法正确的是
| A.反应3C(s)+CaO(s) =CaC2(s)+CO(g)在常温下不能自发进行,说明该反应的ΔH>0 |
B.同温同压下, 在光照和点燃条件的 在光照和点燃条件的 不同 不同 |
| C.夏天,打开啤酒瓶时会在瓶口逸出气体,不可以用勒夏特列原理加以解释 |
D.恒温恒压容器中发生反应N2+O2 2NO,若在容器中充入He,正逆反应的速率均不变 2NO,若在容器中充入He,正逆反应的速率均不变 |
您最近一年使用:0次
2022-11-12更新
|
103次组卷
|
2卷引用:福建省龙岩市一级校联盟(九校)联考2022-2023学年高二上学期半期考化学试题
名校
解题方法
2 . 己二酸是一种二元弱酸,通常为白色结晶体,微溶于冷水,易溶于热水和乙醇。实验室中常用碱性KMnO4溶液氧化环己醇(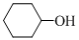 )来制取己二酸
)来制取己二酸 。发生的主要反应可表示为
。发生的主要反应可表示为
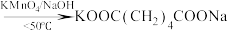
 。
。
具体操作步骤如下:
I.向烧杯中加入5mL 10%氢氧化钠溶液和50mL水,边搅拌边加入9g KMnO4 (可适当加热),待KMnO4溶解后,将溶液转入仪器A中,再向仪器C中加入2.1mL(0.02mol)环己醇,按下图所示连接好装置。

II.打开仪器C中的活塞,控制滴加速度,待环己醇滴加完毕反应温度开始下降时,将仪器A加热煮沸8min,用玻璃棒蘸取溶液点在滤纸上做点滴实验,若出现紫色环,可加入适量的亚硫酸氢钠,趁热抽滤混合物,用少量热水洗涤滤渣(MnO2)2~3次,合并滤液和洗涤液,加热浓缩至原体积的一半左右(溶液微黄),冷却至室温。
III.滴加浓盐酸酸化,加入少量活性炭,加热煮沸,越热抽滤,滤液经一系列操作后得白色晶体1.95g。已知:不同温度下,几种物质在水中的溶解度如下表所示。
回答下列问题:
(1)上图中仪器A的名称为_______ ;仪器B中冷却水的进水口是_______ (填“a”或“b”)。
(2)步骤II中,随环己醇滴速的不同,溶液温度随时间的变化曲线如下图所示,则在实验过程中应选择曲线_______ 对应的滴速,理由是_______ 。

(3)步骤II中加入饱和亚硫酸氢钠溶液的作用是_______ 。
(4)步骤III加浓盐酸酸化时有大量气泡产生,推测该气体是_______ (填化学式)。
(5)步骤III中“一系列操作”包括_______ 、过滤、洗涤、干燥、称量;若己二酸晶体中含有氯化钠,则提纯己二酸的方法是_______ 。
(6)该实验中,己二酸的产率为_______ (保留4位有效数字)。
 )来制取己二酸
)来制取己二酸 。发生的主要反应可表示为
。发生的主要反应可表示为
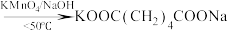
 。
。具体操作步骤如下:
I.向烧杯中加入5mL 10%氢氧化钠溶液和50mL水,边搅拌边加入9g KMnO4 (可适当加热),待KMnO4溶解后,将溶液转入仪器A中,再向仪器C中加入2.1mL(0.02mol)环己醇,按下图所示连接好装置。

II.打开仪器C中的活塞,控制滴加速度,待环己醇滴加完毕反应温度开始下降时,将仪器A加热煮沸8min,用玻璃棒蘸取溶液点在滤纸上做点滴实验,若出现紫色环,可加入适量的亚硫酸氢钠,趁热抽滤混合物,用少量热水洗涤滤渣(MnO2)2~3次,合并滤液和洗涤液,加热浓缩至原体积的一半左右(溶液微黄),冷却至室温。
III.滴加浓盐酸酸化,加入少量活性炭,加热煮沸,越热抽滤,滤液经一系列操作后得白色晶体1.95g。已知:不同温度下,几种物质在水中的溶解度如下表所示。
| 物质 | 己二酸 | 氯化钠 | 氯化钾 |
| 25℃时溶解度/g | 2.1 | 36.1 | 34.3 |
| 70℃时溶解度/g | 38 | 37.8 | 48 |
| 100℃时溶解度/g | 160 | 39.5 | 56.3 |
(1)上图中仪器A的名称为
(2)步骤II中,随环己醇滴速的不同,溶液温度随时间的变化曲线如下图所示,则在实验过程中应选择曲线

(3)步骤II中加入饱和亚硫酸氢钠溶液的作用是
(4)步骤III加浓盐酸酸化时有大量气泡产生,推测该气体是
(5)步骤III中“一系列操作”包括
(6)该实验中,己二酸的产率为
您最近一年使用:0次
名校
解题方法
3 . 某种含二价铜微粒[CuII(OH)(NH3)]+的催化剂可用于汽车尾气脱硝,催化机理如图1,反应过程中不同态物质体系所含的能量如图2。下列说法正确的是
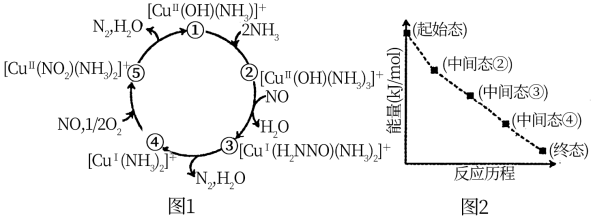

| A.总反应焓变ΔH>0 |
| B.由状态②到状③是铜元素被氧化的过程 |
| C.状态③到状态④的变化过程中有O—H键的形成 |
| D.该脱硝过程的总反应方程式为4NH3+2NO+2O2=6H2O+3N2 |
您最近一年使用:0次
2021-03-08更新
|
267次组卷
|
3卷引用:福建省龙岩市2021届高三毕业班第一次教学质量检测化学试题
解题方法
4 . 反应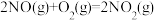 分两步进行,其反应过程的能量变化示意图如图。
分两步进行,其反应过程的能量变化示意图如图。

Ⅰ. △H1
△H1
Ⅱ. △H2
△H2
下列说法正确的是
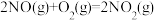 分两步进行,其反应过程的能量变化示意图如图。
分两步进行,其反应过程的能量变化示意图如图。
Ⅰ.
 △H1
△H1Ⅱ.
 △H2
△H2下列说法正确的是
| A.△H1=Ea1 |
| B.化学反应速率:Ⅱ>Ⅰ |
C.2molNO的总键能小于1mol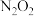 的总键能 的总键能 |
| D.△H2>△H1 |
您最近一年使用:0次
名校
5 . 已知在298K、100kPa下,2NO(g)+2CO(g)=N2(g)+2CO2(g) ΔH=-113kJ·mol-1,ΔS=-145J·mol-1·K-1。下列说法中错误的是
| A.该反应中反应物的总能量高于生成物的总能量 |
| B.该反应常温下不能自发进行,因此需要高温和催化剂 |
| C.该反应体系的混乱度减小 |
| D.增加CO的浓度,可加快反应速率 |
您最近一年使用:0次
名校
解题方法
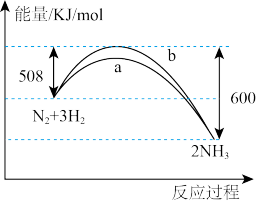
6 . 298K时,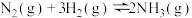
 ;反应过程中能量变化曲线如图所示(两条曲线分别表示使用或不使用催化剂)。下列叙述
;反应过程中能量变化曲线如图所示(两条曲线分别表示使用或不使用催化剂)。下列叙述错误 的是
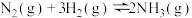
 ;反应过程中能量变化曲线如图所示(两条曲线分别表示使用或不使用催化剂)。下列叙述
;反应过程中能量变化曲线如图所示(两条曲线分别表示使用或不使用催化剂)。下列叙述
| A.加入催化剂,不能提高N2的转化率 |
| B.a曲线是加入催化剂时的能量变化曲线 |
C. |
D.是否使用催化剂, 的数值不受影响 的数值不受影响 |
您最近一年使用:0次
2020-08-10更新
|
80次组卷
|
2卷引用:福建省龙岩市一级达标校2019-2020学年高二下学期期末质检化学试题
名校
解题方法
7 . 某反应A→C反应进程曲线如图所示,下列叙述正确的是
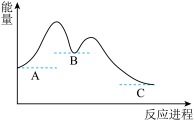

| A.B的能量最低 |
| B.反应过程中两个阶段均放出热量 |
| C.反应A→C的条件一定为加热 |
| D.反应A→C属于放热反应 |
您最近一年使用:0次
2020-07-27更新
|
169次组卷
|
4卷引用:福建省连城县第一中学2021-2022学年高二上学期第一次月考化学试题
名校
解题方法
8 . 根据如下能量关系示意图,下列说法正确的是
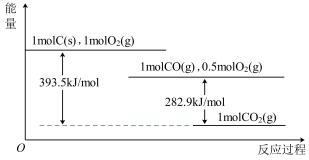

| A.1 mol C(s)与1 mol O2(g)的能量之和为393.5 kJ |
| B.由C→CO的热化学方程式为:2C(s)+O2(g) = 2CO(g) ΔH= −221.2 kJ∙mol−1 |
| C.反应2CO(g)+O2(g) =2CO2(g)中,生成物的总能量大于反应物的总能量 |
| D.将1 mol C(s)磨成粉末后,反应更加剧烈,说明粉碎可以改变ΔH |
您最近一年使用:0次
2020-06-28更新
|
172次组卷
|
3卷引用:福建省龙岩第一中学2021-2022学年高二上学期开学考试化学试题
名校
9 . 联氨(N2H4)常温下为无色液体,可用作火箭燃料。下列说法不正确的是
①2O2(g)+N2(g)=N2O4(l) ΔH1
②N2(g)+2H2(g)= N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2 N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ΔH4=−1048.9 kJ·mol-1
①2O2(g)+N2(g)=N2O4(l) ΔH1
②N2(g)+2H2(g)= N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2 N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ΔH4=−1048.9 kJ·mol-1
| A.ΔH4﹦2ΔH3−2ΔH2−ΔH1 |
B.O2(g)+2H2(g) 2H2O(l) ΔH5,ΔH5>ΔH3 2H2O(l) ΔH5,ΔH5>ΔH3 |
| C.1 mol O2(g)和 2 mol H2(g)具有的总能量高于 2 mol H2O(g) |
| D.联氨和 N2O4 作火箭推进剂的原因之一是反应放出大量的热且产物无污染 |
您最近一年使用:0次
2019-10-20更新
|
289次组卷
|
20卷引用:福建省武平县第一中学2021-2022学年高二上学期第一次月考化学试题
福建省武平县第一中学2021-2022学年高二上学期第一次月考化学试题江苏省徐州市2018届高三考前模拟检测化学试题(已下线)2018年高考题及模拟题汇编 专题07 化学反应中的能量变化甘肃省师范大学附属中学2018-2019学年高二上学期第一次月考化学试题【全国百强校】福建省莆田市第一中学2018-2019学年高二上学期第一次月考化学试题(已下线)2018年11月浙江省普通高校招生选考科目考试化学仿真模拟试卷03(已下线)2019年1月浙江省普通高中学业水平考试化学仿真模拟试题03浙江省杭州市富阳区新登中学2018-2019学年高二上学期期末模拟化学试题福建省三明市第一中学2019-2020学年高二上学期第一次月考化学试题吉林省靖宇县一中2019-2020学年上学期高二9月月考化学试题河北省沧州市肃宁县第一中学2019-2020学年高二上学期第三次月考化学试题福建省三明第一中学2020-2021学年高二上学期第一次月考化学试题河北省沧州市肃宁县第一中学2020-2021学年高二上学期第一次月考化学试题江西省赣州市会昌县会昌中学2020-2021学年高二上学期第一次月考化学试题重庆市铁路中学校2020-2021学年高二上学期11月月考化学试题安徽省合肥市合肥九中2020-2021学年高二上学期10月摸底考化学试题福建省将乐县第一中学2021-2022学年高二上学期第一次月考化学试题江苏省宿迁市北大附属宿迁实验学校2022-2023学年高二上学期开学考试化学试题福建省宁德市第一中学2021-2022学年高二上学期9月月考化学试题江苏省苏州市实验中学2023-2024学年高二上学期10月月考化学试题
名校
解题方法
10 . 已知H2(g)+2ICl(g)=I2(g)+2HCl(g),该反应分①、②两步进行,其能量曲线如图所示, 已知:ICl中氯为-1价,碘为+1价。下列有关说法正确的是


| A.反应①为吸热反应 |
| B.反应①和②均是同种元素间发生的氧化还原反应 |
| C.反应①比反应②的速率慢,与相应正反应的活化能有关 |
| D.HI(g)+ICl(g)=I2(g)+HCl(g) △H=-218 kJ/mol |
您最近一年使用:0次
2019-10-08更新
|
146次组卷
|
8卷引用:福建省漳平市第一中学2019-2020学年高二上学期第一次月考化学试题



