1 . 下列图示与化学用语表述内容不相符 的是
| A.牺牲阳极法实验 | B.AgCl沉淀转化为AgI沉淀 | C.锌铜原电池 | D.H2与Cl2反应过程中焓的变化 |
 |  |  |  |
| 正极:2H2O+O2+4e-= 4OH- | I-(aq)+AgCl(s) AgI(s)+Cl-(aq) AgI(s)+Cl-(aq) | Zn + Cu2+= Zn2+ + Cu | H2(g)+Cl2(g)= 2HCl(g) < |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-01-19更新
|
168次组卷
|
2卷引用:北京市西城区2023-2024学年高二上学期期末考试化学试题
名校
解题方法
2 . 其它条件不变,增大反应物浓度能加快反应速率的主要原因是
| A.活化分子能量明显增加 | B.增加了单位体积内分子总数 |
| C.增加了活化分子的百分数 | D.改变了反应的 |
您最近一年使用:0次
3 . 现有如下3个热化学方程式:
H2(g)+ O2(g)=H2O(g) ΔH1=-akJ/mo ①
O2(g)=H2O(g) ΔH1=-akJ/mo ①
H2(g)+ O2(g)=H2O(l) ΔH2=-bkJ/mol ②
O2(g)=H2O(l) ΔH2=-bkJ/mol ②
2H2(g)+O2(g)=2H2O(l) ΔH3=-ckJ/mol ③
则由下表所列的原因能推导出后面结论的是
H2(g)+
 O2(g)=H2O(g) ΔH1=-akJ/mo ①
O2(g)=H2O(g) ΔH1=-akJ/mo ①H2(g)+
 O2(g)=H2O(l) ΔH2=-bkJ/mol ②
O2(g)=H2O(l) ΔH2=-bkJ/mol ②2H2(g)+O2(g)=2H2O(l) ΔH3=-ckJ/mol ③
则由下表所列的原因能推导出后面结论的是
| 选项 | 原因 | 结论 |
| A | H2的燃烧是放热反应 | a、b、c均大于0 |
| B | ①和②中物质的化学计量数均相同 | a=b |
| C | ③中H2O的状态不同,化学计最数不同 | a、b、c不会有任何等量或不等量关系 |
| D | ③的化学计量数是②的2倍 | ΔH2<ΔH1 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 研究催化剂对 反应速率的影响。恒温、恒容时,
反应速率的影响。恒温、恒容时, 随时间的变化如下。
随时间的变化如下。
下列说法不正确 的是
 反应速率的影响。恒温、恒容时,
反应速率的影响。恒温、恒容时, 随时间的变化如下。
随时间的变化如下。| 时间/min 催化剂  | 0 | 20 | 40 | 60 | 80 |
| 催化剂Ⅰ | 2.40 | 2.00 | 1.60 | 1.20 | 0.80 |
| 催化剂Ⅱ | 2.40 | 1.60 | 0.80 | 0.40 | 0.40 |
A.使用催化剂I,0~20min平均反应速率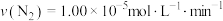 |
B.使用催化剂Ⅱ,达平衡后容器内的压强是初始时的 倍 倍 |
| C.相同条件下,使用催化剂I和催化剂Ⅱ的反应热相同 |
| D.相同条件下,使用催化剂Ⅱ可使该反应的化学平衡常数更大 |
您最近一年使用:0次
5 . 合成氨是人类科技发展史上的一项重大突破。
(1)在一定条件下,N2(g)和H2(g)反应生成0.2 molNH3(g),放出9.24kJ的热量。在下图中画出合成氨反应中用焓(H)变表示反应热的示意图________ 。

(2)将N2和H2通入体积为2L的恒温恒容密闭容器中,5min后达到化学平衡,测得NH3的浓度为0.2mol/L,这段时间内用N2的浓度变化表示的化学反应速率为______________ mol/(L.min)。
(3)理论上,为了增大平衡时H2的转化率,可采取的措施是______________ (写出一条)。
(4)下图是某压强下N2和H2按物质的量之比1:3投料进行反应,反应混合物中NH3的物质的量分数随温度的变化曲线。I是平衡时的曲线,Ⅱ是不同温度下反应经过相同时间测得的曲线,下列说法正确的是______________ 。

a.图中a点,容器内n(N2):n(NH3)=1:4
b.图中b点,v正<v逆
c.400~530℃,Ⅱ中NH3的物质的量分数随温度升高而增大,原因是升高温度化学反应速率增大
(1)在一定条件下,N2(g)和H2(g)反应生成0.2 molNH3(g),放出9.24kJ的热量。在下图中画出合成氨反应中用焓(H)变表示反应热的示意图

(2)将N2和H2通入体积为2L的恒温恒容密闭容器中,5min后达到化学平衡,测得NH3的浓度为0.2mol/L,这段时间内用N2的浓度变化表示的化学反应速率为
(3)理论上,为了增大平衡时H2的转化率,可采取的措施是
(4)下图是某压强下N2和H2按物质的量之比1:3投料进行反应,反应混合物中NH3的物质的量分数随温度的变化曲线。I是平衡时的曲线,Ⅱ是不同温度下反应经过相同时间测得的曲线,下列说法正确的是

a.图中a点,容器内n(N2):n(NH3)=1:4
b.图中b点,v正<v逆
c.400~530℃,Ⅱ中NH3的物质的量分数随温度升高而增大,原因是升高温度化学反应速率增大
您最近一年使用:0次
名校
6 . 下列说法正确的是
| A.任何酸与碱发生中和反应生成1mol H2O的过程中,能量变化均相同 |
B.同温同压不,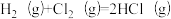 在光照和点燃条件下的∆H不同 在光照和点燃条件下的∆H不同 |
C.已知:① ,② ,② ,则C(s,石墨)=C(s,金刚石) ∆H=+1.5kJ∙mol-1,石墨比金刚石稳定 ,则C(s,石墨)=C(s,金刚石) ∆H=+1.5kJ∙mol-1,石墨比金刚石稳定 |
D.已知:① ,② ,②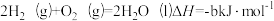 ,则a>b ,则a>b |
您最近一年使用:0次
2023-12-04更新
|
84次组卷
|
2卷引用:北京市八一学校2023-2024学年高二上学期期中测试化学试题
解题方法
7 . 氢能是一种极具发展潜力的清洁能源。
(1)氢气的燃烧热是 ,写出表示该燃烧反应的热化学方程式
,写出表示该燃烧反应的热化学方程式_______ ,若想获得1143.2kJ的热量,在该条件下需要燃烧
_______ g。
以太阳能为热能,热化学硫碘循环分解水是一种目前较具发展前景的制氢方法之一,其反应过程如下图所示:
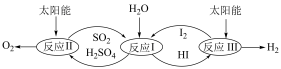
反应Ⅱ: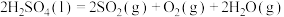
 它由两步反应组成:
它由两步反应组成:
a.
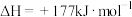
b. 分解。
分解。
(2)上述反应过程中总反应的化学方程式是_______ 。
(3) 和
和 对总反应起到了
对总反应起到了_______ 作用。
(4)从能量的角度分析,该过程实现了_______ 的转化。
(5)写出反应b的热化学方程式_______ 。
(6)热化学硫碘循环分解水制氯与化石能源制氢相比,优势是_______ (任写一条)。
(1)氢气的燃烧热是
 ,写出表示该燃烧反应的热化学方程式
,写出表示该燃烧反应的热化学方程式
以太阳能为热能,热化学硫碘循环分解水是一种目前较具发展前景的制氢方法之一,其反应过程如下图所示:

反应Ⅱ:
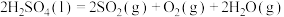
 它由两步反应组成:
它由两步反应组成:a.

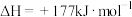
b.
 分解。
分解。(2)上述反应过程中总反应的化学方程式是
(3)
 和
和 对总反应起到了
对总反应起到了(4)从能量的角度分析,该过程实现了
(5)写出反应b的热化学方程式
(6)热化学硫碘循环分解水制氯与化石能源制氢相比,优势是
您最近一年使用:0次
解题方法
8 . 我国力争于2030年前做到碳达峰,2060年前实现碳中和。 资源化利用对缓解碳减排压力具有重要意义。在二氧化碳催化加氢制甲烷的反应体系中,主要发生反应的热化学方程式为:
资源化利用对缓解碳减排压力具有重要意义。在二氧化碳催化加氢制甲烷的反应体系中,主要发生反应的热化学方程式为:
反应Ⅰ:

反应Ⅱ: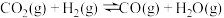
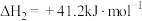
反应Ⅲ:
向恒压、密闭容器中通入 和
和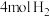 ,平衡时体系内
,平衡时体系内 、
、 、
、 的物质的量(n)与温度(T)的变化关系如图所示。
的物质的量(n)与温度(T)的变化关系如图所示。

(1)反应Ⅰ~Ⅲ中,属于吸热反应的是___________ (填反应序号)。
(2)盖斯定律的重要价值是可以利用已知反应的反应热求得未知反应的反应热,利用上述反应计算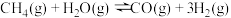 的
的
___________ 。
(3)结合上述反应,解释图中 的物质的量随温度升高而增大的原因:
的物质的量随温度升高而增大的原因:___________ 。
(4)在实际生产中为了提高甲烷的产量,选择的反应条件为较低温度和使用合适的催化剂,从反应原理角度说明选择该反应条件的理由:___________ 、___________ 。
 资源化利用对缓解碳减排压力具有重要意义。在二氧化碳催化加氢制甲烷的反应体系中,主要发生反应的热化学方程式为:
资源化利用对缓解碳减排压力具有重要意义。在二氧化碳催化加氢制甲烷的反应体系中,主要发生反应的热化学方程式为:反应Ⅰ:


反应Ⅱ:
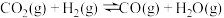
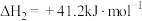
反应Ⅲ:

向恒压、密闭容器中通入
 和
和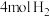 ,平衡时体系内
,平衡时体系内 、
、 、
、 的物质的量(n)与温度(T)的变化关系如图所示。
的物质的量(n)与温度(T)的变化关系如图所示。
(1)反应Ⅰ~Ⅲ中,属于吸热反应的是
(2)盖斯定律的重要价值是可以利用已知反应的反应热求得未知反应的反应热,利用上述反应计算
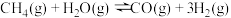 的
的
(3)结合上述反应,解释图中
 的物质的量随温度升高而增大的原因:
的物质的量随温度升高而增大的原因:(4)在实际生产中为了提高甲烷的产量,选择的反应条件为较低温度和使用合适的催化剂,从反应原理角度说明选择该反应条件的理由:
您最近一年使用:0次
名校
解题方法
9 . 下列反应中,属于氧化还原反应且ΔH<0的是
| A.葡萄糖在体内缓慢氧化 |
| B.碳酸氢钠和稀盐酸反应 |
| C.NaOH溶液与盐酸反应 |
D. 晶体与 晶体与 晶体反应 晶体反应 |
您最近一年使用:0次
2023-10-22更新
|
223次组卷
|
2卷引用:北京市顺义区第一中学2023-2024学年高二上学期10月月考化学试题
解题方法
10 . 下列图示与描述不符的是
| A | B | D | |
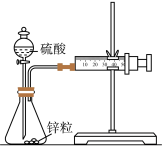 | 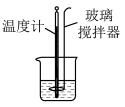 | 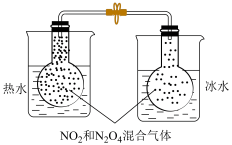  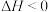 | 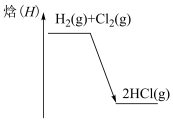  |
| 测定锌与稀硫酸反应速率 | 测定中和反应的反应热 | 研究温度对化学平衡移动的影响 | H2与Cl2反应过程中焓的化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



