1 . 完成下列填空:
(1) 水解的离子方程式为
水解的离子方程式为_______ ,在配制硫化钠溶液时可以加入少量的_______ (填化学式)以抑制其水解。
(2)硫酸铁水溶液呈_______ 性,原因是_______ 用离子方程式表示)。把 溶液蒸干灼烧,最后得到的主要固体产物是
溶液蒸干灼烧,最后得到的主要固体产物是_______ 。
(3)氢能是一种理想的绿色能源,有科学家预言,氢能有可能成为人类未来的主要能源。高纯氢的制备是目前的研究热点,包括氢的制备、储存和应用三个环节。
①适量 在
在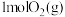 中完全燃烧,生成
中完全燃烧,生成 ,放出
,放出 的热量,请写出表示燃烧热的热化学方程式
的热量,请写出表示燃烧热的热化学方程式_______ 。
②与汽油相比,氢气作为燃料的有点是_______ 。
③下列反应均可获取 。
。
反应I:
反应II: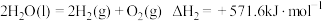
反应III: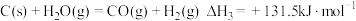
反应IV:
计算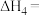
_______ 。
(1)
 水解的离子方程式为
水解的离子方程式为(2)硫酸铁水溶液呈
 溶液蒸干灼烧,最后得到的主要固体产物是
溶液蒸干灼烧,最后得到的主要固体产物是(3)氢能是一种理想的绿色能源,有科学家预言,氢能有可能成为人类未来的主要能源。高纯氢的制备是目前的研究热点,包括氢的制备、储存和应用三个环节。
①适量
 在
在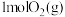 中完全燃烧,生成
中完全燃烧,生成 ,放出
,放出 的热量,请写出表示燃烧热的热化学方程式
的热量,请写出表示燃烧热的热化学方程式②与汽油相比,氢气作为燃料的有点是
③下列反应均可获取
 。
。反应I:

反应II:
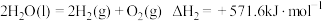
反应III:
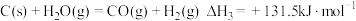
反应IV:

计算
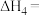
您最近一年使用:0次
2 . 为了更好的解决能源问题,人们在研究如何提高燃料燃烧效率的同时,也在寻找新能源。下列说法不正确的是
| A.太阳能、地热能、核聚变能均属于新能源 |
| B.为了使燃料充分燃烧,通入的空气越多越好 |
| C.通过洁净煤技术及烟气脱硫,减轻燃煤污染,并提高煤燃烧的热利用率 |
| D.为开发氢能,可设法将太阳能聚焦,产生高温使水分解产生氢气 |
您最近一年使用:0次
3 . 什么是燃烧热?理解燃烧热的概念时需注意哪些事项___ ?
您最近一年使用:0次
解题方法
4 . 以甲烷为原料制取氢气是工业上常用的制氢方法。已知有关化学反应的能量变化如图所示:
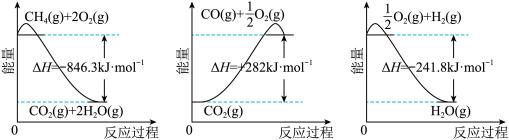
(1)下列说法正确的是___________(填字母)。
(2)CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式为___________ 。

(1)下列说法正确的是___________(填字母)。
| A.CH4的摩尔燃烧焓为846.3 kJ·mol-1 |
| B.CO的摩尔燃烧焓为282 kJ·mol-1 |
| C.H2的摩尔燃烧焓为241.8 kJ·mol-1 |
| D.CO(g)+H2O(g)=CO2(g)+H2(g)为放热反应 |
您最近一年使用:0次
2023高三·全国·专题练习
名校
解题方法
5 . 回答下列问题。
(1)用NH3可以消除氮氧化物的污染,已知:
反应Ⅰ:4NH3(g)+3O2(g) 2N2(g)+6H2O(g) ΔH1=a kJ·mol-1
2N2(g)+6H2O(g) ΔH1=a kJ·mol-1
反应Ⅱ:N2(g)+O2(g) 2NO(g) ΔH2=b kJ·mol-1
2NO(g) ΔH2=b kJ·mol-1
反应Ⅲ:4NH3(g)+6NO(g) 5N2(g)+6H2O(g) ΔH3=c kJ·mol-1
5N2(g)+6H2O(g) ΔH3=c kJ·mol-1
则反应Ⅱ中的b=___________ (用含a、c的代数式表示),反应Ⅲ中的ΔS___________ (填“>”“<”或“=”)0。
(2)已知:①2CO(g)+SO2(g) S(l)+2CO2(g) ΔH1=-37.0 kJ·mol-1
S(l)+2CO2(g) ΔH1=-37.0 kJ·mol-1
②2H2(g)+SO2(g) S(l)+2H2O(g) ΔH2=+45.4 kJ·mol-1
S(l)+2H2O(g) ΔH2=+45.4 kJ·mol-1
③CO的燃烧热ΔH3=-283 kJ·mol-1,
请回答:
表示液态硫(S)的燃烧热的热化学方程式为___________ ;反应②中,正反应活化能E1___________ (填“>”“<”或“=”)ΔH2。
(3)若某温度下,CH3COOH(aq)与NaOH(aq)反应的ΔH=-46.8 kJ·mol-1,H2SO4(aq)与NaOH(aq)的中和热为57.3 kJ·mol-1,则CH3COOH在水溶液中电离的反应热ΔH1=___________ 。
(4)已知:
则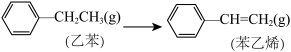 +H2(g) ΔH=
+H2(g) ΔH=___________ ;又知H2和苯乙烯的燃烧热ΔH分别为-290 kJ·mol-1和-4400 kJ·mol-1,则乙苯的燃烧热ΔH=___________ kJ·mol-1。
(1)用NH3可以消除氮氧化物的污染,已知:
反应Ⅰ:4NH3(g)+3O2(g)
 2N2(g)+6H2O(g) ΔH1=a kJ·mol-1
2N2(g)+6H2O(g) ΔH1=a kJ·mol-1反应Ⅱ:N2(g)+O2(g)
 2NO(g) ΔH2=b kJ·mol-1
2NO(g) ΔH2=b kJ·mol-1反应Ⅲ:4NH3(g)+6NO(g)
 5N2(g)+6H2O(g) ΔH3=c kJ·mol-1
5N2(g)+6H2O(g) ΔH3=c kJ·mol-1则反应Ⅱ中的b=
(2)已知:①2CO(g)+SO2(g)
 S(l)+2CO2(g) ΔH1=-37.0 kJ·mol-1
S(l)+2CO2(g) ΔH1=-37.0 kJ·mol-1②2H2(g)+SO2(g)
 S(l)+2H2O(g) ΔH2=+45.4 kJ·mol-1
S(l)+2H2O(g) ΔH2=+45.4 kJ·mol-1③CO的燃烧热ΔH3=-283 kJ·mol-1,
请回答:
表示液态硫(S)的燃烧热的热化学方程式为
(3)若某温度下,CH3COOH(aq)与NaOH(aq)反应的ΔH=-46.8 kJ·mol-1,H2SO4(aq)与NaOH(aq)的中和热为57.3 kJ·mol-1,则CH3COOH在水溶液中电离的反应热ΔH1=
(4)已知:
| 化学键 | C—H | C—C | C=C | H—H |
| 键能/(kJ·mol-1) | 412 | 348 | 612 | 436 |
 +H2(g) ΔH=
+H2(g) ΔH=
您最近一年使用:0次
6 . Ⅰ.燃料电池电动汽车是利用氢气、甲醇、天然气(主要成分为甲烷)、汽油等燃料和空气中的氧在催化剂的作用下在燃料电池中经电化学反应产生的电能,并作为主要动力源驱动的汽车。
(1)汽车行驶的过程中,能量的转化形式为_______ 。
Ⅱ.利用下表数据回答下列问题:
(2)表示乙烷燃烧热的热化学方程式为_______ 。
(3)稳定性:正丁烷_______ 异丁烷(填“>”“<”或“=”);原因_______ 。
(4)相同质量的燃料,_______ (填“C”或“H”)的质量分数越大,燃烧放出的热量越多。
(5)二氧化碳是重要的温室气体,从环保角度分析,放出相同的热量时选择_______ (填“乙烷”或“甲醇”)作为燃料产生的CO2较少。
(6)现有氢气和丙烷混合气体3 mol,完全燃烧共产生2791.5 kJ的热量,则氢气和丙烷的物质的量之比为_______ 。
(1)汽车行驶的过程中,能量的转化形式为
Ⅱ.利用下表数据回答下列问题:
| 燃料 | 燃烧热/(kJ·mol-1) | 燃料 | 燃烧热/(kJ·mol-1) |
| 氢气 | 285.8 | 甲醇(CH3OH) | 726.51 |
| 甲烷(CH4) | 890.3 | 正丁烷(CH3CH2CH2CH3) | 2878.0 |
| 乙烷(C2H6) | 1559.8 | 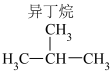 | 2869.6 |
| 丙烷(C3H8) | 2219.9 |
(3)稳定性:正丁烷
(4)相同质量的燃料,
(5)二氧化碳是重要的温室气体,从环保角度分析,放出相同的热量时选择
(6)现有氢气和丙烷混合气体3 mol,完全燃烧共产生2791.5 kJ的热量,则氢气和丙烷的物质的量之比为
您最近一年使用:0次
7 . 化学反应中的热效应又称反应热,包括燃烧热、中和热等,其数据广泛应用于科学研究和工业生产方面。
(1)若 石墨完全燃烧放出的热量为
石墨完全燃烧放出的热量为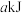 ,则石墨完全燃烧的热化学方程式为
,则石墨完全燃烧的热化学方程式为___________ 。
(2)利用如图所示装置测定中和反应的反应热的实验步骤如下:①用量筒量取 盐酸倒入内筒中,测出盐酸温度;②用另一量筒量取
盐酸倒入内筒中,测出盐酸温度;②用另一量筒量取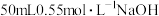 溶液,测出
溶液,测出 溶液温度;③将
溶液温度;③将 溶液沿玻璃棒缓慢倒入内筒中,设法使之混合均匀,测出混合液最高温度。装置中a的作用是
溶液沿玻璃棒缓慢倒入内筒中,设法使之混合均匀,测出混合液最高温度。装置中a的作用是___________ ,上述实验步骤中一处不合理的操作应改成___________ 。假设盐酸和氢氧化钠溶液的密度都是 ,又知中和反应后生成溶液的比热容
,又知中和反应后生成溶液的比热容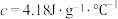 。测得溶液的温度依次为20.1℃、20.3℃、23.4℃,可计算出中和反应的反应热
。测得溶液的温度依次为20.1℃、20.3℃、23.4℃,可计算出中和反应的反应热
___________  (保留三位有效数字)。如果采用氨水代替氢氧化钠溶液,测得的中和反应的反应热
(保留三位有效数字)。如果采用氨水代替氢氧化钠溶液,测得的中和反应的反应热
___________ (“偏大”“偏小”或“相等”)。
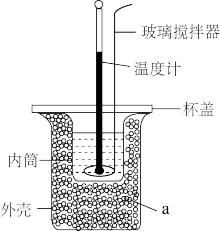
(3)键能指 气态分子解离为气态原子所需的能量。已知
气态分子解离为气态原子所需的能量。已知 ,其中H—H、O=O、O—H的键能依次为
,其中H—H、O=O、O—H的键能依次为 、
、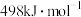 、
、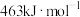 ,又知
,又知
 ,则氢气的燃烧热
,则氢气的燃烧热
___________ 。
(1)若
 石墨完全燃烧放出的热量为
石墨完全燃烧放出的热量为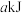 ,则石墨完全燃烧的热化学方程式为
,则石墨完全燃烧的热化学方程式为(2)利用如图所示装置测定中和反应的反应热的实验步骤如下:①用量筒量取
 盐酸倒入内筒中,测出盐酸温度;②用另一量筒量取
盐酸倒入内筒中,测出盐酸温度;②用另一量筒量取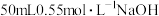 溶液,测出
溶液,测出 溶液温度;③将
溶液温度;③将 溶液沿玻璃棒缓慢倒入内筒中,设法使之混合均匀,测出混合液最高温度。装置中a的作用是
溶液沿玻璃棒缓慢倒入内筒中,设法使之混合均匀,测出混合液最高温度。装置中a的作用是 ,又知中和反应后生成溶液的比热容
,又知中和反应后生成溶液的比热容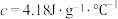 。测得溶液的温度依次为20.1℃、20.3℃、23.4℃,可计算出中和反应的反应热
。测得溶液的温度依次为20.1℃、20.3℃、23.4℃,可计算出中和反应的反应热
 (保留三位有效数字)。如果采用氨水代替氢氧化钠溶液,测得的中和反应的反应热
(保留三位有效数字)。如果采用氨水代替氢氧化钠溶液,测得的中和反应的反应热

(3)键能指
 气态分子解离为气态原子所需的能量。已知
气态分子解离为气态原子所需的能量。已知 ,其中H—H、O=O、O—H的键能依次为
,其中H—H、O=O、O—H的键能依次为 、
、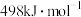 、
、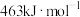 ,又知
,又知
 ,则氢气的燃烧热
,则氢气的燃烧热
您最近一年使用:0次
8 . 能源是国民经济发展的重要基础。请根据所学知识回答下列问题:
Ⅰ.在标准状况下,1.68L家用燃料(仅由C、H两种元素组成的某气体)质量为1.2g,在25℃和101kPa下完全燃烧生成 和
和 时,放出66.77kJ的热量。
时,放出66.77kJ的热量。
(1)该气体的分子式为___________ 。该气体的燃烧热
___________ 。(保留一位小数)
Ⅱ.火箭发射时可以用肼( ,液态)作燃料,
,液态)作燃料, 作氧化剂,二者反应生成
作氧化剂,二者反应生成 和水蒸气。
和水蒸气。
已知:
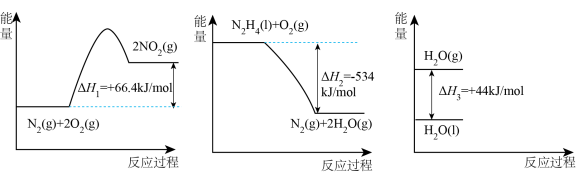
(2)请写出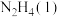 与
与 反应的热化学方程式
反应的热化学方程式___________ 。
(3)32g液态肼与足量 反应生成氮气和液态水时,放出的热量是
反应生成氮气和液态水时,放出的热量是___________ kJ。
(4)上述反应用于火箭推进器的原因:①能快速产生大量气体;②___________ 。
Ⅲ.氢能是一种极具发展潜力的清洁能源。 可用CO在高温下与水蒸气反应制得,是目前大规模制取氢气的方法之一
可用CO在高温下与水蒸气反应制得,是目前大规模制取氢气的方法之一
已知:在25℃、101kPa下,
①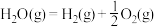
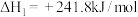
②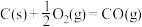
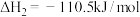
③

(5)25℃、101kPa下,CO与水蒸气反应转化为 和
和 的热化学方程式为
的热化学方程式为___________ 。
Ⅰ.在标准状况下,1.68L家用燃料(仅由C、H两种元素组成的某气体)质量为1.2g,在25℃和101kPa下完全燃烧生成
 和
和 时,放出66.77kJ的热量。
时,放出66.77kJ的热量。(1)该气体的分子式为

Ⅱ.火箭发射时可以用肼(
 ,液态)作燃料,
,液态)作燃料, 作氧化剂,二者反应生成
作氧化剂,二者反应生成 和水蒸气。
和水蒸气。已知:

(2)请写出
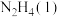 与
与 反应的热化学方程式
反应的热化学方程式(3)32g液态肼与足量
 反应生成氮气和液态水时,放出的热量是
反应生成氮气和液态水时,放出的热量是(4)上述反应用于火箭推进器的原因:①能快速产生大量气体;②
Ⅲ.氢能是一种极具发展潜力的清洁能源。
 可用CO在高温下与水蒸气反应制得,是目前大规模制取氢气的方法之一
可用CO在高温下与水蒸气反应制得,是目前大规模制取氢气的方法之一已知:在25℃、101kPa下,
①
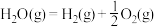
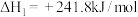
②
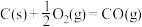
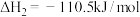
③


(5)25℃、101kPa下,CO与水蒸气反应转化为
 和
和 的热化学方程式为
的热化学方程式为
您最近一年使用:0次
2023高二上·全国·专题练习
9 . 热化学方程式的书写
书写表示燃烧热的热化学方程式时,以燃烧_____ 可燃物为标准来配平其余物质的化学计量数,同时可燃物要完全燃烧且生成_____ 。例如:H2(g)+ O2(g)=H2O(l) ΔH=-285.8kJ·mol-1
O2(g)=H2O(l) ΔH=-285.8kJ·mol-1
书写表示燃烧热的热化学方程式时,以燃烧
 O2(g)=H2O(l) ΔH=-285.8kJ·mol-1
O2(g)=H2O(l) ΔH=-285.8kJ·mol-1
您最近一年使用:0次
10 . 冬天常用煤炉燃煤取暖,夜里由于煤炉进气不足常导致煤气中毒事件发生。
(1)等量的煤不充分燃烧放出的热量和完全燃烧相比有何变化_____ ?
(2)煤不完全燃烧放出的热量是不是标准燃烧热_____ ?

(1)等量的煤不充分燃烧放出的热量和完全燃烧相比有何变化
(2)煤不完全燃烧放出的热量是不是标准燃烧热
您最近一年使用:0次



