解题方法
1 . 运用化学反应原理研究碳、氮的单质及其化合物的反应对缓解环境污染、能源危机具有重要意义。
(1)CO还原NO的反应为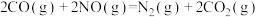 ,请回答下列问题:
,请回答下列问题:
①已知该反应为自发反应,则该反应的反应热△H_______ 0(填“>”或“<”或“=”)
②已知: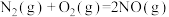


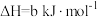
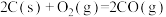

则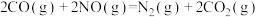 △H =
△H =______  (用含a、b、c的表达式表示)。
(用含a、b、c的表达式表示)。
③一定温度下,将2 mol CO、4 mol NO充入2 L密闭容器。5 min到达平衡,测得N2的物质的量为0.5 mol,则:
i.5min内v(NO)=_______ 。
ii.该条件下,可判断此反应到达平衡的标志是_______ 。
A.单位时间内,消耗2 mol CO同时形成1 mol N2
B.混合气体的平均相对分子质量不再改变。
C.混合气体的密度不再改变。
D.CO与NO的转化率比值不再改变。
④某研究小组探究催化剂对CO、NO转化的影响。将CO和NO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中N2的含量,从而确定尾气脱氮率(即NO的转化率),结果如图所示:
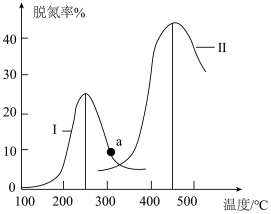
i.由图可知:要达到最大脱氮率,该反应应采取的最佳实验条件为___________ 。
ii.若低于200℃,图中曲线Ⅰ脱氮率随温度升高变化不大的主要原因为___________ 。
(2)用焦炭还原NO的反应为: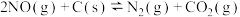 。恒容恒温条件下,向体积均为1 L的甲、乙、两三个容器中分别加入足量的焦炭和一定量的NO,测得各容器中NO的物质的量n(NO)随反应时间(t)的变化情况如下表所示:
。恒容恒温条件下,向体积均为1 L的甲、乙、两三个容器中分别加入足量的焦炭和一定量的NO,测得各容器中NO的物质的量n(NO)随反应时间(t)的变化情况如下表所示:
①T___________ 400℃(填“>”或“<”)。
②乙容器达平衡时n(N2)=___________ mol。
(1)CO还原NO的反应为
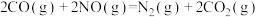 ,请回答下列问题:
,请回答下列问题:①已知该反应为自发反应,则该反应的反应热△H
②已知:
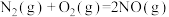


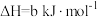
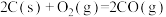

则
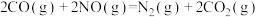 △H =
△H = (用含a、b、c的表达式表示)。
(用含a、b、c的表达式表示)。③一定温度下,将2 mol CO、4 mol NO充入2 L密闭容器。5 min到达平衡,测得N2的物质的量为0.5 mol,则:
i.5min内v(NO)=
ii.该条件下,可判断此反应到达平衡的标志是
A.单位时间内,消耗2 mol CO同时形成1 mol N2
B.混合气体的平均相对分子质量不再改变。
C.混合气体的密度不再改变。
D.CO与NO的转化率比值不再改变。
④某研究小组探究催化剂对CO、NO转化的影响。将CO和NO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中N2的含量,从而确定尾气脱氮率(即NO的转化率),结果如图所示:

i.由图可知:要达到最大脱氮率,该反应应采取的最佳实验条件为
ii.若低于200℃,图中曲线Ⅰ脱氮率随温度升高变化不大的主要原因为
(2)用焦炭还原NO的反应为:
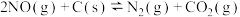 。恒容恒温条件下,向体积均为1 L的甲、乙、两三个容器中分别加入足量的焦炭和一定量的NO,测得各容器中NO的物质的量n(NO)随反应时间(t)的变化情况如下表所示:
。恒容恒温条件下,向体积均为1 L的甲、乙、两三个容器中分别加入足量的焦炭和一定量的NO,测得各容器中NO的物质的量n(NO)随反应时间(t)的变化情况如下表所示:
容器 | 0 | 40 | 80 | 120 | 160 |
| 甲/400℃ | 2.00 | 1.5 | 1.10 | 0.80 | 0.80 |
| 乙/400℃ | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
| 丙/T℃ | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
②乙容器达平衡时n(N2)=
您最近一年使用:0次





