名校
1 . 氨对人类的生存和发展有着重要意义,1909年哈伯在实验室中首次利用氮气与氢气反应合成氨,实现了人工固氮。
(1)反应N2(g)+3H2(g) 2NH3(g)的化学平衡常数表达式为
2NH3(g)的化学平衡常数表达式为_______ 。在一定条件下氨的平衡含量如表:
①该反应为_______ (填“吸热”或“放热”)反应。
②哈伯选用的条件是550℃、10MPa,而非200℃、10MPa,可能的原因是_______ 。
(2)实验室研究是工业生产的基石。如图中的实验数据是在其它条件不变时,不同温度(200℃、400℃、600℃)、压强下,平衡混合物中NH3的物质的量分数的变化情况。

①曲线a对应的温度是____________ 。
②M、N、Q点平衡常数K的大小关系是______________ 。
(3)尽管哈伯的合成氨法被评为“20世纪科学领域中最辉煌的成就”之一,但仍存在耗能高、产率低等问题。因此,科学家在持续探索,寻求合成氨的新路径。如图为电解法合成氨的原理示意图,阴极的电极反应式为_______ 。

(4)NH3转化为NO是工业制取硝酸的重要一步。已知:100kPa、298K时:
4NH3(g)+3O2(g) 2N2(g)+6H2O(g) ΔH=—1268kJ/mol
2N2(g)+6H2O(g) ΔH=—1268kJ/mol
2NO(g) N2(g)+O2(g) ΔH=—180.5kJ/mol
N2(g)+O2(g) ΔH=—180.5kJ/mol
请写出NH3转化为NO的热化学方程式_______ 。
(1)反应N2(g)+3H2(g)
 2NH3(g)的化学平衡常数表达式为
2NH3(g)的化学平衡常数表达式为| 温度/℃ | 压强/MPa | 氨的平衡含量 |
| 200 | 10 | 81.5% |
| 550 | 10 | 8.25% |
②哈伯选用的条件是550℃、10MPa,而非200℃、10MPa,可能的原因是
(2)实验室研究是工业生产的基石。如图中的实验数据是在其它条件不变时,不同温度(200℃、400℃、600℃)、压强下,平衡混合物中NH3的物质的量分数的变化情况。

①曲线a对应的温度是
②M、N、Q点平衡常数K的大小关系是
(3)尽管哈伯的合成氨法被评为“20世纪科学领域中最辉煌的成就”之一,但仍存在耗能高、产率低等问题。因此,科学家在持续探索,寻求合成氨的新路径。如图为电解法合成氨的原理示意图,阴极的电极反应式为

(4)NH3转化为NO是工业制取硝酸的重要一步。已知:100kPa、298K时:
4NH3(g)+3O2(g)
 2N2(g)+6H2O(g) ΔH=—1268kJ/mol
2N2(g)+6H2O(g) ΔH=—1268kJ/mol2NO(g)
 N2(g)+O2(g) ΔH=—180.5kJ/mol
N2(g)+O2(g) ΔH=—180.5kJ/mol请写出NH3转化为NO的热化学方程式
您最近一年使用:0次
2022-12-01更新
|
194次组卷
|
6卷引用:北京市房山区2022届高三第二次模拟测试化学试题
2 . 工业废气中的二氧化硫和氮氧化物是大气主要污染物,脱硫脱氮是环境治理的热点问题。回答下列问题:
(1)已知氮及其化合物发生如下反应:
N2(g)+O2(g) 2NO(g) ΔH=+180kJ·mol-1
2NO(g) ΔH=+180kJ·mol-1
N2(g)+2O2(g) 2NO2(g) ΔH=+68kJ·mol-1
2NO2(g) ΔH=+68kJ·mol-1
则2NO(g)+O2(g) 2NO2(g)ΔH
2NO2(g)ΔH___ kJ·mol-1。
(2)利用KMnO4脱除二氧化硫的离子方程式为:___
①□MnO +□SO2+□H2O
+□SO2+□H2O □MnO
□MnO +□ +□ 。(在“□”里填入系数,在“__”上填入微粒符号)
+□ +□ 。(在“□”里填入系数,在“__”上填入微粒符号)
②在上述反应中加入CaCO3可以提高SO2去除率,原因是___ 。
(3)CaSO3与Na2SO4混合浆液可用于脱除NO2,反应过程为:
I.CaSO3(s)+SO (aq)
(aq) CaSO4(s)+SO
CaSO4(s)+SO (aq)
(aq)
II.SO (aq)+2NO2(g)+H2O(l)
(aq)+2NO2(g)+H2O(l) SO
SO (aq)+2NO
(aq)+2NO (aq)+2H+(aq)
(aq)+2H+(aq)
浆液中CaSO3质量一定时,Na2SO4的质量与NO2的去除率变化趋势如图所示。
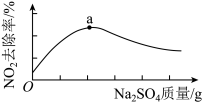
a点后NO2去除率降低的原因是___ 。
(4)检测烟道气中NOx含量的步骤如下:
I.将VL气样通入适量酸化的H2O2溶液中,使NOx完全被氧化为NO ;
;
II.加水稀释至100.00mL,量取20.00mL该溶液,与V1mLc1mol·L-1FeSO4标准溶液(过量)充分混合;
III.用c2mol·L-1KMnO4标准溶液滴定剩余的Fe2+,终点时消耗V2mL。
①NO被H2O2氧化为NO 的离子方程式为
的离子方程式为___ 。
②滴定过程中主要使用的玻璃仪器有___ 和锥形瓶等。
③滴定过程中发生下列反应:
3Fe2++NO +4H+=NO↑+3Fe3++2H2O
+4H+=NO↑+3Fe3++2H2O
MnO +5Fe2++8H+=Mn2++5Fe3++4H2O
+5Fe2++8H+=Mn2++5Fe3++4H2O
烟气气样中NOx折合成NO2的含量为__ mg·m-3。
(1)已知氮及其化合物发生如下反应:
N2(g)+O2(g)
 2NO(g) ΔH=+180kJ·mol-1
2NO(g) ΔH=+180kJ·mol-1N2(g)+2O2(g)
 2NO2(g) ΔH=+68kJ·mol-1
2NO2(g) ΔH=+68kJ·mol-1则2NO(g)+O2(g)
 2NO2(g)ΔH
2NO2(g)ΔH(2)利用KMnO4脱除二氧化硫的离子方程式为:
①□MnO
 +□SO2+□H2O
+□SO2+□H2O □MnO
□MnO +□ +□ 。(在“□”里填入系数,在“__”上填入微粒符号)
+□ +□ 。(在“□”里填入系数,在“__”上填入微粒符号)②在上述反应中加入CaCO3可以提高SO2去除率,原因是
(3)CaSO3与Na2SO4混合浆液可用于脱除NO2,反应过程为:
I.CaSO3(s)+SO
 (aq)
(aq) CaSO4(s)+SO
CaSO4(s)+SO (aq)
(aq)II.SO
 (aq)+2NO2(g)+H2O(l)
(aq)+2NO2(g)+H2O(l) SO
SO (aq)+2NO
(aq)+2NO (aq)+2H+(aq)
(aq)+2H+(aq)浆液中CaSO3质量一定时,Na2SO4的质量与NO2的去除率变化趋势如图所示。

a点后NO2去除率降低的原因是
(4)检测烟道气中NOx含量的步骤如下:
I.将VL气样通入适量酸化的H2O2溶液中,使NOx完全被氧化为NO
 ;
;II.加水稀释至100.00mL,量取20.00mL该溶液,与V1mLc1mol·L-1FeSO4标准溶液(过量)充分混合;
III.用c2mol·L-1KMnO4标准溶液滴定剩余的Fe2+,终点时消耗V2mL。
①NO被H2O2氧化为NO
 的离子方程式为
的离子方程式为②滴定过程中主要使用的玻璃仪器有
③滴定过程中发生下列反应:
3Fe2++NO
 +4H+=NO↑+3Fe3++2H2O
+4H+=NO↑+3Fe3++2H2OMnO
 +5Fe2++8H+=Mn2++5Fe3++4H2O
+5Fe2++8H+=Mn2++5Fe3++4H2O烟气气样中NOx折合成NO2的含量为
您最近一年使用:0次



