解题方法
1 . 某钒渣主要成分为 (含有少量
(含有少量 、
、 ),以其为原料生产
),以其为原料生产 的工艺如下图:
的工艺如下图:

已知:
i.钒酸(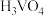 )是强酸,
)是强酸, (偏钒酸铵)难溶于水;
(偏钒酸铵)难溶于水; 价钒在溶液中的主要存在形式与溶液
价钒在溶液中的主要存在形式与溶液 的关系如表所示。
的关系如表所示。
ii.室温下,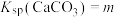 ,
,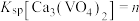 。
。
iii. 在溶液
在溶液 时开始沉淀,溶液
时开始沉淀,溶液 时沉淀完全。
时沉淀完全。
请回答以下问题:
(1)“酸浸”前需将块状固体粉碎,其目的是_______ ;焙烧过程中 生成
生成 的化学方程式为
的化学方程式为___________ 。
(2)已知 难溶于水,可溶于盐酸。若“酸浸”时溶液的
难溶于水,可溶于盐酸。若“酸浸”时溶液的 ,则
,则 溶于盐酸的离子方程式为
溶于盐酸的离子方程式为________ 。
(3)“转沉”时,发生反应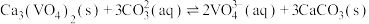 ,该反应的平衡常数
,该反应的平衡常数
________ (用含m、n的代数式表示)。
(4)“沉钒2”的沉钒率随温度的变化如图所示,温度高于80℃沉钒率下降的原因是_________ 。

(5)产品纯度测定:将 产品
产品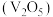 溶于足量稀硫酸配成
溶于足量稀硫酸配成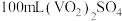 溶液。取
溶液。取 该溶液于锥形瓶中,用
该溶液于锥形瓶中,用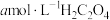 标准溶液进行滴定,经过三次滴定,达到滴定终点时平均消耗标准溶液的体积为
标准溶液进行滴定,经过三次滴定,达到滴定终点时平均消耗标准溶液的体积为 。
。
①完成下列滴定过程的离子方程式:____________ 。

②产品的纯度为_________ (用质量分数表示,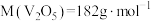 )。
)。
 (含有少量
(含有少量 、
、 ),以其为原料生产
),以其为原料生产 的工艺如下图:
的工艺如下图:
已知:
i.钒酸(
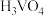 )是强酸,
)是强酸, (偏钒酸铵)难溶于水;
(偏钒酸铵)难溶于水; 价钒在溶液中的主要存在形式与溶液
价钒在溶液中的主要存在形式与溶液 的关系如表所示。
的关系如表所示。 | 4~6 | 6~8 | 8~10 | 10~12 |
| 主要离子 |  |  |  |  |
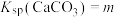 ,
,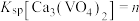 。
。iii.
 在溶液
在溶液 时开始沉淀,溶液
时开始沉淀,溶液 时沉淀完全。
时沉淀完全。请回答以下问题:
(1)“酸浸”前需将块状固体粉碎,其目的是
 生成
生成 的化学方程式为
的化学方程式为(2)已知
 难溶于水,可溶于盐酸。若“酸浸”时溶液的
难溶于水,可溶于盐酸。若“酸浸”时溶液的 ,则
,则 溶于盐酸的离子方程式为
溶于盐酸的离子方程式为(3)“转沉”时,发生反应
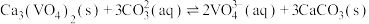 ,该反应的平衡常数
,该反应的平衡常数
(4)“沉钒2”的沉钒率随温度的变化如图所示,温度高于80℃沉钒率下降的原因是

(5)产品纯度测定:将
 产品
产品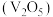 溶于足量稀硫酸配成
溶于足量稀硫酸配成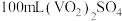 溶液。取
溶液。取 该溶液于锥形瓶中,用
该溶液于锥形瓶中,用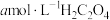 标准溶液进行滴定,经过三次滴定,达到滴定终点时平均消耗标准溶液的体积为
标准溶液进行滴定,经过三次滴定,达到滴定终点时平均消耗标准溶液的体积为 。
。①完成下列滴定过程的离子方程式:

②产品的纯度为
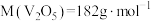 )。
)。
您最近一年使用:0次
解题方法
2 . 工业上用含三价钒(V2O3)为主的某石煤为原料(含有Al2O3、SiO2、Fe2O3等杂质),低温硫酸化焙烧—水浸工艺制备V2O5,其流程如图:

资料:
ⅰ.VOSO4高温易分解
ⅱ.含磷有机试剂对溶液中离子萃取能力为Fe(III)>V(IV)>V(V)>Fe(II)
ⅲ.含磷有机试剂萃取过程中溶液的H+浓度越高,萃取率越低,萃取钒效果越差
ⅳ.10VO +8H2O
+8H2O H2V10O
H2V10O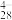 +14H+
+14H+
ⅴ.氢氧化物完全沉淀时溶液的pH表
(1)焙烧过程中向石煤中加硫酸焙烧,将V2O3转化为VOSO4的化学方程式是____ 。
(2)预处理过程中先加入Na2SO3溶液进行还原预处理,加入Na2SO3溶液的第一个作用是将V(V)还原为V(IV)减少钒的损失,再用氨水混合并调节溶液pH。
①请结合相关离子方程式,说明加入Na2SO3的第二个作用____ 。
②解释加氨水调节pH≈5的原因是____ 。
(3)上述I的具体操作为____ 。
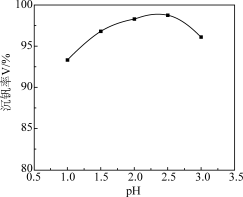
(4)沉钒过程中先加入NaClO3进行氧化,再加氨水调节pH,铵盐会将H2V10O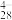 中的钒元素以多钒酸铵((NH4)2V6O16)的形式沉淀。溶液pH值与沉钒率的关系如图,请结合反应原理解释沉钒的pH=2.5的原因是
中的钒元素以多钒酸铵((NH4)2V6O16)的形式沉淀。溶液pH值与沉钒率的关系如图,请结合反应原理解释沉钒的pH=2.5的原因是____ 。
(5)测定产品中V2O5的纯度:
称取ag产品,先用硫酸溶解,得到(VO2)2SO4溶液。再加入b1mLc1mol·L-1(NH4)2Fe(SO4)2溶液(VO +2H++Fe2+=VO2++Fe3++H2O)最后用c2mol·L-1KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液的体积为b2mL。已知MnO
+2H++Fe2+=VO2++Fe3++H2O)最后用c2mol·L-1KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液的体积为b2mL。已知MnO 被还原为Mn2+,假设杂质不参与反应。则产品中V2O5的质量分数是
被还原为Mn2+,假设杂质不参与反应。则产品中V2O5的质量分数是____ 。(V2O5的摩尔质量:182g•mol-1)

资料:
ⅰ.VOSO4高温易分解
ⅱ.含磷有机试剂对溶液中离子萃取能力为Fe(III)>V(IV)>V(V)>Fe(II)
ⅲ.含磷有机试剂萃取过程中溶液的H+浓度越高,萃取率越低,萃取钒效果越差
ⅳ.10VO
 +8H2O
+8H2O H2V10O
H2V10O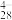 +14H+
+14H+ⅴ.氢氧化物完全沉淀时溶液的pH表
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 完全沉淀 | 3.2 | 9.0 | 4.7 |
(2)预处理过程中先加入Na2SO3溶液进行还原预处理,加入Na2SO3溶液的第一个作用是将V(V)还原为V(IV)减少钒的损失,再用氨水混合并调节溶液pH。
①请结合相关离子方程式,说明加入Na2SO3的第二个作用
②解释加氨水调节pH≈5的原因是
(3)上述I的具体操作为
(4)沉钒过程中先加入NaClO3进行氧化,再加氨水调节pH,铵盐会将H2V10O
 中的钒元素以多钒酸铵((NH4)2V6O16)的形式沉淀。溶液pH值与沉钒率的关系如图,请结合反应原理解释沉钒的pH=2.5的原因是
中的钒元素以多钒酸铵((NH4)2V6O16)的形式沉淀。溶液pH值与沉钒率的关系如图,请结合反应原理解释沉钒的pH=2.5的原因是
(5)测定产品中V2O5的纯度:
称取ag产品,先用硫酸溶解,得到(VO2)2SO4溶液。再加入b1mLc1mol·L-1(NH4)2Fe(SO4)2溶液(VO
 +2H++Fe2+=VO2++Fe3++H2O)最后用c2mol·L-1KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液的体积为b2mL。已知MnO
+2H++Fe2+=VO2++Fe3++H2O)最后用c2mol·L-1KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液的体积为b2mL。已知MnO 被还原为Mn2+,假设杂质不参与反应。则产品中V2O5的质量分数是
被还原为Mn2+,假设杂质不参与反应。则产品中V2O5的质量分数是
您最近一年使用:0次
解题方法
3 . 氮及其化合物在农业、医药、国防等领域应用广泛。请回答下列问题
(1)实验室加热 和
和  固体混合物制取
固体混合物制取  ,反应的化学方程式是
,反应的化学方程式是___________ 。
(2)工业合成氨及氨氧化制取硝酸的流程示意图如下。
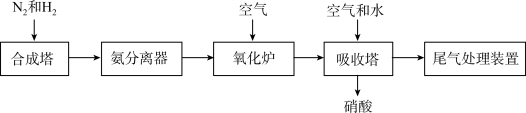
①合成塔中生成 ,说明
,说明  具有
具有___________ (填“氧化性”或“还原性”)。
②氧化炉中 转化为
转化为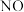 ,发生反应的化学方程式是
,发生反应的化学方程式是___________ 。
③吸收塔中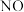 最终可转化为
最终可转化为  。通入空气是为了提供
。通入空气是为了提供___________ (填字母)。
a. b.
b. c.
c.
④尾气处理装置中,可用 将尾气中
将尾气中  还原为
还原为  。反应的化学方程式是
。反应的化学方程式是___________ 。
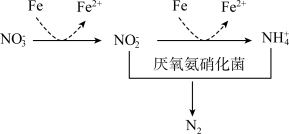
(3)氮元素含量过高会造成水体污染,添加铁粉能够提高氮的脱除率,工艺如下图所示。试从价态角度分析原因___________ 。
(1)实验室加热
 和
和  固体混合物制取
固体混合物制取  ,反应的化学方程式是
,反应的化学方程式是(2)工业合成氨及氨氧化制取硝酸的流程示意图如下。

①合成塔中生成
 ,说明
,说明  具有
具有②氧化炉中
 转化为
转化为 ,发生反应的化学方程式是
,发生反应的化学方程式是③吸收塔中
 最终可转化为
最终可转化为  。通入空气是为了提供
。通入空气是为了提供a.
 b.
b. c.
c.
④尾气处理装置中,可用
 将尾气中
将尾气中  还原为
还原为  。反应的化学方程式是
。反应的化学方程式是(3)氮元素含量过高会造成水体污染,添加铁粉能够提高氮的脱除率,工艺如下图所示。试从价态角度分析原因

您最近一年使用:0次
名校
4 . 合成氨是人类科学技术上的一项重大突破,氨有广泛的应用。
已知:
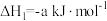
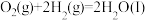
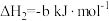
(1)由 与
与 反应生成
反应生成 的热化学方程式是
的热化学方程式是
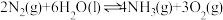

___________ 
(2)工业上主要以 、
、 为原料气合成
为原料气合成 。
。
将物质的量之比为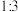 的
的 和
和 充入
充入 的密闭容器中,在一定条件下达到平衡,测得平衡时数据如下:
的密闭容器中,在一定条件下达到平衡,测得平衡时数据如下:
①该条件下 的转化率为
的转化率为___________ ,平衡常数
___________ (本题均可用分数表示):
②若按以下浓度投料,其它反应条件与①相同,起始时反应进行的方向为___________ (填“正向”、“逆向”或“无法判断”)。
③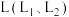 、X可分别代表压强或温度。图1表示L一定时,合成氨反应中
、X可分别代表压强或温度。图1表示L一定时,合成氨反应中 的平衡转化率随X的变化关系。
的平衡转化率随X的变化关系。

i.X代表的物理量是_______________ 。
ⅱ.判断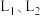 的大小关系,并简述理由
的大小关系,并简述理由__________________ 。
(3)电化学气敏传感器可用于检测环境中 的含量,其工作原理如图2所示,则a极的电极反应式为
的含量,其工作原理如图2所示,则a极的电极反应式为______________________ 。

已知:

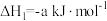
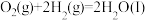
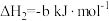
(1)由
 与
与 反应生成
反应生成 的热化学方程式是
的热化学方程式是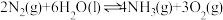


(2)工业上主要以
 、
、 为原料气合成
为原料气合成 。
。将物质的量之比为
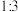 的
的 和
和 充入
充入 的密闭容器中,在一定条件下达到平衡,测得平衡时数据如下:
的密闭容器中,在一定条件下达到平衡,测得平衡时数据如下:物质 |
|
|
|
平衡时物质的量/ | 0.2 | 0.6 | 0.2 |
 的转化率为
的转化率为
②若按以下浓度投料,其它反应条件与①相同,起始时反应进行的方向为
物质 |
|
|
|
起始浓度( | 0.5 | 1.5 | 0.5 |
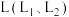 、X可分别代表压强或温度。图1表示L一定时,合成氨反应中
、X可分别代表压强或温度。图1表示L一定时,合成氨反应中 的平衡转化率随X的变化关系。
的平衡转化率随X的变化关系。
i.X代表的物理量是
ⅱ.判断
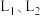 的大小关系,并简述理由
的大小关系,并简述理由(3)电化学气敏传感器可用于检测环境中
 的含量,其工作原理如图2所示,则a极的电极反应式为
的含量,其工作原理如图2所示,则a极的电极反应式为
您最近一年使用:0次
5 . 某煤化工厂废水含有大量有机物、氨氮、氰化物、悬浮颗粒等有害物质,处理流程如图所示。

已知:
(1)萃取塔中经过______ (填写操作名称)可得含酚有机层。
(2)蒸氨塔中需要连续加入碱液并保持较高温度,请从化学平衡角度解释原因:______ 。
(3)缺氧池中含有NH 及CN-,其中CN-(C为+2价)可被回流硝化液中的NO
及CN-,其中CN-(C为+2价)可被回流硝化液中的NO 氧化为无毒气体。请补全该反应的离子方程式:
氧化为无毒气体。请补全该反应的离子方程式:______ 。
CN-+NO +
+ ______=
______= ______+CO2+
______+CO2+ ______
______
(4)向好氧池中投入Na2CO3的目的是______ 。
(5)下列关于混凝沉淀池中的说法合理的是______ (填写序号)。
a.混凝沉淀池溶液的pH控制在6.5左右
b.FeSO4水解产生Fe(OH)2胶体,吸附水中的悬浮颗粒
c.相同条件下,使用Fe2(SO4)3可获得相同的混凝效果
(6)出水检测
甲醛法可以测定水样中NH 的含量,其反应原理为4NH
的含量,其反应原理为4NH +6HCHO=3H++6H2O+(CH2)6N4H+,然后用NaOH标准溶液滴定反应生成的酸[滴定时,1mol(CH2)6N4H+与1molH+相当]。
+6HCHO=3H++6H2O+(CH2)6N4H+,然后用NaOH标准溶液滴定反应生成的酸[滴定时,1mol(CH2)6N4H+与1molH+相当]。
实验步骤:
i.移取VmL出水样品,以酚酞为指示剂,用cmol/LNaOH标准液滴定至终点,中和样品中的酸,消耗NaOH的体积为V1mL;
ii.另取同样体积的样品,加入足量的中性甲醛溶液,摇匀,静置5min后,加入1~2滴酚酞溶液,用NaOH标准溶液滴定至终点,消耗NaOH的体积为V2mL。
①步骤ii中滴定至终点的现象为______ 。
②该水样中残留NH 浓度为
浓度为______ mol/L。

已知:
| 离子 | 开始沉淀pH | 完全沉淀pH |
| Fe2+ | 6.3 | 8.3 |
| Fe3+ | 1.1 | 3.2 |
(2)蒸氨塔中需要连续加入碱液并保持较高温度,请从化学平衡角度解释原因:
(3)缺氧池中含有NH
 及CN-,其中CN-(C为+2价)可被回流硝化液中的NO
及CN-,其中CN-(C为+2价)可被回流硝化液中的NO 氧化为无毒气体。请补全该反应的离子方程式:
氧化为无毒气体。请补全该反应的离子方程式:CN-+NO
 +
+ ______=
______= ______+CO2+
______+CO2+ ______
______(4)向好氧池中投入Na2CO3的目的是
(5)下列关于混凝沉淀池中的说法合理的是
a.混凝沉淀池溶液的pH控制在6.5左右
b.FeSO4水解产生Fe(OH)2胶体,吸附水中的悬浮颗粒
c.相同条件下,使用Fe2(SO4)3可获得相同的混凝效果
(6)出水检测
甲醛法可以测定水样中NH
 的含量,其反应原理为4NH
的含量,其反应原理为4NH +6HCHO=3H++6H2O+(CH2)6N4H+,然后用NaOH标准溶液滴定反应生成的酸[滴定时,1mol(CH2)6N4H+与1molH+相当]。
+6HCHO=3H++6H2O+(CH2)6N4H+,然后用NaOH标准溶液滴定反应生成的酸[滴定时,1mol(CH2)6N4H+与1molH+相当]。实验步骤:
i.移取VmL出水样品,以酚酞为指示剂,用cmol/LNaOH标准液滴定至终点,中和样品中的酸,消耗NaOH的体积为V1mL;
ii.另取同样体积的样品,加入足量的中性甲醛溶液,摇匀,静置5min后,加入1~2滴酚酞溶液,用NaOH标准溶液滴定至终点,消耗NaOH的体积为V2mL。
①步骤ii中滴定至终点的现象为
②该水样中残留NH
 浓度为
浓度为
您最近一年使用:0次
名校
6 . 含硫化合物,不仅用于研究化学反应的原理,也在生产生活有普遍应用。
(1)以反应 为例,探究外界条件对化学反应速率的影响,实验方案如下表所示。
为例,探究外界条件对化学反应速率的影响,实验方案如下表所示。
请回答:①上表中,a为_______ ,b为_______ 。
②上述三个实验中的反应速率最快的应该是实验_______ (用I、II、III作答)
(2)亚硫酸钠是一种常见的食品添加剂。为检验某食品中亚硫酸钠含量(通常以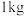 样品中含
样品中含 的质量计),某研究小组同学设计了如下实验方案。
的质量计),某研究小组同学设计了如下实验方案。
I.称取样品 ;
;
II.向样品中加入足量稀硫酸;
III.将I中产生的 用足量
用足量 溶液吸收;
溶液吸收;
IV.将II所得硫酸溶液用氢氧化钠标准液滴定;
V.数据处理。
① 是一种食品添加剂。写出
是一种食品添加剂。写出 与稀硫酸反应的离子方程式
与稀硫酸反应的离子方程式_______ 。
②步骤III中 的作用是
的作用是_______ 。
③步骤IV中可选用的指示剂为_______ 。下图显示滴定终点时,滴定管(量程为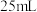 )读数为
)读数为_______  。
。

④步骤IV中消耗 溶液
溶液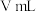 ,则
,则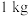 样品中含
样品中含 的质量是
的质量是_______ g(用含W、V的代数式表示)。
⑤步骤IV中的下列操作会造成该实验亚硫酸盐含量测定结果偏低的有_______ 。
a.滴定开始读数时仰视读数
b.装入氢氧化钠标准液前,碱式滴定管未用氢氧化钠标准液润洗
c.锥形瓶内用水冲洗后未干燥
d.在滴定过程中发现局部溶液发生色变就立即停止滴定
(1)以反应
 为例,探究外界条件对化学反应速率的影响,实验方案如下表所示。
为例,探究外界条件对化学反应速率的影响,实验方案如下表所示。| 实验序号 |  溶液 溶液 |  溶液 溶液 | 蒸馏水 | 温度/℃ | ||
浓度/( ) ) | 体积/mL | 浓度/( ) ) | 体积/mL | 体积/mL | ||
| I | 0.1 | 1.5 | 0.1 | 1.5 | 10 | 20 |
| II | 0.1 | 2.5 | 0.1 | 1.5 | 9 | a |
| III | 0.1 | b | 0.1 | 1.5 | 9 | 30 |
②上述三个实验中的反应速率最快的应该是实验
(2)亚硫酸钠是一种常见的食品添加剂。为检验某食品中亚硫酸钠含量(通常以
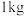 样品中含
样品中含 的质量计),某研究小组同学设计了如下实验方案。
的质量计),某研究小组同学设计了如下实验方案。I.称取样品
 ;
;II.向样品中加入足量稀硫酸;
III.将I中产生的
 用足量
用足量 溶液吸收;
溶液吸收;IV.将II所得硫酸溶液用氢氧化钠标准液滴定;
V.数据处理。
①
 是一种食品添加剂。写出
是一种食品添加剂。写出 与稀硫酸反应的离子方程式
与稀硫酸反应的离子方程式②步骤III中
 的作用是
的作用是③步骤IV中可选用的指示剂为
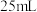 )读数为
)读数为 。
。
④步骤IV中消耗
 溶液
溶液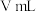 ,则
,则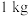 样品中含
样品中含 的质量是
的质量是⑤步骤IV中的下列操作会造成该实验亚硫酸盐含量测定结果偏低的有
a.滴定开始读数时仰视读数
b.装入氢氧化钠标准液前,碱式滴定管未用氢氧化钠标准液润洗
c.锥形瓶内用水冲洗后未干燥
d.在滴定过程中发现局部溶液发生色变就立即停止滴定
您最近一年使用:0次
2023-02-21更新
|
245次组卷
|
2卷引用:北京市房山区2022-2023学年高二上学期期末考试化学试题
7 . 以CO2为原料合成甲醇可以减少CO2的排放,实现碳的循环利用。一种铜基催化剂对该反应有良好的催化效果。
I.催化反应机理
(1)乙醇胺(HOCH2CH2NH2)可用做CO2捕获剂,乙醇胺溶液能够吸收和释放CO2的原因是_____ 。
(2)有学者提出CO2转化成甲醇的催化机理如图所示。反应的副产物有_____ 。
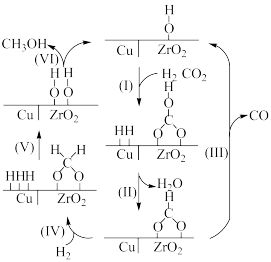
II.催化剂的性能测试
一定条件下使CO2、H2混合气体通过反应器,检测反应器出口气体的成分及其含量,计算CO2的转化率和CH3OH的选择性以评价催化剂的性能。
已知:i.反应器内发生的反应有:
a.CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49.5kJ•mol-1
CH3OH(g)+H2O(g) △H=-49.5kJ•mol-1
b.CO2(g)+H2(g) CO(g)+H2O(g) △H=+41.2kJ•mol-1
CO(g)+H2O(g) △H=+41.2kJ•mol-1
ii.CH3OH选择性= ×100%
×100%
(3)220℃时,测得反应器出口气体中全部含碳物质的物质的量之比n(CH3OH):n(CO2):n(CO)=1:7.20:0.11,则该温度下CO2转化率=_____ ×100%(列出计算式)。
(4)其他条件相同时,反应温度对CO2的转化率和CH3OH的选择性的影响如图所示:
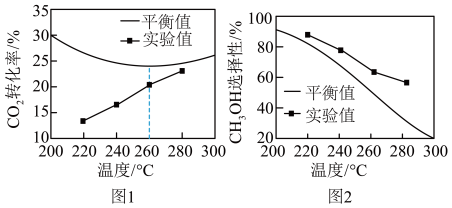
①由图1可知实验中反应均未达到化学平衡状态的依据是______ 。
②温度高于260℃时,CO2平衡转化率变化的原因是_____ 。
③由图2可知,温度相同时CH3OH选择性的实验值略高于其平衡值,从化学反应速率的角度解释原因_____ 。
I.催化反应机理
(1)乙醇胺(HOCH2CH2NH2)可用做CO2捕获剂,乙醇胺溶液能够吸收和释放CO2的原因是
(2)有学者提出CO2转化成甲醇的催化机理如图所示。反应的副产物有

II.催化剂的性能测试
一定条件下使CO2、H2混合气体通过反应器,检测反应器出口气体的成分及其含量,计算CO2的转化率和CH3OH的选择性以评价催化剂的性能。
已知:i.反应器内发生的反应有:
a.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H=-49.5kJ•mol-1
CH3OH(g)+H2O(g) △H=-49.5kJ•mol-1b.CO2(g)+H2(g)
 CO(g)+H2O(g) △H=+41.2kJ•mol-1
CO(g)+H2O(g) △H=+41.2kJ•mol-1ii.CH3OH选择性=
 ×100%
×100%(3)220℃时,测得反应器出口气体中全部含碳物质的物质的量之比n(CH3OH):n(CO2):n(CO)=1:7.20:0.11,则该温度下CO2转化率=
(4)其他条件相同时,反应温度对CO2的转化率和CH3OH的选择性的影响如图所示:

①由图1可知实验中反应均未达到化学平衡状态的依据是
②温度高于260℃时,CO2平衡转化率变化的原因是
③由图2可知,温度相同时CH3OH选择性的实验值略高于其平衡值,从化学反应速率的角度解释原因
您最近一年使用:0次
名校
8 . 氨对人类的生存和发展有着重要意义,1909年哈伯在实验室中首次利用氮气与氢气反应合成氨,实现了人工固氮。
(1)反应N2(g)+3H2(g) 2NH3(g)的化学平衡常数表达式为
2NH3(g)的化学平衡常数表达式为_______ 。在一定条件下氨的平衡含量如表:
①该反应为_______ (填“吸热”或“放热”)反应。
②哈伯选用的条件是550℃、10MPa,而非200℃、10MPa,可能的原因是_______ 。
(2)实验室研究是工业生产的基石。如图中的实验数据是在其它条件不变时,不同温度(200℃、400℃、600℃)、压强下,平衡混合物中NH3的物质的量分数的变化情况。

①曲线a对应的温度是____________ 。
②M、N、Q点平衡常数K的大小关系是______________ 。
(3)尽管哈伯的合成氨法被评为“20世纪科学领域中最辉煌的成就”之一,但仍存在耗能高、产率低等问题。因此,科学家在持续探索,寻求合成氨的新路径。如图为电解法合成氨的原理示意图,阴极的电极反应式为_______ 。

(4)NH3转化为NO是工业制取硝酸的重要一步。已知:100kPa、298K时:
4NH3(g)+3O2(g) 2N2(g)+6H2O(g) ΔH=—1268kJ/mol
2N2(g)+6H2O(g) ΔH=—1268kJ/mol
2NO(g) N2(g)+O2(g) ΔH=—180.5kJ/mol
N2(g)+O2(g) ΔH=—180.5kJ/mol
请写出NH3转化为NO的热化学方程式_______ 。
(1)反应N2(g)+3H2(g)
 2NH3(g)的化学平衡常数表达式为
2NH3(g)的化学平衡常数表达式为| 温度/℃ | 压强/MPa | 氨的平衡含量 |
| 200 | 10 | 81.5% |
| 550 | 10 | 8.25% |
②哈伯选用的条件是550℃、10MPa,而非200℃、10MPa,可能的原因是
(2)实验室研究是工业生产的基石。如图中的实验数据是在其它条件不变时,不同温度(200℃、400℃、600℃)、压强下,平衡混合物中NH3的物质的量分数的变化情况。

①曲线a对应的温度是
②M、N、Q点平衡常数K的大小关系是
(3)尽管哈伯的合成氨法被评为“20世纪科学领域中最辉煌的成就”之一,但仍存在耗能高、产率低等问题。因此,科学家在持续探索,寻求合成氨的新路径。如图为电解法合成氨的原理示意图,阴极的电极反应式为

(4)NH3转化为NO是工业制取硝酸的重要一步。已知:100kPa、298K时:
4NH3(g)+3O2(g)
 2N2(g)+6H2O(g) ΔH=—1268kJ/mol
2N2(g)+6H2O(g) ΔH=—1268kJ/mol2NO(g)
 N2(g)+O2(g) ΔH=—180.5kJ/mol
N2(g)+O2(g) ΔH=—180.5kJ/mol请写出NH3转化为NO的热化学方程式
您最近一年使用:0次
2022-12-01更新
|
197次组卷
|
6卷引用:北京市房山区2022届高三第二次模拟测试化学试题
9 . 把铝条放入盛有过量稀盐酸的试管中,下列因素中不会 影响生成氢气速率的是
| A.盐酸的浓度 | B.铝条的表面积 | C.溶液的温度 | D.盐酸中 杂质的含量 杂质的含量 |
您最近一年使用:0次
10 . 三氧化二镍( )是一种重要的电子元件材料和蓄电池材料。工业上利用含镍废料(镍、铁、钙、镁合金为主)制取草酸镍(
)是一种重要的电子元件材料和蓄电池材料。工业上利用含镍废料(镍、铁、钙、镁合金为主)制取草酸镍( ),再高温煅烧草酸镍制取
),再高温煅烧草酸镍制取 。工艺流程图如下所示:
。工艺流程图如下所示:

已知:ⅰ.草酸的钙、镁、镍盐以及 、
、 均难溶于水。
均难溶于水。
ⅱ.溶液中金属阳离子的氢氧化物开始沉淀和沉淀完全的pH(20℃)如下表:
请回答下列问题:
(1) 中Ni的化合价为
中Ni的化合价为______ ;操作a为______ 。
(2)①加入 的作用是
的作用是____________ 。
②加入碳酸钠溶液调pH至4.0~5.0,其目的为__________________ 。
(3)滤渣C中的主要物质是____________ 。
(4)草酸镍( )在热空气中干燥脱水后,再高温下煅烧,可制得
)在热空气中干燥脱水后,再高温下煅烧,可制得 ,同时获得混合气体。
,同时获得混合气体。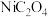 受热分解的化学方程式为
受热分解的化学方程式为____________ 。
(5)若镍废料中镍含量为50%,用该方法处理1 t镍废料得到0.56 t (假设不含杂质),则产率为
(假设不含杂质),则产率为______ (保留2位小数)。
(6)工业上还可用电解法制取 。用NaOH溶液调
。用NaOH溶液调 溶液的pH至7.5,加入适量
溶液的pH至7.5,加入适量 后利用惰性电极电解。电解过程中产生的
后利用惰性电极电解。电解过程中产生的 有80%在弱碱性条件下生成
有80%在弱碱性条件下生成 ,再把二价镍氧化为三价镍。
,再把二价镍氧化为三价镍。
补齐 与
与 反应,生成
反应,生成 的离子方程式
的离子方程式____________ 。
□ □
□ □
□ □
□ □________
□________
 )是一种重要的电子元件材料和蓄电池材料。工业上利用含镍废料(镍、铁、钙、镁合金为主)制取草酸镍(
)是一种重要的电子元件材料和蓄电池材料。工业上利用含镍废料(镍、铁、钙、镁合金为主)制取草酸镍( ),再高温煅烧草酸镍制取
),再高温煅烧草酸镍制取 。工艺流程图如下所示:
。工艺流程图如下所示:
已知:ⅰ.草酸的钙、镁、镍盐以及
 、
、 均难溶于水。
均难溶于水。ⅱ.溶液中金属阳离子的氢氧化物开始沉淀和沉淀完全的pH(20℃)如下表:
| 金属离子 |  |  |  |  |  |
开始沉淀时( mol/L)的pH mol/L)的pH | 7.7 | 7.5 | 2.2 | 12.3 | 9.6 |
完全时(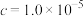 mol/L)的pH mol/L)的pH | 9.2 | 9.0 | 3.2 | 微溶 | 11.1 |
(1)
 中Ni的化合价为
中Ni的化合价为(2)①加入
 的作用是
的作用是②加入碳酸钠溶液调pH至4.0~5.0,其目的为
(3)滤渣C中的主要物质是
(4)草酸镍(
 )在热空气中干燥脱水后,再高温下煅烧,可制得
)在热空气中干燥脱水后,再高温下煅烧,可制得 ,同时获得混合气体。
,同时获得混合气体。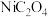 受热分解的化学方程式为
受热分解的化学方程式为(5)若镍废料中镍含量为50%,用该方法处理1 t镍废料得到0.56 t
 (假设不含杂质),则产率为
(假设不含杂质),则产率为(6)工业上还可用电解法制取
 。用NaOH溶液调
。用NaOH溶液调 溶液的pH至7.5,加入适量
溶液的pH至7.5,加入适量 后利用惰性电极电解。电解过程中产生的
后利用惰性电极电解。电解过程中产生的 有80%在弱碱性条件下生成
有80%在弱碱性条件下生成 ,再把二价镍氧化为三价镍。
,再把二价镍氧化为三价镍。补齐
 与
与 反应,生成
反应,生成 的离子方程式
的离子方程式□
 □
□ □
□ □
□ □________
□________
您最近一年使用:0次
2023-04-22更新
|
330次组卷
|
4卷引用:北京师范大学良乡附中2023-2024学年高三上学期10月月考化学试题
北京师范大学良乡附中2023-2024学年高三上学期10月月考化学试题北京市大兴区2022-2023学年高二上学期期末考试化学试题(已下线)2023年北京卷高考真题变式题(工业流程题)(已下线)工业流程题


 )
)

