1 . 化学与社会、生产密切相关,下列说法不正确 的是
| A.对于一个化学反应,反应的途径有可能不同,但其焓变一定相同 |
| B.氧化还原反应所释放的化学能,是化学电源的主要能量来源 |
| C.标准燃烧热的数值与该物质燃烧时的热化学方程式中的计量数成正比 |
| D.新能源汽车的使用和推广,将有助于促进我国的“碳达峰”“碳中和”任务的完成 |
您最近一年使用:0次
2 . 烯烃是一种应用广泛的化学原料。烯烃之间存在下列三个反应:
反应I:
反应II:
反应III:
在恒压密闭容器中,反应达平衡时,三种组分的物质的量分数x随温度T的变化关系如图所示。
反应I:

反应II:

反应III:

在恒压密闭容器中,反应达平衡时,三种组分的物质的量分数x随温度T的变化关系如图所示。

A.反应III的 |
B.700K时反应II的平衡常数 (以物质的量分数代替平衡浓度) (以物质的量分数代替平衡浓度) |
C.提高 物质的量分数,需研发低温条件下活性好且耐高压的催化剂 物质的量分数,需研发低温条件下活性好且耐高压的催化剂 |
| D.超过700K后曲线a下降的原因可能是随着温度升高反应I逆向移动,反应II正向移动 |
您最近一年使用:0次
名校
解题方法
3 . 已知下列热化学方程式: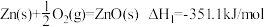 ;
;
 ,由此可知
,由此可知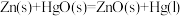 的
的 ,其中
,其中 的值是
的值是
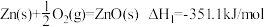 ;
; ,由此可知
,由此可知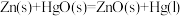 的
的 ,其中
,其中 的值是
的值是A.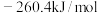 | B.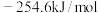 |
C.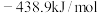 | D.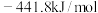 |
您最近一年使用:0次
2022-10-22更新
|
226次组卷
|
3卷引用:江苏省连云港市厉庄高级中学2022-2023学年高三上学期第一次质量检测化学试题
4 . 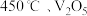 催化
催化 和
和 反应时、能量变化如图所示,反应机理如下:
反应时、能量变化如图所示,反应机理如下:
反应①: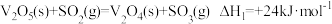
反应②: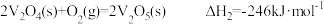

下列说法正确的是
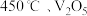 催化
催化 和
和 反应时、能量变化如图所示,反应机理如下:
反应时、能量变化如图所示,反应机理如下:反应①:
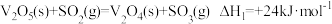
反应②:
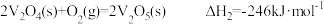

下列说法正确的是
A.反应①的 |
| B.反应②是慢反应,决定该反应速率 |
C.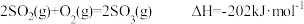 |
D.使用 可以降低反应的焓变 可以降低反应的焓变 |
您最近一年使用:0次
名校
5 . 有效去除废水中的H2SiF6、F-,改善水质是环境部门的重要研究课题。
(1)AlF3是有机合成中常用催化剂,利用废水中的H2SiF6可转变制得,相关的热化学方程式如下:
3H2SiF6(aq)+2Al(OH)3(s)=Al2(SiF6)3(aq)+6H2O(l);ΔH=akJ·mol-1
Al2(SiF6)3(aq)+6H2O(l)=2AlF3(aq)+3SiO2(s)+12HF(aq);ΔH=bkJ·mol-1
3HF(aq)+Al(OH)3(s)=AlF3(aq)+3H2O(l);ΔH=ckJ·mol-1
则反应H2SiF6(aq)+2Al(OH)3(s)=2AlF3(aq)+SiO2(s)+4H2O(l)的ΔH=__ kJ·mol-1。
(2)废水的酸碱度及废水中的Fe3+对F-浓度的测定都会产生一定的影响。
①测定时,通常控制废水的pH在5~6之间。pH过小所测F-浓度偏低,其原因是__ 。
②Fe3+与柠檬酸根(C6F5O73-)、F-反应可表示为Fe3++nC6H5O73- Fe(C6H5O7)n(3n-3)-、Fe3++nF-
Fe(C6H5O7)n(3n-3)-、Fe3++nF- FeFn(3-n)。向含有Fe3+的含氟废水中加入柠檬酸钠(C6H5O7Na3)可消除Fe3+对F-测定的干扰,其原因是
FeFn(3-n)。向含有Fe3+的含氟废水中加入柠檬酸钠(C6H5O7Na3)可消除Fe3+对F-测定的干扰,其原因是__ 。
(3)利用聚苯胺可吸附去除水中F-。用惰性电极电解苯胺( )和盐酸的混合液可在阳极获得聚苯胺薄膜,变化过程如图:
)和盐酸的混合液可在阳极获得聚苯胺薄膜,变化过程如图:

写出阳极生成二聚体的电极反应方程式:___ 。
(4)利用MgCO3、Ca(OH)2和CaCO3等可沉淀去除废水中F-。
①以MgCl2溶液、尿素[CO(NH2)2]为原料可制得MgCO3,写出该反应的化学方程式:__ 。
②取三份相同的含F-的酸性废水,分别加入足量的MgCO3、Ca(OH)2和CaCO3。相同时间后溶液的pH及F-残留量如图1所示。实际废水处理过程中常选用MgCO3的理由是:__ 。

③改变碳酸镁添加量,处理后废水中F-含量及溶液pH的变化如图2所示。添加量超过2.4g·L-1后,F-含量略有升高的原因是___ 。{Ksp(MgF2)=7.4×10-11,Ksp[Mg(OH)2]=5.6×10-12}
(1)AlF3是有机合成中常用催化剂,利用废水中的H2SiF6可转变制得,相关的热化学方程式如下:
3H2SiF6(aq)+2Al(OH)3(s)=Al2(SiF6)3(aq)+6H2O(l);ΔH=akJ·mol-1
Al2(SiF6)3(aq)+6H2O(l)=2AlF3(aq)+3SiO2(s)+12HF(aq);ΔH=bkJ·mol-1
3HF(aq)+Al(OH)3(s)=AlF3(aq)+3H2O(l);ΔH=ckJ·mol-1
则反应H2SiF6(aq)+2Al(OH)3(s)=2AlF3(aq)+SiO2(s)+4H2O(l)的ΔH=
(2)废水的酸碱度及废水中的Fe3+对F-浓度的测定都会产生一定的影响。
①测定时,通常控制废水的pH在5~6之间。pH过小所测F-浓度偏低,其原因是
②Fe3+与柠檬酸根(C6F5O73-)、F-反应可表示为Fe3++nC6H5O73-
 Fe(C6H5O7)n(3n-3)-、Fe3++nF-
Fe(C6H5O7)n(3n-3)-、Fe3++nF- FeFn(3-n)。向含有Fe3+的含氟废水中加入柠檬酸钠(C6H5O7Na3)可消除Fe3+对F-测定的干扰,其原因是
FeFn(3-n)。向含有Fe3+的含氟废水中加入柠檬酸钠(C6H5O7Na3)可消除Fe3+对F-测定的干扰,其原因是(3)利用聚苯胺可吸附去除水中F-。用惰性电极电解苯胺(
 )和盐酸的混合液可在阳极获得聚苯胺薄膜,变化过程如图:
)和盐酸的混合液可在阳极获得聚苯胺薄膜,变化过程如图:
写出阳极生成二聚体的电极反应方程式:
(4)利用MgCO3、Ca(OH)2和CaCO3等可沉淀去除废水中F-。
①以MgCl2溶液、尿素[CO(NH2)2]为原料可制得MgCO3,写出该反应的化学方程式:
②取三份相同的含F-的酸性废水,分别加入足量的MgCO3、Ca(OH)2和CaCO3。相同时间后溶液的pH及F-残留量如图1所示。实际废水处理过程中常选用MgCO3的理由是:

③改变碳酸镁添加量,处理后废水中F-含量及溶液pH的变化如图2所示。添加量超过2.4g·L-1后,F-含量略有升高的原因是
您最近一年使用:0次
2020-05-27更新
|
174次组卷
|
3卷引用:江苏省连云港市老六所四星高中(海州高中 、赣榆高中 、海头中学 、东海高中 新海高中 、灌云高中)2020届高三模拟考试化学试题
江苏省连云港市老六所四星高中(海州高中 、赣榆高中 、海头中学 、东海高中 新海高中 、灌云高中)2020届高三模拟考试化学试题(已下线)江苏省七市(南通、泰州、扬州、徐州、淮安、宿迁、连云港)2019届高三第三次调研考试 化学试题江苏省南京市高淳高级中学2021届高三10月阶段性检测化学试题



