1 . 已知室温下,将 CuSO4·5H2O(s)溶于水会使溶液温度降低, 将 CuSO4(s)溶于水会使溶液温度升高。则下列能量转化关系的判断不正确的是
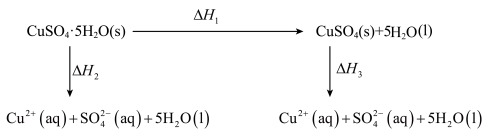

| A.∆H1>0 | B.∆H2>∆H3 | C.∆H3>∆H1 | D.∆H2=∆H1+∆H3 |
您最近一年使用:0次
2021-08-11更新
|
954次组卷
|
28卷引用:【校级联考】福建省平和一中、南靖一中等五校2018-2019学年高二上学期第一次联考化学试题
【校级联考】福建省平和一中、南靖一中等五校2018-2019学年高二上学期第一次联考化学试题福建省福州市第四十中学2021-2022学年高二上学期9月阶段测试化学试题浙江省学考选考科目考试绍兴市适应性试卷(2018年3月)化学试题(已下线)【新东方】高中化学165浙江省丽水市2017-2018学年高二下学期期末教学质量监控化学试题山东省菏泽市2020-2021学年高二上学期期中考试化学试题(A)安徽省临泉第一中学2020-2021学年高二上学期第三次月考化学试题广西钦州市2020-2021学年高二上学期期末教学质量监测化学试题广西南宁市宾阳县宾阳中学2021-2022学年高二上学期10月月考化学试题浙江省杭州市富阳区实验中学2021-2022学年高二上学期10月月考化学试题(已下线)2021年6月浙江高考化学试题变式题21-25河南省南阳市第六完全学校高级中学2022-2023学年高二上学期9月半月考化学试题浙江省台州市书生中学等三校2022-2023学年高二上学期第一次月考化学试题陕西省汉中市洋县中学2022-2023学年高二上学期期中考试化学试题(已下线)专题02 盖斯定律、反应热的计算【考题猜想】(6大题型)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)(已下线)2019年9月15日 《每日一题》2020年一轮复习 —— 每周一测(已下线)专题6.1 化学能与热能(讲)——2020年高考化学一轮复习讲练测(已下线)课时29 盖斯定律及反应热计算-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(浙江专用)河北省保定市唐县一中2021-2022学年高三上学期第二次月考化学试题(已下线)专题09 化学反应与能量变化-备战2022年高考化学学霸纠错(全国通用)广东省广州市广东华侨中学2021-2022学年高一下学期期中考试化学试题(已下线)考点17 化学反应的热效应-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第25练 反应热的计算-2023年高考化学一轮复习小题多维练(全国通用)陕西省延安市第一中学2021-2022学年高一下学期第二次月考化学试题浙江省宁波市北仑中学2022-2023学年高一下学期期中考试化学(选考)试题(已下线)考点17 化学反应的热效应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
2 . 科学家利用Li4SiO4吸附CO2,对于实现废气资源的再利用及碳循环经济技术的发展都具有重要意义。回答下列问题:
(1)可用Li2CO3与SiO2反应制取吸附剂Li4SiO4。
已知:2Li2O(s)+SiO2(s)=Li4SiO4(s) ΔH1=akJ⋅mol-1
Li2CO3(s)+SiO2(s)=Li2SiO3(s)+CO2(g) ΔH2=bkJ⋅mol-1
Li2SiO3(s)=Li2O(s)+SiO2(s) ΔH3=ckJ⋅mol-1
则2Li2CO3(s)+SiO2(s)=Li4SiO4(s)+2CO2(g) ΔH=______ kJ⋅mol−1(用含a、b、c的式子表示)。
(2)CO2的吸附回收及材料再生的原理如下图所示:
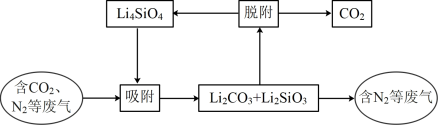
“吸附”过程中主要反应的化学方程式为______ 。
(3)为了探究Li4SiO4的吸附效果,在刚性容器中放入1000g的Li4SiO4吸附剂,通入10.0mol不同比例的N2和CO2混合气体,控制反应时间均为2小时,得到Li4SiO4吸附CO2后固体样品质量百分数与温度的关系如下图所示。
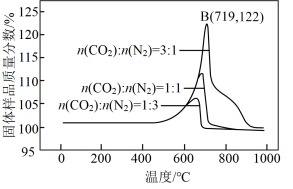
①该反应为______ 反应(填“吸热”或“放热”)。
②A点的v正_____ v逆(填“>”、“<”或“=”),理由是_____ 。
③不同CO2的体积分数对于吸附速率的影响是______ 。
④保持B点的温度不变,若所用刚性容器体积为原来的一半,则平衡时理论上c(CO2)较原平衡______ (填“增大”、“减小”或“不变”)。
⑤B点CO2的吸收率为______ (保留3位有效数字)。
(1)可用Li2CO3与SiO2反应制取吸附剂Li4SiO4。
已知:2Li2O(s)+SiO2(s)=Li4SiO4(s) ΔH1=akJ⋅mol-1
Li2CO3(s)+SiO2(s)=Li2SiO3(s)+CO2(g) ΔH2=bkJ⋅mol-1
Li2SiO3(s)=Li2O(s)+SiO2(s) ΔH3=ckJ⋅mol-1
则2Li2CO3(s)+SiO2(s)=Li4SiO4(s)+2CO2(g) ΔH=
(2)CO2的吸附回收及材料再生的原理如下图所示:

“吸附”过程中主要反应的化学方程式为
(3)为了探究Li4SiO4的吸附效果,在刚性容器中放入1000g的Li4SiO4吸附剂,通入10.0mol不同比例的N2和CO2混合气体,控制反应时间均为2小时,得到Li4SiO4吸附CO2后固体样品质量百分数与温度的关系如下图所示。

①该反应为
②A点的v正
③不同CO2的体积分数对于吸附速率的影响是
④保持B点的温度不变,若所用刚性容器体积为原来的一半,则平衡时理论上c(CO2)较原平衡
⑤B点CO2的吸收率为
您最近一年使用:0次
2021-04-06更新
|
179次组卷
|
2卷引用:福建省漳州市2021届高中毕业班第二次教学质量检测化学试题
名校
解题方法
3 . 白磷、红磷是磷的两种同素异形体,在空气中燃烧得到磷的氧化物,空气不足时生成 P4O6,空气充足时生成 P4O10。
(1)已知 298K 时白磷、红磷完全燃烧的热化学方程式分别为
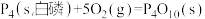 △H1 =-2983.2kJ/mol
△H1 =-2983.2kJ/mol
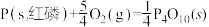 △H2 =-738.5kJ/mol
△H2 =-738.5kJ/mol
则该温度下白磷转化为红磷的热化学方程式为________________________ .
(2)已知 298K 时白磷不完全燃烧的热化学方程式为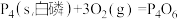 △H =-1638kJ/mol。在某密闭容器中加入 62g 白磷和50.4L氧气(标准状况),控制条件使之恰好完全反应。则所得到的P4O6 与P4O10 的物质的量之比为
△H =-1638kJ/mol。在某密闭容器中加入 62g 白磷和50.4L氧气(标准状况),控制条件使之恰好完全反应。则所得到的P4O6 与P4O10 的物质的量之比为________________ ,反应过程中放出的热为_________________
(3)已知白磷和 PCl3 的分子结构如图所示,现提供以下化学键的键能(KJ/mol):P-P:198, Cl-Cl:243, P-Cl :331 .
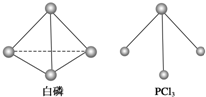
则反应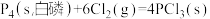 的反应热 △H2 =
的反应热 △H2 =__________ .
(1)已知 298K 时白磷、红磷完全燃烧的热化学方程式分别为
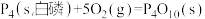 △H1 =-2983.2kJ/mol
△H1 =-2983.2kJ/mol 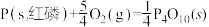 △H2 =-738.5kJ/mol
△H2 =-738.5kJ/mol 则该温度下白磷转化为红磷的热化学方程式为
(2)已知 298K 时白磷不完全燃烧的热化学方程式为
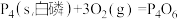 △H =-1638kJ/mol。在某密闭容器中加入 62g 白磷和50.4L氧气(标准状况),控制条件使之恰好完全反应。则所得到的P4O6 与P4O10 的物质的量之比为
△H =-1638kJ/mol。在某密闭容器中加入 62g 白磷和50.4L氧气(标准状况),控制条件使之恰好完全反应。则所得到的P4O6 与P4O10 的物质的量之比为(3)已知白磷和 PCl3 的分子结构如图所示,现提供以下化学键的键能(KJ/mol):P-P:198, Cl-Cl:243, P-Cl :331 .

则反应
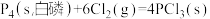 的反应热 △H2 =
的反应热 △H2 =
您最近一年使用:0次
2019-11-21更新
|
346次组卷
|
12卷引用:【校级联考】福建省平和一中、南靖一中等五校2018-2019学年高二上学期第一次联考化学试题
【校级联考】福建省平和一中、南靖一中等五校2018-2019学年高二上学期第一次联考化学试题(已下线)2012-2013学年江西省南昌市第二中学高二第一次月考化学试卷(已下线)2014高考名师推荐化学盖斯定律及其应用2016-2017学年江苏省泰州中学高二上月考一化学试卷河南省鹤壁市淇滨高级中学2017-2018学年高二上学期第二次月考化学试题山西省朔州市平鲁区李林中学2018-2019学年高二上学期第一次月考化学试题四川省遂宁市第二中学2019-2020学年高二上学期期中考试化学试题(已下线)专题1 化学反应与能量(章末培优)-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)黑龙江省哈尔滨市依兰县高级中学2021-2022学年高二上学期第一次月考化学试题(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练黑龙江省宾县第一中学校2021-2022学年高三上学期第一次月考化学试题



