1 . 如图所示,有关化学反应和能量变化的说法正确的是
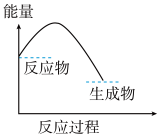

| A.铝热反应属于氧化还原反应,故能量变化不符合该图 |
| B.Ba(OH)2•8H2O晶体和NH4Cl晶体反应能量变化如图所示 |
| C.符合该能量变化的化学反应均可用于设计成原电池 |
| D.反应物总键能小于产物总键能的反应符合该图的能量变化 |
您最近一年使用:0次
2 . 下列说法正确的是
| A.需要加热才能发生的反应一定是吸热反应 |
| B.化学反应一定伴有能量的变化,但有能量变化的未必就是化学反应 |
| C.凡是化合反应都是放热反应,凡是分解反应都是吸热反应 |
| D.C(石墨,s)=C(金刚石,s) ΔH>0,则金刚石比石墨稳定 |
您最近一年使用:0次
3 . (Ⅰ)请回答下列问题:
(1)在101kPa时,一定量的CO在1.00mol O2中完全燃烧,生成2.00mol CO2,放出566.0kJ热量,CO的燃烧热为ΔH=_______ ,表示CO燃烧热的热化学方程式_______ 。
(Ⅱ)试分别从能量变化和化学键变化角度研究反应2H2(g)+O2(g)=2H2O(l)的焓变。
(2)已知该反应为放热反应,下图能正确表示该反应中能量变化的是_______ 。
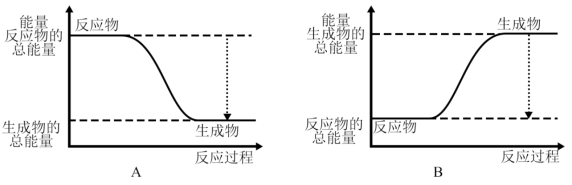
(3)从断键和成键的角度分析上述反应中能量的变化。已知化学键的键能:
由此计算2mol H2在氧气中完全燃烧生成气态水放出的热量_______ 。
(Ⅲ)依据盖斯定律回答下列问题:
已知火箭发射时可用肼(N2H4)作燃料,二氧化氮作氧化剂,这两者反应生成氮气和水蒸气。
且N2(g)+2O2(g)=2NO2(g);ΔH1=+67.7kJ/mol ①
N2H4(g)+O2(g)=N2(g)+2H2O(g);ΔH2=-534kJ/mol ②
(4)写出肼与NO2反应的热应化学方程式_______ 。
(1)在101kPa时,一定量的CO在1.00mol O2中完全燃烧,生成2.00mol CO2,放出566.0kJ热量,CO的燃烧热为ΔH=
(Ⅱ)试分别从能量变化和化学键变化角度研究反应2H2(g)+O2(g)=2H2O(l)的焓变。
(2)已知该反应为放热反应,下图能正确表示该反应中能量变化的是

(3)从断键和成键的角度分析上述反应中能量的变化。已知化学键的键能:
| 化学键 | H-H | O=O | H-O |
| 键能/kJ·mol-1 | 436 | 496 | 463 |
(Ⅲ)依据盖斯定律回答下列问题:
已知火箭发射时可用肼(N2H4)作燃料,二氧化氮作氧化剂,这两者反应生成氮气和水蒸气。
且N2(g)+2O2(g)=2NO2(g);ΔH1=+67.7kJ/mol ①
N2H4(g)+O2(g)=N2(g)+2H2O(g);ΔH2=-534kJ/mol ②
(4)写出肼与NO2反应的热应化学方程式
您最近一年使用:0次
4 . 氢卤酸的能量关系如图所示,下列说法错误的是
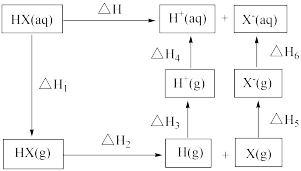

| A.相同条件下,HBr的△H2比HI的大 |
| B.相同条件下,HCl的△H3+△H4与HBr的相等 |
| C.已知HF气体溶于水放热,则HF的△H1>0 |
| D.一定条件下,气态原子生成1molH-X键放出akJ能量,则该条件下的△H2=-akJ•mol-1 |
您最近一年使用:0次
解题方法
5 . 如图是C和H2O(g)反应的能量变化图示,下列说法正确的是
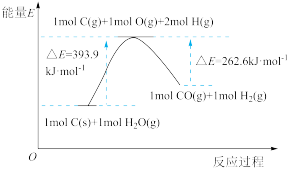

| A.该反应为吸热反应 |
| B.1 mol C(g)和1 mol H2O(g)具有的总能量低于1 mol C(s)和1 mol H2O(g)具有的总能量 |
| C.1 mol C(s)和1 mol H2O(g)反应生成1 mol CO(g)和1 mol H2(g),吸收131.3 kJ热量 |
| D.1 mol H2O(g)中O-H键断裂需要吸收393.9 kJ热量 |
您最近一年使用:0次
名校
6 . 如图所示,有关化学反应和能量变化的说法不正确的是
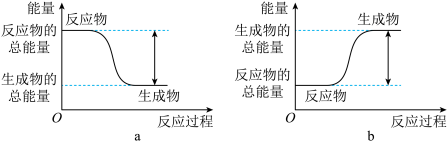

| A.图a表示的是放热反应的能量变化 |
| B.图b表示反应物的化学键断裂吸收的总能量高于生成物的化学键形成释放的总能量 |
| C.图a表示的反应不需要加热就一定能发生,图b表示的反应一定需要加热才能发生 |
| D.图b可以表示氯化铵固体与氢氧化钡晶体反应的能量变化 |
您最近一年使用:0次
2022-09-15更新
|
377次组卷
|
5卷引用:贵州省黔西南州兴义市同源中学2021-2022学年高二上学期期中考试化学试题
名校
7 . 下列说法正确的是
| A.反应热是1mol物质参加反应时的能量变化 |
| B.需要加热才能发生的反应一定是吸热反应 |
| C.任何条件下,化学反应的焓变都等于化学反应的反应热 |
| D.在一定条件下,某一化学反应是吸热反应还是放热反应,由生成物与反应物能量的相对大小来决定 |
您最近一年使用:0次
2022-09-15更新
|
248次组卷
|
3卷引用:贵州省黔西南州兴义市同源中学2021-2022学年高二上学期期中考试化学试题
8 . 可逆反应2NO2 (g)⇌N2O4 (g) ΔH= −56.9 kJ·mol−1在平衡移动时的颜色变化可以用来指示放热过程和吸热过程。下面是某同学的部分实验报告。
(1)甲烧杯中NO2球的红棕色变浅,说明平衡2NO2 (g)⇌N2O4 (g)向_______ (填“正反应”或“逆反应”)方向移动,所以NH4NO3晶体溶于水是_______ (填“放热”或“吸热”)过程。
(2)根据乙烧杯中的现象,补全CaO与H2O反应过程的能量变化示意图_______ 。

(3)改变下列条件都可使反应的反应速率改变,其中通过降低活化能加快反应速率的是_______ 。
a.浓度 b.压强 c.温度 d.催化剂
 | 1.向甲烧杯中加入NH4NO3晶体,此烧杯中NO2球的红棕色变浅。 2.向乙烧杯中投入一定量的CaO固体,此烧杯中NO2球的红棕色变深。 |
(2)根据乙烧杯中的现象,补全CaO与H2O反应过程的能量变化示意图

(3)改变下列条件都可使反应的反应速率改变,其中通过降低活化能加快反应速率的是
a.浓度 b.压强 c.温度 d.催化剂
您最近一年使用:0次
9 . 下列与化学反应过程中的能量变化相关的叙述中,不正确的是
| A.化学反应热效应数值与参加反应的物质多少有关 |
| B.放热反应的反应速率总是大于吸热反应的反应速率 |
| C.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| D.化学反应过程中的能量变化除了热能外,也可以是光能、电能等 |
您最近一年使用:0次
2022-09-15更新
|
153次组卷
|
3卷引用:北京市第一五九中学2021-2022学年高二上学期期中考试化学试题
解题方法
10 . 为了探究化学能与热能的转化,某实验小组设计了如图所示的三套实验装置:
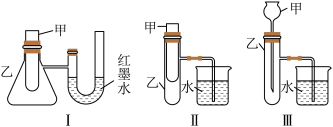
(1)上述3个装置中,不能证明“铜与浓硝酸反应是吸热反应还是放热反应”的是(不能用手触摸和使用温度计)_____ 。
(2)某同学选用装置I进行实验(实验前U形管里液面左右相平),在甲试管里加入适量氢氧化钠溶液与稀盐酸,U形管中可观察到的现象是_____ ,说明该反应属于____ (填“吸热反应”或“放热反应”)。
(3)为定量测定(2)中反应的反应热,使50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在简易量热计中进行中和反应。回答下列问题:
①该实验中NaOH的浓度大于盐酸的浓度的作用是_____ 。
②实验中若改用60mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液进行反应,与上述实验相比,所求中和热_____ (填“相等”或“不相等”)。
(4)已知一些化学键的键能数据如表所示:
请根据键能数据估算CH4(g)和F2(g)反应生成CF4(g)和HF(g)的热化学方程式:_____ 。
(5)已知反应:N2(g)+O2(g)=2NO(g) △H1
2H2(g)+O2(g)=2H2O(g) △H2
N2(g)+3H2(g)=2NH3(g) △H3
利用上述三个反应,计算4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H4的反应焓变为____ (用含△H1、△H2、△H3的式子表示)。

(1)上述3个装置中,不能证明“铜与浓硝酸反应是吸热反应还是放热反应”的是(不能用手触摸和使用温度计)
(2)某同学选用装置I进行实验(实验前U形管里液面左右相平),在甲试管里加入适量氢氧化钠溶液与稀盐酸,U形管中可观察到的现象是
(3)为定量测定(2)中反应的反应热,使50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在简易量热计中进行中和反应。回答下列问题:
①该实验中NaOH的浓度大于盐酸的浓度的作用是
②实验中若改用60mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液进行反应,与上述实验相比,所求中和热
(4)已知一些化学键的键能数据如表所示:
| 化学键 | C-H | C-F | H-F | F-F |
| 键能/kJ•mol-1 | 414 | 489 | 565 | 155 |
(5)已知反应:N2(g)+O2(g)=2NO(g) △H1
2H2(g)+O2(g)=2H2O(g) △H2
N2(g)+3H2(g)=2NH3(g) △H3
利用上述三个反应,计算4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H4的反应焓变为
您最近一年使用:0次



