1 . 将20g Ba(OH)2·8H2O研细后与10g NH4Cl晶体一起放入烧杯中,用玻璃棒快速搅拌。实验现象为:
①___________ ;②______________ ;③_________ 。发生反应的化学方程式是_________ 。
①
您最近一年使用:0次
2 . 某同学进行如下实验,研究化学反应中的热量变化。
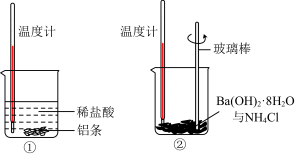
请回答下列问题:
(1)反应后①中温度升高,②中温度降低。由此判断铝条与盐酸的反应是________ 反应(填“放热”或“吸热”,下同),Ba(OH)2·8H2O与NH4Cl的反应是________ 反应。
(2)①中反应的离子方程式是_________ ,该反应的还原剂是_________ 。

请回答下列问题:
(1)反应后①中温度升高,②中温度降低。由此判断铝条与盐酸的反应是
(2)①中反应的离子方程式是
您最近一年使用:0次
2019-07-16更新
|
1087次组卷
|
4卷引用:北京市西城区2018-2019学年高一第二学期期末考试化学试题
北京市西城区2018-2019学年高一第二学期期末考试化学试题2019-2020学年新人教版必修2同步练习题:6.1化学反应与能量变化(已下线)专题04 化学能与热能(核心素养卷)-【新教材精创】2019-2020学年高一化学新教材知识讲学(必修第二册)北京市西城区高一化学下学期前三章综合阶段性试卷
3 . 在一个小烧杯里加入约20 g已研磨成粉末的氢氧化钡晶体[Ba(OH) 2 ·8H 2 O],将小烧杯放在事先已滴有3~4滴水的玻璃片上,然后向烧杯内加入约10 g氯化铵晶体,并立即用玻璃棒迅速搅拌。试回答下列问题:
(1)写出反应的化学方程式:_____________________________ 。
(2)实验中要立即用玻璃棒迅速搅拌的原因是___________________________ 。
(3)如果实验中没有看到“结冰”现象,可能的原因是_____________________________ (答出一条即可)。
(4)如果没有看到“结冰”现象,我们还可以采取哪些方式来说明该反应吸热?___________________ (答出两种方案)。
(5)“结冰”现象说明该反应是一个________ (填“放出”或“吸收”)能量的反应。即断开旧化学键______ (填“吸收”或“放出”)的能量________ (填“>”或“<”)形成新化学键________ (填“吸收”或“放出”)的能量。
(6)该反应在常温下就可进行,说明_________________________________
(1)写出反应的化学方程式:
(2)实验中要立即用玻璃棒迅速搅拌的原因是
(3)如果实验中没有看到“结冰”现象,可能的原因是
(4)如果没有看到“结冰”现象,我们还可以采取哪些方式来说明该反应吸热?
(5)“结冰”现象说明该反应是一个
(6)该反应在常温下就可进行,说明
您最近一年使用:0次
2019-05-31更新
|
91次组卷
|
2卷引用:【校级联考】吉林省长春市九台区师范高中、实验高中2018-2019学年高一下学期期中考试化学试题
名校
4 . 在一试管中放入几小块镁片,把试管放入盛有25 ℃的饱和石灰水的烧杯中,用胶头滴管滴入5 mL1 mol/L盐酸于试管中。试回答下列问题:
(1)实验中产生的现象是_________ 。
(2)产生上述现象的原因是____________ 。
(3)写出有关的离子方程式:____________ 。
(4)由实验推知:MgCl2溶液与H2的总能量________ (填“<”“>”或“=”)镁片和盐酸的总能量。
(5)实验室制氢气常用____________ ,为什么不用镁的原因是____________ 。
(1)实验中产生的现象是
(2)产生上述现象的原因是
(3)写出有关的离子方程式:
(4)由实验推知:MgCl2溶液与H2的总能量
(5)实验室制氢气常用
您最近一年使用:0次
2019-05-04更新
|
144次组卷
|
3卷引用:【校级联考】江西省赣州市五校协作体2018-2019学年高一下学期期中联考化学试题
名校
5 . 室温下将40 g已磨成粉末的Ba(OH)2•8H2O和20 g NH4Cl置于250 mL锥形瓶中,迅速搅拌将固体药品混合均匀,20 s后用带有玻璃管的单孔橡皮塞塞紧瓶口,玻璃管口悬挂一湿润的红色石蕊试纸,如图所示。试回答:
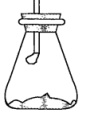
(1)湿润的红色石蕊试纸的变化是________ ,用化学方程式作出相关解释_______ 。
(2)若将锥形瓶中的Ba(OH)2•8H2O和NH4Cl换成__________ ,也可出现装置内温度降低的现象。

(1)湿润的红色石蕊试纸的变化是
(2)若将锥形瓶中的Ba(OH)2•8H2O和NH4Cl换成
您最近一年使用:0次
6 . 能源是现代社会发展的支柱之一。
(1)化学反应中的能量变化,主要表现为热量的变化。
①下列反应中,属于放热反应的是_________ (填字母)。
a.Ba(OH)2·8H2O与NH4Cl混合搅拌
b.高温煅烧石灰石
c.铝与盐酸反应
②某同学进行如图所示实验,测量稀盐酸与烧碱溶液中和反应的能量变化。实验表明,反应温度升高;由此判断该反应是_____________ (填“吸热”或“放热”)反应,其离子方程式是__________________________ 。
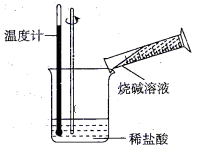
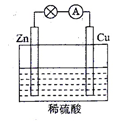
(2)电能是现代社会应用最广泛的能源之一。如图所示的原电池装置中,负极是____ ,正极上能够观察到的现象是________ ,正极的电极反应式是____________ 。原电池工作一段时间后,若消耗锌6.5 g,则放出气体_______ g。
(1)化学反应中的能量变化,主要表现为热量的变化。
①下列反应中,属于放热反应的是
a.Ba(OH)2·8H2O与NH4Cl混合搅拌
b.高温煅烧石灰石
c.铝与盐酸反应
②某同学进行如图所示实验,测量稀盐酸与烧碱溶液中和反应的能量变化。实验表明,反应温度升高;由此判断该反应是

(2)电能是现代社会应用最广泛的能源之一。如图所示的原电池装置中,负极是

您最近一年使用:0次
2018-08-02更新
|
339次组卷
|
5卷引用:2012-2013学年北京市西城区(北区)高一下学期期末考试化学试卷
(已下线)2012-2013学年北京市西城区(北区)高一下学期期末考试化学试卷(已下线)2012-2013学年山东省聊城市四县六校高一下学期期末联考化学试卷黑龙江省伊春市第二中学2017-2018学年高一下学期期末考试(理)化学试题陕西省榆林市绥德中学2017-2018学年高一下学期期末考试化学试题河北省张家口市尚义县第一中学2019-2020学年高一下学期期中考试化学试题
解题方法
7 . Ⅰ.化学反应中的焓变(Δ H)与反应物和生成物的键能(E)有关。下表给出了一些化学键的键能:
已知工业合成氨: N2(g)+3H2(g) 2NH3(g) Δ H= -92.4 kJ· mol-1, 请回答下列问题:
2NH3(g) Δ H= -92.4 kJ· mol-1, 请回答下列问题:
(1)表中 a =______ kJ· mol-1
(2)1 mol N2和 3 mol H2充分反应,放出的热量______ 92.4 kJ(填“>”、“<”或“=”)。
II.随着人类对温室效应和资源短缺等问题的重视,如何降低大气中 CO2的含量及有效地开发利用CO2,引起了普遍的重视。
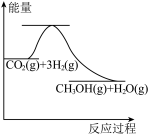
(1)目前工业上有一种方法是用 CO2来生产甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。下图表示该反应进行过程中能量的变化,该反应是
CH3OH(g)+H2O(g)。下图表示该反应进行过程中能量的变化,该反应是_____ (填“吸热”或“放热”)反应;
(2)下列各项中,能说明 CO2(g)+3H2(g) CH3OH(g)+H2O(g)已达到平衡的是
CH3OH(g)+H2O(g)已达到平衡的是____ (填选项)。
A.恒温、恒容条件下,容器内的压强不发生变化
B.一定条件下,CH3OH 分解的速率和 CH3OH 生成的速率相等
C.一定条件下,单位时间内消耗 1 mol CO2,同时生成 1 mol CH3OH
D.一定条件下,H2O(g)的浓度保持不变
| 化学键 | H-H | N≡N | O=O | O-H | N-H |
| 键能(kJ/mol) | 436 | 942 | 500 | 463 | a |
 2NH3(g) Δ H= -92.4 kJ· mol-1, 请回答下列问题:
2NH3(g) Δ H= -92.4 kJ· mol-1, 请回答下列问题:(1)表中 a =
(2)1 mol N2和 3 mol H2充分反应,放出的热量
II.随着人类对温室效应和资源短缺等问题的重视,如何降低大气中 CO2的含量及有效地开发利用CO2,引起了普遍的重视。
(1)目前工业上有一种方法是用 CO2来生产甲醇:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。下图表示该反应进行过程中能量的变化,该反应是
CH3OH(g)+H2O(g)。下图表示该反应进行过程中能量的变化,该反应是
(2)下列各项中,能说明 CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)已达到平衡的是
CH3OH(g)+H2O(g)已达到平衡的是A.恒温、恒容条件下,容器内的压强不发生变化
B.一定条件下,CH3OH 分解的速率和 CH3OH 生成的速率相等
C.一定条件下,单位时间内消耗 1 mol CO2,同时生成 1 mol CH3OH
D.一定条件下,H2O(g)的浓度保持不变
您最近一年使用:0次
名校
解题方法
8 . 某实验小组同学进行如下实验,以探究化学反应中的能量变化。
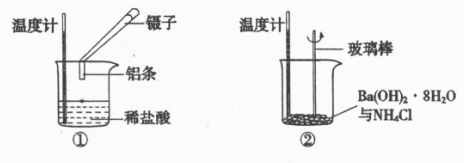
(1)实验表明:②中的温度降低,由此判断氢氧化钡晶体与氯化铵晶体反应是____________ (填“吸热”或“放热”)反应。
(2)实验①中,该小组同学在烧杯中加入5 mL 1.0 mol/L盐酸,再放入用砂纸打磨过的铝条,观察产生H2的速率,如图A所示,该反应是________ (填“吸热”或“放热”)反应,其能量变化可用下图中的___________ (填“B”或“C”)表示。

A中0—t1段化学反应速率变化的原因是__________________ 。

(1)实验表明:②中的温度降低,由此判断氢氧化钡晶体与氯化铵晶体反应是
(2)实验①中,该小组同学在烧杯中加入5 mL 1.0 mol/L盐酸,再放入用砂纸打磨过的铝条,观察产生H2的速率,如图A所示,该反应是

A中0—t1段化学反应速率变化的原因是
您最近一年使用:0次
2018-06-15更新
|
279次组卷
|
2卷引用:【全国百强校】北京四中2017-2018学年下学期高一年级期中考试化学试卷(学考)
2016高二·全国·课时练习
名校
解题方法
9 . 某学习小组设计以下实验,探究化学反应中的热效应,把试管放入盛有25℃的饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管往其中滴加5 mL盐酸。
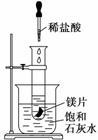
试回答下列问题:
(1)实验中观察到的现象是_____________________________________________ 。
(2)产生上述现象的原因是____________________________________________ 。
(3)写出有关反应的离子方程式______________________________________ 。
(4)由实验推知,MgCl2和H2的总能量______ (填“大于”、“小于”或“等于”)镁片和盐酸的总能量。
(5)如果将本题中“25℃的饱和石灰水”换成“20℃碳酸饮料”进行实验探究,实验中观察到的另一现象是________________________________________________________________ ,其原因是_________________________________________________________________ 。

试回答下列问题:
(1)实验中观察到的现象是
(2)产生上述现象的原因是
(3)写出有关反应的离子方程式
(4)由实验推知,MgCl2和H2的总能量
(5)如果将本题中“25℃的饱和石灰水”换成“20℃碳酸饮料”进行实验探究,实验中观察到的另一现象是
您最近一年使用:0次
2017-11-27更新
|
721次组卷
|
4卷引用:同步君 人教版 选修四 第一章 第一节 第二课时 热化学方程式
(已下线)同步君 人教版 选修四 第一章 第一节 第二课时 热化学方程式高中化学人教版 选修四 第一章 化学反应与能量 第一节 化学反应与能量的变化 化学反应与能量第二课时(热化学方程式)(已下线)1.1.1 化学反应的焓变(1)(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)海南省琼海市嘉积中学2023-2024学年高二上学期期末考试化学试题A卷
12-13高一下·广东河源·阶段练习
名校
10 . 如右图所示,把试管放入盛有25 ℃饱和澄清石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入10 mL盐酸于试管中,试回答下列问题:
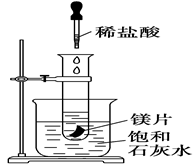
(1)实验中观察到的现象是________________________________ 。
(2)产生上述现象的原因是____________________________ 。
(3)写出有关反应的离子方程式:_________________________________ ;
反应中转移了0. 04mol电子时;标准状况下产生多少________ mL的H2;消耗镁多少________ g(保留两位小数);生成的MgCl2物质的量浓度为________ 。(溶液体积保持不变)
(4)由实验推知,镁片溶液和盐酸的总能量________ (填“大于”、“小于”或“等于”) MgCl2和H2的总能量;此反应为________ (填放热反应或者吸热反应)。

(1)实验中观察到的现象是
(2)产生上述现象的原因是
(3)写出有关反应的离子方程式:
反应中转移了0. 04mol电子时;标准状况下产生多少
(4)由实验推知,镁片溶液和盐酸的总能量
您最近一年使用:0次



