1 . 已知:H2(g)+Cl2(g)=2HCl(g) ΔH=-184.6 kJ·mol-1
2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1452 kJ·mol-1
H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1
下列说法正确的是
2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1452 kJ·mol-1
H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1
下列说法正确的是
A.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照条件和点燃条件下的 不同 不同 |
| B.CH3OH(l)的燃烧热为1452 kJ·mol-1 |
C. H2SO4(aq)+ H2SO4(aq)+ Ba(OH)2(aq)= Ba(OH)2(aq)= BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1 BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1 |
| D.同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多 |
您最近一年使用:0次
2021-04-24更新
|
266次组卷
|
3卷引用:江苏省沭阳县2020-2021学年高二下学期中调研测试化学试题
江苏省沭阳县2020-2021学年高二下学期中调研测试化学试题(已下线)第二节 燃烧热 能源(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)贵州省黔西南布依族苗族自治州2022-2023学年高二上学期期末考试化学试题
解题方法
2 . 已知下列两个热化学方程式:2H2(g) + O2(g) = 2H2O(1) ΔH= -571.6 kJ•mol-1,C3H8(g) + 5O2(g)= 3CO2(g) + 4H2O(l) ΔH= -2220 kJ•mol-1,下列说法正确的是
| A.相同质量H2和C3H8分别完全燃烧,C3H8放出的热量多 |
| B.C3H8 完全燃烧生成1mol H2O(l)放出的热量为555 kJ |
| C.l mol H2和2 molC3H8 组成的混合气体完全燃烧放出的热量为5011.6 kJ |
| D.H2和C3H8的混合气体共4mol,完全燃烧时放出3256 kJ热量,则 n(H2):n(C3H8)=1:1 |
您最近一年使用:0次
2020-05-27更新
|
160次组卷
|
2卷引用:江苏省苏州市2019-2020学年高一下学期期中考试化学试题(新区实验)
解题方法
3 . (1)沼气是一种能源,它的主要成分是CH4,常温下,0.5molCH4完全燃烧生成CO2(g)和液态水时,放出445kJ热量,则热化学方程式为__ 。
(2)已知: N2(g)+
N2(g)+ H2(g)=N(g)+3H(g) ΔH1=+akJ·mol-1
H2(g)=N(g)+3H(g) ΔH1=+akJ·mol-1
N(g)+3H(g)=NH3(g) ΔH2=-bkJ·mol-1
NH3(g)=NH3(l) ΔH3=-ckJ·mol-1
写出N2(g)和H2(g)反应生成液氨的热化学方程式__ 。
(3)SF6是一种优良的绝缘气体,分子结构中,只存在S-F键,已知1molS(s)转化为气态硫原子吸收能量280kJ,F-F键能为160kJ·mol-1,S-F键能为330kJ·mol-1,试写出S(s)和F2(g)反应生成SF6(g)的热化学方程式__ 。
(2)已知:
 N2(g)+
N2(g)+ H2(g)=N(g)+3H(g) ΔH1=+akJ·mol-1
H2(g)=N(g)+3H(g) ΔH1=+akJ·mol-1N(g)+3H(g)=NH3(g) ΔH2=-bkJ·mol-1
NH3(g)=NH3(l) ΔH3=-ckJ·mol-1
写出N2(g)和H2(g)反应生成液氨的热化学方程式
(3)SF6是一种优良的绝缘气体,分子结构中,只存在S-F键,已知1molS(s)转化为气态硫原子吸收能量280kJ,F-F键能为160kJ·mol-1,S-F键能为330kJ·mol-1,试写出S(s)和F2(g)反应生成SF6(g)的热化学方程式
您最近一年使用:0次
2020-02-26更新
|
102次组卷
|
2卷引用:江苏省海安市实验中学2021-2022学年高二上学期第一次月考化学试题
名校
4 . 下列叙述中正确的是
| A.反应MgCl2(l)=Mg(l)+Cl2(g)的ΔH<0、ΔS>0 |
B.加热Na2CO3溶液, 增大 增大 |
| C.由热化学方程式2CO(g)+O2(g)=2CO2 (g) ΔH=-566 kJ·mol-1可知,CO的燃烧热是566 kJ·mol-1 |
| D.中和等体积、等浓度的醋酸和盐酸,醋酸消耗的NaOH的物质的量小 |
您最近一年使用:0次
2019-12-06更新
|
172次组卷
|
2卷引用:江苏省南通一中2018~2019学年高二上学期期末调研模拟化学(选修)试题
5 . CH4既是一种重要的能源,也是一种重要的化工原料。
(1)已知8.0 g CH4完全燃烧生成液态水放出444.8 kJ热量。则CH4 (g)+2O2(g)=CO2(g)+2H2O(l) ΔH=____________ kJ·mol-1。
(2)在一定温度和催化剂作用下,CH4与CO2可直接转化成乙酸,这是实现“减排”的一种研究方向。
①在不同温度下,催化剂的催化效率与乙酸的生成速率如图所示,则该反应的最佳温度应控制在___________ 左右。
②该反应催化剂的有效成分为偏铝酸亚铜 (CuAlO2,难溶物)。将CuAlO2溶解在稀硝酸中生成两种盐并放出NO气体,其离子方程式为_____________________ 。
(3)CH4还原法是处理NOx气体的一种方法。已知一定条件下CH4与NOx反应转化为N2和CO2,若标准状况下8.96 L CH4可处理22.4 L NOx,则x值为_______________ 。
(1)已知8.0 g CH4完全燃烧生成液态水放出444.8 kJ热量。则CH4 (g)+2O2(g)=CO2(g)+2H2O(l) ΔH=
(2)在一定温度和催化剂作用下,CH4与CO2可直接转化成乙酸,这是实现“减排”的一种研究方向。
①在不同温度下,催化剂的催化效率与乙酸的生成速率如图所示,则该反应的最佳温度应控制在
②该反应催化剂的有效成分为偏铝酸亚铜 (CuAlO2,难溶物)。将CuAlO2溶解在稀硝酸中生成两种盐并放出NO气体,其离子方程式为

(3)CH4还原法是处理NOx气体的一种方法。已知一定条件下CH4与NOx反应转化为N2和CO2,若标准状况下8.96 L CH4可处理22.4 L NOx,则x值为
您最近一年使用:0次
名校
6 . 下列过程吸收热量的是 ( )
| A.食物腐败 | B.干冰升华 |
| C.酸碱中和 | D.镁条燃烧 |
您最近一年使用:0次
2018-02-28更新
|
347次组卷
|
2卷引用:南通市2018年高二学业水平测试模拟一 化学 试题
7 . 已知:①H+(aq)+OH-(aq)===H2O(l) ΔH1=-57.3 kJ·mol-1,
②H2(g)+ O2(g)===H2O(g) ΔH2=-241.8 kJ·mol-1,下列有关说法正确的是
O2(g)===H2O(g) ΔH2=-241.8 kJ·mol-1,下列有关说法正确的是
②H2(g)+
 O2(g)===H2O(g) ΔH2=-241.8 kJ·mol-1,下列有关说法正确的是
O2(g)===H2O(g) ΔH2=-241.8 kJ·mol-1,下列有关说法正确的是
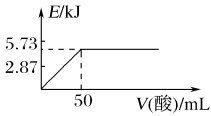
| A.向含0.1 mol NaOH的溶液中加入一定体积的0.1 mol·L-1乙二酸,反应中的能量变化如上图所示 |
| B.H2SO4(aq)+Ba(OH)2(aq)===BaSO4(s)+2H2O(l) ΔH=-114.6 kJ·mol-1 |
| C.氢气的标准燃烧热为241.8 kJ·mol-1 |
| D.若反应②中水为液态,则同样条件下的反应热:ΔH>ΔH2 |
您最近一年使用:0次
2017-08-19更新
|
992次组卷
|
8卷引用:2018版化学(苏教版)高考总复习专题六课时跟踪训练--化学反应的热效应
2018版化学(苏教版)高考总复习专题六课时跟踪训练--化学反应的热效应(已下线)2018年9月16日 《每日一题》一轮复习- 每周一测(已下线)2019年9月15日 《每日一题》2020年一轮复习 —— 每周一测辽宁省大连市旅顺口区2020届高三10月月考化学试题四川省威远中学2019-2020学年高二下学期第二次月考化学试题黑龙江哈尔滨市第九中学2021届高三上学期第三次月考化学试题黑龙江省大庆实验中学2020-2021学年高二上学期期末考试化学试题陕西省西北农林科技大学附属中学2021-2022学年高二上学期期末考试化学试题
名校
8 . 25℃、101kPa时,1g甲醇完全燃烧生成CO2和液态水,同时放出22.68kJ热量,下列表示该反应的热化学方程式的是
A.CH3OH(l)+ O2(g)=CO2(g)+2H2O(l) △H =-725.8kJ/mol O2(g)=CO2(g)+2H2O(l) △H =-725.8kJ/mol |
| B.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) △H =+145.6kJ/mol |
| C.2CH2OH(l)+3O2(g)=2CO2(g)+4H2O(l) △H =-22.68kJ/mol |
D.CH3OH(l) + O2(g)=CO2(g)+2H2O(g) △H =-725.8kJ/mol O2(g)=CO2(g)+2H2O(g) △H =-725.8kJ/mol |
您最近一年使用:0次
2017-04-22更新
|
617次组卷
|
2卷引用:2016-2017学年江苏省沭阳县高二下学期期中调研测试化学试卷
9 . 某种发动机燃料由A、B两种物质混合而成,A、B两种物质含有C、H、O三种元素中的两种或三种。已知常温下A、B及CO、H2的燃烧热如下:
A、B按不同比例混合的燃料91.2g,在足量的氧气中燃烧时,放出的热量Q与B的物质的量分数x的关系如右图。

(1)A、B的相对分子质量为A________ ,B_______ 。
(2)等物质的量的A、B混合的燃料73g,在160LO2中完全燃烧,得到104L气体,通过碱石灰吸收后剩余3.2L(气体体积均在标准状况下测定)。由此可推得混合物中N(C)∶N(H)∶N(O)=__________ ,A分子式为_________ ,B分子式为_________ 。
(3)1mol等物质的量的A、B混合的燃料,在一定量的氧气中燃烧,放出热量2980kJ,则反应中生成CO_________ mol。
| 物 质 | A | B | CO | H2 |
| 燃烧热/kJ·mol-1 | 725 | 5518 | 283 | 286 |
A、B按不同比例混合的燃料91.2g,在足量的氧气中燃烧时,放出的热量Q与B的物质的量分数x的关系如右图。

(1)A、B的相对分子质量为A
(2)等物质的量的A、B混合的燃料73g,在160LO2中完全燃烧,得到104L气体,通过碱石灰吸收后剩余3.2L(气体体积均在标准状况下测定)。由此可推得混合物中N(C)∶N(H)∶N(O)=
(3)1mol等物质的量的A、B混合的燃料,在一定量的氧气中燃烧,放出热量2980kJ,则反应中生成CO
您最近一年使用:0次



