名校
解题方法
1 . 碳元素及其化合物在自然界广泛存在且具有重要应用。 具有较大的燃烧热
具有较大的燃烧热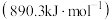 ,是常见燃料。用
,是常见燃料。用 溶液吸收
溶液吸收 生成
生成 溶液是
溶液是 “固定”再利用的方法之一、电解
“固定”再利用的方法之一、电解 溶液可获得
溶液可获得 ;向
;向 溶液中加入铁粉,反应初期产生
溶液中加入铁粉,反应初期产生 并生成
并生成 迅速转化为活性
迅速转化为活性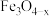 ,活性
,活性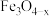 催化
催化 加氢生成
加氢生成 。“侯氏制碱法”是以
。“侯氏制碱法”是以 为原料制备
为原料制备 。下列化学反应表示正确的是
。下列化学反应表示正确的是
 具有较大的燃烧热
具有较大的燃烧热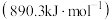 ,是常见燃料。用
,是常见燃料。用 溶液吸收
溶液吸收 生成
生成 溶液是
溶液是 “固定”再利用的方法之一、电解
“固定”再利用的方法之一、电解 溶液可获得
溶液可获得 ;向
;向 溶液中加入铁粉,反应初期产生
溶液中加入铁粉,反应初期产生 并生成
并生成 迅速转化为活性
迅速转化为活性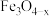 ,活性
,活性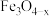 催化
催化 加氢生成
加氢生成 。“侯氏制碱法”是以
。“侯氏制碱法”是以 为原料制备
为原料制备 。下列化学反应表示正确的是
。下列化学反应表示正确的是A.甲烷的燃烧: |
B.铁粉和 溶液反应制 溶液反应制 |
C. 通入氨的饱和食盐水中: 通入氨的饱和食盐水中: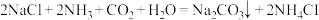 |
D.催化电解 生成 生成 的阳极反应式: 的阳极反应式: |
您最近一年使用:0次
名校
解题方法
2 . 下列方程式与所给事实不相符的是
A.硫酸铜溶液中加少量氨水:Cu2++2NH3·H2O=Cu(OH)2↓+2 |
B.氢气燃烧热为285.8kJ/mol:H2(g)+ O2(g)=H2O(l) ΔH=−285.8kJ/mol O2(g)=H2O(l) ΔH=−285.8kJ/mol |
| C.用KSCN溶液检验Fe3+:Fe3++3SCN−=Fe(SCN)3↓ |
| D.加热CuCl2溶液,溶液变成黄绿色:[Cu(H2O)4]2++4Cl−⇌[CuCl4]2−+4H2O ΔH>0 |
您最近一年使用:0次
名校
3 . 下列有关方程式错误的是
A. 燃烧热的热化学方程式: 燃烧热的热化学方程式: 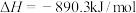 |
B.铅酸蓄电池充电时的阳极反应: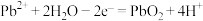 |
C. 沉淀转化为 沉淀转化为 沉淀: 沉淀: |
D.煅烧黄铁矿制 : : |
您最近一年使用:0次
2024-02-14更新
|
114次组卷
|
2卷引用:重庆市西南大学附中2023-2024学年高二上学期期末考试化学试题
名校
4 . 下列说法正确的是
| A.甲烷的燃烧热为890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g) =CO2(g)+2H2O(g) ΔH=−890.3 kJ/mol |
B.500℃、30MPa下将0.5mol N2和1.5mol H2置于密闭容器中充分反应生成NH3,放出19.3kJ热量,其热化学方程式为N2(g)+3H2(g) 2NH3(g) ΔH=−38.6 kJ/mol 2NH3(g) ΔH=−38.6 kJ/mol |
| C.HCl和NaOH反应的中和热为 ΔH=−57.3kJ/mol,则1 mol稀盐酸与1molNaOH反应放出的热量为−57.3kJ/mol |
| D.已知H2+Cl2 =2HCl 为放热反应,则1 mol H2与1molCl2 所具有的总键能小于2molHCl所具有的总键能 |
您最近一年使用:0次
5 . 已知碳、一氧化碳、晶体硅的燃烧热分别是△H1、△H2、△H3,则工业冶炼晶体硅的反应为
 。则下列判断错误的是
。则下列判断错误的是

 。则下列判断错误的是
。则下列判断错误的是A.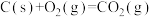  | B.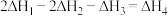 |
C.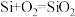  | D. |
您最近一年使用:0次
名校
6 . 标准状态下,下列微粒气态时的相对能量如下表:
依据表中数据,下列说法正确的是
| 物质(g) | O | H | 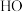 |  |  |  |  |  |
能量 | 249 | 218 | 39 | 0 | 0 | 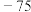 |  | 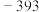 |
A. 的燃烧热 的燃烧热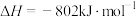 |
B.反应: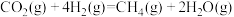 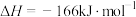 |
C. 的键能为 的键能为 |
D.已知: 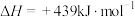 ,则 ,则 的键能是 的键能是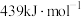 |
您最近一年使用:0次
名校
7 . 下列说法正确的是
A.甲烷的燃烧热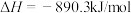 。则 。则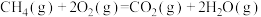 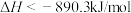 |
B.25℃ 时, 时,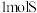 和 和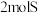 的燃烧热相等 的燃烧热相等 |
C.一定条件下,将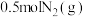 和 和 置于密闭的容器中充分反应生成 置于密闭的容器中充分反应生成 ,放热19.3kJ,热化学方程式为: ,放热19.3kJ,热化学方程式为: 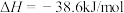 |
D.在稀溶液中: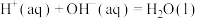 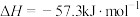 ,若将含 ,若将含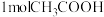 的醋酸稀溶液与含 的醋酸稀溶液与含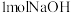 的稀溶液混合,放出的热量大于57.3kJ 的稀溶液混合,放出的热量大于57.3kJ |
您最近一年使用:0次
2023-12-04更新
|
136次组卷
|
4卷引用:重庆市育才中学校2022-2023学年高二上学期期末考试化学试题
名校
解题方法
8 . 化学反应中均伴随着能量的变化,回答下列问题:
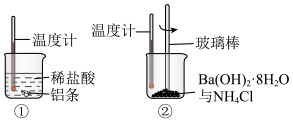
(1)某同学进行如下实验,图①和②中温度计示数降低的是_______ ;
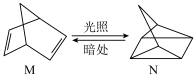
(2)有机物M可转化成N,转化过程如下,则M、N相比,较稳定的是_______ ;
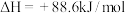
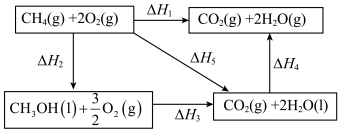
(3)已知 在一定条件下可发生如图的一系列反应,下列说法正确的是_______;
在一定条件下可发生如图的一系列反应,下列说法正确的是_______;
(4)金属Ni可活化 放出
放出 ,其反应历程如图所示:
,其反应历程如图所示:
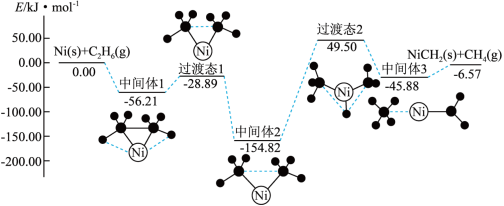
下列关于活化历程的说法正确的是_______。
(5) 与
与 经催化重整,制得合成气:
经催化重整,制得合成气: 已知上述反应中相关的化学键键能数据如下,则该反应的
已知上述反应中相关的化学键键能数据如下,则该反应的
_______ kJ/mol。
(6)在25℃、101kPa下,1g乙烷气体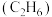 燃烧生成
燃烧生成 和液态水时放热QkJ,则表示乙烷燃烧热的热化学方程式为
和液态水时放热QkJ,则表示乙烷燃烧热的热化学方程式为_______ 。
(7)中和热的测定实验中,取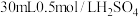 溶液与50mL0.5mol/LNaOH溶液进行中和反应,三次实验温度平均升高4℃,已知溶液的比热容近似为
溶液与50mL0.5mol/LNaOH溶液进行中和反应,三次实验温度平均升高4℃,已知溶液的比热容近似为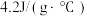 ,溶液的密度均近似为
,溶液的密度均近似为 。通过计算可得稀硫酸和稀NaOH溶液的中和热
。通过计算可得稀硫酸和稀NaOH溶液的中和热
_______ kJ/mol。
(1)某同学进行如下实验,图①和②中温度计示数降低的是

(2)有机物M可转化成N,转化过程如下,则M、N相比,较稳定的是

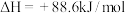
(3)已知
 在一定条件下可发生如图的一系列反应,下列说法正确的是_______;
在一定条件下可发生如图的一系列反应,下列说法正确的是_______;
A. | B.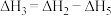 |
C. | D. |
(4)金属Ni可活化
 放出
放出 ,其反应历程如图所示:
,其反应历程如图所示:
下列关于活化历程的说法正确的是_______。
| A.中间体1→中间体2的过程是放热过程 |
| B.加入催化剂可降低该反应的反应热,加快反应速率 |
C.1molNi和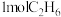 的总能量小于 的总能量小于 和 和 的总能量 的总能量 |
| D.中间体2→中间体3的过程是决速步骤 |
(5)
 与
与 经催化重整,制得合成气:
经催化重整,制得合成气: 已知上述反应中相关的化学键键能数据如下,则该反应的
已知上述反应中相关的化学键键能数据如下,则该反应的
| 化学键 |  |  |  | 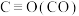 |
| 键能/(kJ/mol) | 413 | 745 | 436 | 1075 |
(6)在25℃、101kPa下,1g乙烷气体
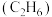 燃烧生成
燃烧生成 和液态水时放热QkJ,则表示乙烷燃烧热的热化学方程式为
和液态水时放热QkJ,则表示乙烷燃烧热的热化学方程式为(7)中和热的测定实验中,取
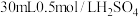 溶液与50mL0.5mol/LNaOH溶液进行中和反应,三次实验温度平均升高4℃,已知溶液的比热容近似为
溶液与50mL0.5mol/LNaOH溶液进行中和反应,三次实验温度平均升高4℃,已知溶液的比热容近似为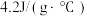 ,溶液的密度均近似为
,溶液的密度均近似为 。通过计算可得稀硫酸和稀NaOH溶液的中和热
。通过计算可得稀硫酸和稀NaOH溶液的中和热
您最近一年使用:0次
名校
解题方法
9 . 下列热化学相关的描述正确的是
A. 在光照和点燃条件下 在光照和点燃条件下 不同 不同 |
B.已知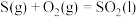  , ,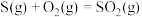  ,则 ,则 |
C.表示 的燃烧热: 的燃烧热: 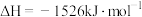 |
D.一定条件下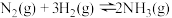 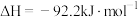 ,则 ,则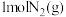 和 和  置于密闭容器中充分反应放热 置于密闭容器中充分反应放热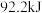 |
您最近一年使用:0次
2023-11-10更新
|
259次组卷
|
3卷引用:重庆市第八中学校2023-2024学年高二上学期期中考试化学试题
名校
解题方法
10 . 下列说法正确的是
A. 的燃烧热 的燃烧热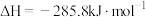 ,则 ,则  |
B.已知稀溶液中, 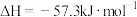 ,则稀醋酸与稀氢氧化钠溶液反应生成 ,则稀醋酸与稀氢氧化钠溶液反应生成 水时放出 水时放出 的热量 的热量 |
C.已知 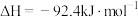 ,则在一定条件下将 ,则在一定条件下将 和 和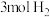 置于一密闭容器中充分反应,放出 置于一密闭容器中充分反应,放出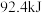 的热量 的热量 |
D.相同条件下,反应 在光照和点燃条件下的 在光照和点燃条件下的 不同 不同 |
您最近一年使用:0次



