名校
解题方法
1 . 下列各组热化学方程式中,化学反应的ΔH前者大于后者的有
①H2(g)+F2(g)=2HF(g) ΔH1 H2(g)+Cl2(g)=2HCl(g) ΔH2
②C8H8(l)+ O2(g)=8CO2(g)+9H2O(g) ΔH3 C8H8(g)+
O2(g)=8CO2(g)+9H2O(g) ΔH3 C8H8(g)+ O2(g)=8CO2(g)+9H2O(l) ΔH4
O2(g)=8CO2(g)+9H2O(l) ΔH4
③2N2(g)+6H2(g) 4NH3(g) ΔH5 N2(g)+3H2(g)
4NH3(g) ΔH5 N2(g)+3H2(g) 2NH3(g) ΔH6
2NH3(g) ΔH6
④CaCO3(s)=CaO(s)+CO2(g) ΔH7 CaO(s)+H2O(l)=Ca(OH)2(s) ΔH8
⑤NaOH(aq)+CH3COOH(aq)=CH3COONa(aq)+H2O(l) ΔH9 HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l) ΔH10
①H2(g)+F2(g)=2HF(g) ΔH1 H2(g)+Cl2(g)=2HCl(g) ΔH2
②C8H8(l)+
 O2(g)=8CO2(g)+9H2O(g) ΔH3 C8H8(g)+
O2(g)=8CO2(g)+9H2O(g) ΔH3 C8H8(g)+ O2(g)=8CO2(g)+9H2O(l) ΔH4
O2(g)=8CO2(g)+9H2O(l) ΔH4③2N2(g)+6H2(g)
 4NH3(g) ΔH5 N2(g)+3H2(g)
4NH3(g) ΔH5 N2(g)+3H2(g) 2NH3(g) ΔH6
2NH3(g) ΔH6④CaCO3(s)=CaO(s)+CO2(g) ΔH7 CaO(s)+H2O(l)=Ca(OH)2(s) ΔH8
⑤NaOH(aq)+CH3COOH(aq)=CH3COONa(aq)+H2O(l) ΔH9 HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l) ΔH10
| A.2项 | B.3项 | C.4项 | D.5项 |
您最近半年使用:0次
2 . ①H2O(l)=H2(g)+ O2(g) ΔH=+285.8kJ·mol-1
O2(g) ΔH=+285.8kJ·mol-1
②H2(g)+ O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
③C(s)+ O2(g)=CO(g) ΔH=-110.5kJ·mol-1
O2(g)=CO(g) ΔH=-110.5kJ·mol-1
④C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1
回答下列问题:
(1)上述反应中属于放热反应的是___________ 。(填序号)
(2)H2的燃烧热为___________ 。
(3)燃烧10gH2生成液态水,放出的热量为___________ 。
 O2(g) ΔH=+285.8kJ·mol-1
O2(g) ΔH=+285.8kJ·mol-1②H2(g)+
 O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8kJ·mol-1③C(s)+
 O2(g)=CO(g) ΔH=-110.5kJ·mol-1
O2(g)=CO(g) ΔH=-110.5kJ·mol-1④C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1
回答下列问题:
(1)上述反应中属于放热反应的是
(2)H2的燃烧热为
(3)燃烧10gH2生成液态水,放出的热量为
您最近半年使用:0次
3 . 已知: 、
、 、
、 的燃烧热分别为
的燃烧热分别为 、
、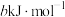 和
和 (a、b、c都大于0)。则反应
(a、b、c都大于0)。则反应 的
的 为
为
 、
、 、
、 的燃烧热分别为
的燃烧热分别为 、
、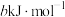 和
和 (a、b、c都大于0)。则反应
(a、b、c都大于0)。则反应 的
的 为
为A. | B.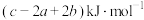 |
C.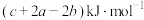 | D.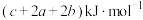 |
您最近半年使用:0次
名校
解题方法
4 . 下列化学反应的表示正确的是
A.尿素和 溶液在碱性条件下反应: 溶液在碱性条件下反应: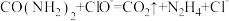 |
B.1-溴丙烷与氢氧化钠水溶液共热: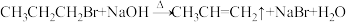 |
C.过量氨水和硫酸铜溶液反应: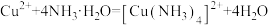 |
D.常温下 为液体,具有很高的燃烧热 为液体,具有很高的燃烧热 ,肼燃烧的热化学方程式: ,肼燃烧的热化学方程式: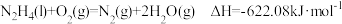 |
您最近半年使用:0次
解题方法
5 . 依据叙述,按要求填空
(1)在25℃、101kPa下,1g甲醇(CH3OH液态)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为___________ 。
(2)11.2L(标准状况)H2在足量Cl2中燃烧生成HCl气体,放出91.5kJ热量,其热化学方程式:___________ 。
(3)已知1molC(石墨,s)与适量H2O(g)反应生成CO(g)和H2(g),吸收131.3kJ热量,请写出该反应的热化学方程式:___________ 。
(4)甲醛(HCHO)俗称蚁醛,是一种重要的化工原料。可通过以下方法将甲醇转化为甲醛。
脱氢法:CH3OH(g)=HCHO(g)+H2(g) △H1=+92.09kJ/mol
氧化法:CH3OH(g)+ O2(g)=HCHOg+H2O(g) △H2
O2(g)=HCHOg+H2O(g) △H2
已知:2H2(g)+O2(g)=2H2O(g) △H3=-483.64kJ/mol,则△H2=___________ 。
(1)在25℃、101kPa下,1g甲醇(CH3OH液态)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为
(2)11.2L(标准状况)H2在足量Cl2中燃烧生成HCl气体,放出91.5kJ热量,其热化学方程式:
(3)已知1molC(石墨,s)与适量H2O(g)反应生成CO(g)和H2(g),吸收131.3kJ热量,请写出该反应的热化学方程式:
(4)甲醛(HCHO)俗称蚁醛,是一种重要的化工原料。可通过以下方法将甲醇转化为甲醛。
脱氢法:CH3OH(g)=HCHO(g)+H2(g) △H1=+92.09kJ/mol
氧化法:CH3OH(g)+
 O2(g)=HCHOg+H2O(g) △H2
O2(g)=HCHOg+H2O(g) △H2已知:2H2(g)+O2(g)=2H2O(g) △H3=-483.64kJ/mol,则△H2=
您最近半年使用:0次
解题方法
6 . 工业上,常用水蒸气通过炽热的焦炭制得水煤气(主要成分为 和
和 ),其反应的化学方程式为
),其反应的化学方程式为 ,请回答下列问题:
,请回答下列问题:
(1)上述反应的能量变化图像如图所示。下列反应的能量变化与上述反应相同的是___________。
(2)一定条件下,焦炭和水蒸气在体积一定的密闭容器中进行反应,下列有关说法正确的是___________ 。
A.充入He使容器压强增大,能提高反应速率
B.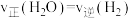 ,说明反应达到平衡状态
,说明反应达到平衡状态
C.容器中焦炭的质量不再变化,说明反应达到平衡状态
D.混合气体的密度不再发生改变时,反应达平衡状态
E.升高温度,能使正反应速率增大,逆反应速率减小
(3)298K时,1gH2燃烧生成H2O(g)放热121kJ,1molH2O(l)蒸发吸热44kJ,表示H2燃烧热的热化学方程式为___________ 。
(4)恒温下,将1molN2和3molH2置于体积为2L的密闭容器中进行反应N2+3H2⇌2NH3,若5min时测得氢气浓度为0.9mol/L,则用氨气表示5min内的化学反应速率为___________ ,N2的转化率为___________ ,欲提高合成氨的反应速率可采取的措施为___________ 。(任意答2点)
(5)工业制备硝酸过程中,通常对氨气进行催化氧化,其化学方程式为___________ 。
 和
和 ),其反应的化学方程式为
),其反应的化学方程式为 ,请回答下列问题:
,请回答下列问题:(1)上述反应的能量变化图像如图所示。下列反应的能量变化与上述反应相同的是___________。

| A.铝粉与氧化铁的反应 |
B.氯化铵与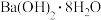 的反应 的反应 |
C.锌片与稀硫酸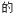 反应 反应 |
| D.钠与冷水的反应 |
(2)一定条件下,焦炭和水蒸气在体积一定的密闭容器中进行反应,下列有关说法正确的是
A.充入He使容器压强增大,能提高反应速率
B.
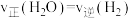 ,说明反应达到平衡状态
,说明反应达到平衡状态C.容器中焦炭的质量不再变化,说明反应达到平衡状态
D.混合气体的密度不再发生改变时,反应达平衡状态
E.升高温度,能使正反应速率增大,逆反应速率减小
(3)298K时,1gH2燃烧生成H2O(g)放热121kJ,1molH2O(l)蒸发吸热44kJ,表示H2燃烧热的热化学方程式为
(4)恒温下,将1molN2和3molH2置于体积为2L的密闭容器中进行反应N2+3H2⇌2NH3,若5min时测得氢气浓度为0.9mol/L,则用氨气表示5min内的化学反应速率为
(5)工业制备硝酸过程中,通常对氨气进行催化氧化,其化学方程式为
您最近半年使用:0次
名校
解题方法
7 . 25 ℃、101 kPa下,1g甲醇燃烧生成CO2和液态水时放热22.69 kJ,下列热化学方程式正确的是
| A.CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l) ΔH=726kJ·mol-1 |
| B.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1 452 kJ·mol-1 |
| C.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-726 kJ·mol-1 |
| D.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=1 452 kJ·mol-1 |
您最近半年使用:0次
8 . 填空
(1)硅是太阳能电池的重要材料。“精炼硅”反应历程中的能量变化如下图所示:_____ 。反应III为_____ (选填“吸热”或“放热”)反应。
(2)在25℃、101kpa下,1g甲烷燃烧生成CO2和液态水时放热22.68kJ。则表示甲烷燃烧的热化学方程式为_____ 。
(3)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为_____ 。
(1)硅是太阳能电池的重要材料。“精炼硅”反应历程中的能量变化如下图所示:
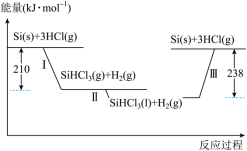
(2)在25℃、101kpa下,1g甲烷燃烧生成CO2和液态水时放热22.68kJ。则表示甲烷燃烧的热化学方程式为
(3)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
您最近半年使用:0次
名校
9 . 请回答下列问题:
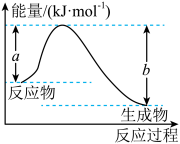
(1)如图表示某反应的能量变化关系,则此反应为___________ (填“吸热”或“放热”)反应,其中ΔH=___________ (用含有a、b的关系式表示)。___________ 114.6kJ(填“大于”、“等于”或“小于”)。
(3)在25℃,101kPa下,16g的N2H4(g)完全燃烧生成氮气和液态水时放热316kJ,则表示N2H4(g)燃烧热的热化学方程式为___________ 。
(4)甲醇(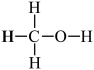 )既是重要的化工原料,又可作为燃料。利用水煤气(主要成分为CO和H2)在催化剂作用下合成甲醇,发生的反应为:CO(g)+2H2(g)
)既是重要的化工原料,又可作为燃料。利用水煤气(主要成分为CO和H2)在催化剂作用下合成甲醇,发生的反应为:CO(g)+2H2(g) CH3OH(g) ΔH。已知反应中相关的化学键键能数据如下:H-H键键能为436kJ/mol;C-O键键能为343kJ/mol;H-O键键能为463kJ/mol;H-C键键能为413kJ/mol;CO中的化学键键能为1071kJ/mol。计算该反应的ΔH=
CH3OH(g) ΔH。已知反应中相关的化学键键能数据如下:H-H键键能为436kJ/mol;C-O键键能为343kJ/mol;H-O键键能为463kJ/mol;H-C键键能为413kJ/mol;CO中的化学键键能为1071kJ/mol。计算该反应的ΔH=___________ 。
(1)如图表示某反应的能量变化关系,则此反应为
(3)在25℃,101kPa下,16g的N2H4(g)完全燃烧生成氮气和液态水时放热316kJ,则表示N2H4(g)燃烧热的热化学方程式为
(4)甲醇(
 )既是重要的化工原料,又可作为燃料。利用水煤气(主要成分为CO和H2)在催化剂作用下合成甲醇,发生的反应为:CO(g)+2H2(g)
)既是重要的化工原料,又可作为燃料。利用水煤气(主要成分为CO和H2)在催化剂作用下合成甲醇,发生的反应为:CO(g)+2H2(g) CH3OH(g) ΔH。已知反应中相关的化学键键能数据如下:H-H键键能为436kJ/mol;C-O键键能为343kJ/mol;H-O键键能为463kJ/mol;H-C键键能为413kJ/mol;CO中的化学键键能为1071kJ/mol。计算该反应的ΔH=
CH3OH(g) ΔH。已知反应中相关的化学键键能数据如下:H-H键键能为436kJ/mol;C-O键键能为343kJ/mol;H-O键键能为463kJ/mol;H-C键键能为413kJ/mol;CO中的化学键键能为1071kJ/mol。计算该反应的ΔH=
您最近半年使用:0次
名校
解题方法
10 . 下列说法正确的是
| A.已知:H-H键、H-N键和N≡N键的键焓ΔH分别为436kJ·mol﹣1、391kJ·mol﹣1和946kJ·mol﹣1,则N2(g)+3H2(g)=2NH3(g) ΔH=﹣92kJ·mol﹣1 |
| B.已知:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=﹣802.3kJ/mol,则甲烷的燃烧热为802.3kJ/mol |
| C.已知:4P(红磷,s)=P4(白磷,s) ΔH>0,则相同条件下,白磷比红磷稳定 |
D.已知:H+(aq)+OH﹣(aq)=H2O(l) ΔH=﹣57.3kJ mol﹣1,则H2SO4和Ba(OH)2反应:H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l) ΔH=﹣114.6kJ mol﹣1,则H2SO4和Ba(OH)2反应:H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l) ΔH=﹣114.6kJ mol﹣1 mol﹣1 |
您最近半年使用:0次



