1 . 下列化学反应的表示正确的是
A.尿素和NaClO溶液在碱性条件下反应: |
B.过量氨水和硫酸铜溶液反应: |
C.1-溴丙烷与氢氧化钠水溶液共热: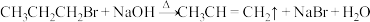 |
D.常温下N2H4为液体,具有很高的燃烧热(622.08 kJ⋅mol-1),肼燃烧的热化学方程式: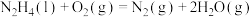 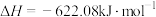 |
您最近一年使用:0次
2 . 下列表示相应化学反应的方程式正确的是
A.表示铅酸蓄电池充电时的阴极反应式: |
B.表示丙烷燃烧热的热化学方程式: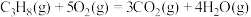 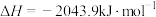 |
C.表示乙醇被酸性重铬酸钾溶液氧化的离子方程式: |
D.表示合成锦纶66的有机反应式:nH2N(CH2)6NH2+nHOOC(CH2)4COOH 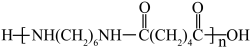 +(2n-1)H2O +(2n-1)H2O |
您最近一年使用:0次
解题方法
3 . 下列关于热化学反应的描述,正确的是
A.含 的稀溶液与足量的稀盐酸反应,放出 的稀溶液与足量的稀盐酸反应,放出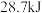 的热量表示该反应的热化学方程式是 的热量表示该反应的热化学方程式是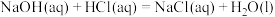  |
B.燃料电池中将甲醇蒸气转化为水蒸气的热化学方程式是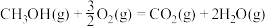 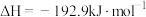 ,则 ,则 的燃烧热为 的燃烧热为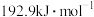 |
C.已知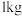 金属铍完全燃烧放出的热量为 金属铍完全燃烧放出的热量为 。则铍燃烧的热化学方程式为 。则铍燃烧的热化学方程式为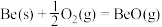 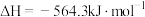 |
D.葡萄糖的燃烧热是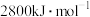 ,则 ,则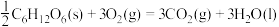 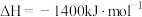 |
您最近一年使用:0次
名校
4 . 各相关物质的燃烧热数据如下表。下列热化学方程式正确的是
| 物质 | 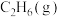 |  |  |
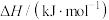 | 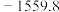 | 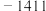 |  |
A.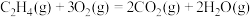 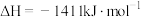 |
B.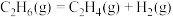 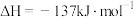 |
C.2H2O(l)=2H2(g)+O2(g) 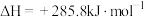 |
D.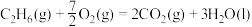  |
您最近一年使用:0次
解题方法
5 . 已知:①2H2(g)+O2(g) =2H2O(l),ΔH1=-572 kJ·mol-1
②2H2O2(l) = 2H2O(l)+O2(g),ΔH2=-196 kJ·mol-1
1.请写出生产H2O2总反应的热化学方程式___________ 。
2.反应①中的ΔH1___________ (选填: A.是 B.否)为H2的燃烧热,原因为___________ 。
3.H2O2沸点为150.2℃,受热容易分解。某试剂厂欲将7%的过氧化氢溶液浓缩成30%的溶液,以下方法中可以采用的是___________。
②2H2O2(l) = 2H2O(l)+O2(g),ΔH2=-196 kJ·mol-1
1.请写出生产H2O2总反应的热化学方程式
2.反应①中的ΔH1
3.H2O2沸点为150.2℃,受热容易分解。某试剂厂欲将7%的过氧化氢溶液浓缩成30%的溶液,以下方法中可以采用的是___________。
| A.常压蒸馏 | B.减压蒸馏 | C.加热蒸发 | D.加氧化钙除水 |
您最近一年使用:0次
6 . 下列化学反应与方程式不相符的是
A.甲烷的燃烧热为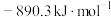 : :   |
B.向血红色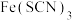 溶液中加入过量铁粉至溶液浅绿色: 溶液中加入过量铁粉至溶液浅绿色: |
C.碱性锌锰电池的正极反应: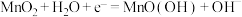 |
D.阿司匹林的制备: |
您最近一年使用:0次
解题方法
7 . 研发二氧化碳利用技术,降低空气中二氧化碳含量是当今研究热点。
(1)已知常温常压下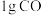 的燃烧放热
的燃烧放热 ,请写出表示
,请写出表示 燃烧热的热化学方程式
燃烧热的热化学方程式___________ 。
(2)1雨水中含有来自大气的 ,溶于水中的
,溶于水中的 进一步和水反应,发生电离:
进一步和水反应,发生电离:
①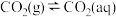 ②
②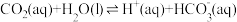
 时,反应②的平衡常数为K,溶液中
时,反应②的平衡常数为K,溶液中 的浓度与其在空气中的分压成正比(分压=总压×物质的量分数),比例系数为
的浓度与其在空气中的分压成正比(分压=总压×物质的量分数),比例系数为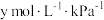 ,当大气压强为
,当大气压强为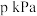 ,大气中
,大气中 的物质的量分数为x时,溶液中
的物质的量分数为x时,溶液中 浓度为
浓度为___________  (用题中的字母表示,忽略
(用题中的字母表示,忽略 的电离)。
的电离)。
(3)目前 和
和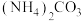 已经被用作工业捕碳剂,它们与
已经被用作工业捕碳剂,它们与 可发生如下反应:
可发生如下反应:
反应I: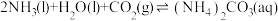
反应Ⅱ:
为研究温度对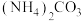 捕获
捕获 效率的影响,在某温度
效率的影响,在某温度 下,将一定量的
下,将一定量的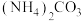 溶液置于密闭容器中,并充入一定量的
溶液置于密闭容器中,并充入一定量的 气体(用氨气作为稀释剂),在t时刻,测得容器中
气体(用氨气作为稀释剂),在t时刻,测得容器中 气体的浓度。然后分别在温度为
气体的浓度。然后分别在温度为 下,保持其它初始实验条件不变,重复上述实验,经过相同时间测得
下,保持其它初始实验条件不变,重复上述实验,经过相同时间测得 气体浓度,得到趋势图(见图1)。则:
气体浓度,得到趋势图(见图1)。则:
 气体浓度呈现如图1所示的变化趋势的原因
气体浓度呈现如图1所示的变化趋势的原因___________ 。
②反应Ⅱ在温度为 时,溶液
时,溶液 随时间变化的趋势曲线如图2所示,当时间达到
随时间变化的趋势曲线如图2所示,当时间达到 时,将该体系升温至
时,将该体系升温至 ,请在图2中画出
,请在图2中画出 时刻至平衡时,溶液的
时刻至平衡时,溶液的 变化总趋势曲线
变化总趋势曲线___________ 。
(4)研究表明, 气体可被电还原。在电解质水溶液中,三种不同催化剂(a、b、c)上
气体可被电还原。在电解质水溶液中,三种不同催化剂(a、b、c)上 电还原为
电还原为 的反应进程中(
的反应进程中( 被还原为
被还原为 的反应可同时发生),相对能量变化如图。
的反应可同时发生),相对能量变化如图。
(1)已知常温常压下
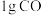 的燃烧放热
的燃烧放热 ,请写出表示
,请写出表示 燃烧热的热化学方程式
燃烧热的热化学方程式(2)1雨水中含有来自大气的
 ,溶于水中的
,溶于水中的 进一步和水反应,发生电离:
进一步和水反应,发生电离:①
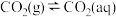 ②
②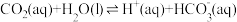
 时,反应②的平衡常数为K,溶液中
时,反应②的平衡常数为K,溶液中 的浓度与其在空气中的分压成正比(分压=总压×物质的量分数),比例系数为
的浓度与其在空气中的分压成正比(分压=总压×物质的量分数),比例系数为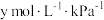 ,当大气压强为
,当大气压强为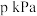 ,大气中
,大气中 的物质的量分数为x时,溶液中
的物质的量分数为x时,溶液中 浓度为
浓度为 (用题中的字母表示,忽略
(用题中的字母表示,忽略 的电离)。
的电离)。(3)目前
 和
和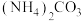 已经被用作工业捕碳剂,它们与
已经被用作工业捕碳剂,它们与 可发生如下反应:
可发生如下反应:反应I:
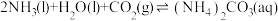
反应Ⅱ:

为研究温度对
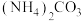 捕获
捕获 效率的影响,在某温度
效率的影响,在某温度 下,将一定量的
下,将一定量的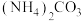 溶液置于密闭容器中,并充入一定量的
溶液置于密闭容器中,并充入一定量的 气体(用氨气作为稀释剂),在t时刻,测得容器中
气体(用氨气作为稀释剂),在t时刻,测得容器中 气体的浓度。然后分别在温度为
气体的浓度。然后分别在温度为 下,保持其它初始实验条件不变,重复上述实验,经过相同时间测得
下,保持其它初始实验条件不变,重复上述实验,经过相同时间测得 气体浓度,得到趋势图(见图1)。则:
气体浓度,得到趋势图(见图1)。则: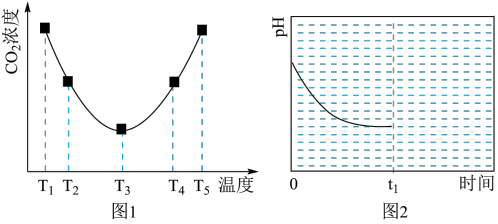
 气体浓度呈现如图1所示的变化趋势的原因
气体浓度呈现如图1所示的变化趋势的原因②反应Ⅱ在温度为
 时,溶液
时,溶液 随时间变化的趋势曲线如图2所示,当时间达到
随时间变化的趋势曲线如图2所示,当时间达到 时,将该体系升温至
时,将该体系升温至 ,请在图2中画出
,请在图2中画出 时刻至平衡时,溶液的
时刻至平衡时,溶液的 变化总趋势曲线
变化总趋势曲线(4)研究表明,
 气体可被电还原。在电解质水溶液中,三种不同催化剂(a、b、c)上
气体可被电还原。在电解质水溶液中,三种不同催化剂(a、b、c)上 电还原为
电还原为 的反应进程中(
的反应进程中( 被还原为
被还原为 的反应可同时发生),相对能量变化如图。
的反应可同时发生),相对能量变化如图。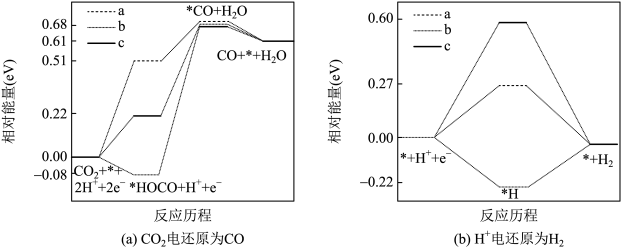
A.电解质水溶液的酸性越强,越有利于 气体电化学还原 气体电化学还原 |
B.a催化剂条件下, 电还原的活化能约为 电还原的活化能约为 |
C.c催化剂条件下, 电还原的活化能小于 电还原的活化能小于 电还原的活化能,更容易发生 电还原的活化能,更容易发生 的电还原 的电还原 |
D. 电还原为 电还原为 从易到难的顺序为c、a、b 从易到难的顺序为c、a、b |
您最近一年使用:0次
解题方法
8 . 联氨(N2H4)在常温下为无色液体,可用作火箭燃料。已知反应:
①2O2(g)+N2(g)=N2O4(l) △H1
②N2(g)+2H2(g)=N2H4(l) △H2
③O2(g)+2H2(g)=2H2O(g) △H3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) △H4=-1048.9kJ•mol-1
下列说法不正确 的是
①2O2(g)+N2(g)=N2O4(l) △H1
②N2(g)+2H2(g)=N2H4(l) △H2
③O2(g)+2H2(g)=2H2O(g) △H3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) △H4=-1048.9kJ•mol-1
下列说法
| A.O2(g)+2H2(g)=2H2O(l) △H5,△H5>△H3 |
| B.△H2不可表示N2的燃烧热 |
| C.1molO2(g)和2molH2(g)具有的总能量高于2molH2O(g)具有的总能量 |
| D.联氨和N2O4作火箭推进剂的原因之一是反应放出大量的热 |
您最近一年使用:0次
名校
解题方法
9 . 目前,处理烟气中 常采用两种方法:碱液吸收法和还原法。
常采用两种方法:碱液吸收法和还原法。
I.碱液吸收法
已知常温下:
第一步:用过量的浓氨水吸收 ,并在空气中氧化;
,并在空气中氧化;
第二步:加入石灰水,发生反应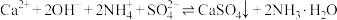 K。
K。
(1)25℃时,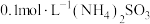 溶液的pH
溶液的pH___________ 7(填“>”“<”或“=”),并说明理由:___________ 。在该溶液中: ___________
___________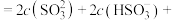 ___________。
___________。___________
(2)0.1mol/L下列溶液中,溶液中 由大到小的顺序是
由大到小的顺序是___________ 。
① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥
(3)第一步氧化的目的是将硫元素全部转化为 ,该过程中溶液pH
,该过程中溶液pH___________ (填“升高”“不变”或“降低”)。
(4)计算第二步中反应的K=___________ 。
(5)测定一定浓度的 溶液pH与温度的关系曲线如图所示,下列分析错误的是___________。
溶液pH与温度的关系曲线如图所示,下列分析错误的是___________。
(6)用过量的 溶液吸收
溶液吸收 的离子方程式:
的离子方程式:___________ 。
Ⅱ.水煤气还原法
已知:①
 ;
;
②
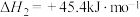 ;
;
③CO的燃烧热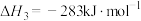 。
。
(7)表示液态硫的燃烧热的热化学方程式为___________ 。
(8)反应②中,正反应活化能
___________ (填“>”“<”或“=”) 。
。
(9)在一定压强下,发生反应①。平衡时 的转化率
的转化率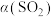 与投料比的比值
与投料比的比值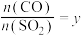 、温度T的关系如图所示。比较平衡时CO的转化率
、温度T的关系如图所示。比较平衡时CO的转化率 :N
:N___________ M(填“>”“<”或“=”,下同)。逆反应速率N___________ P。 、2molCO和
、2molCO和 发生反应①、②,第5min时达到平衡,测得混合气体中
发生反应①、②,第5min时达到平衡,测得混合气体中 、
、 的物质的量分别为1.6mol、1.8mol。
的物质的量分别为1.6mol、1.8mol。
①该温度下,反应②的平衡常数K为___________ 。(填数值)
②其他条件不变,在第7min时缩小容器体积,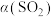
___________ (填“增大”“减小”或“不变”)。
 常采用两种方法:碱液吸收法和还原法。
常采用两种方法:碱液吸收法和还原法。I.碱液吸收法
已知常温下:
 |  |  |  |
 | 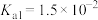  |  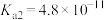 | 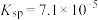 |
 ,并在空气中氧化;
,并在空气中氧化;第二步:加入石灰水,发生反应
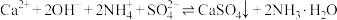 K。
K。(1)25℃时,
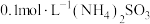 溶液的pH
溶液的pH ___________
___________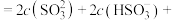 ___________。
___________。(2)0.1mol/L下列溶液中,溶液中
 由大到小的顺序是
由大到小的顺序是①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥
(3)第一步氧化的目的是将硫元素全部转化为
 ,该过程中溶液pH
,该过程中溶液pH(4)计算第二步中反应的K=
(5)测定一定浓度的
 溶液pH与温度的关系曲线如图所示,下列分析错误的是___________。
溶液pH与温度的关系曲线如图所示,下列分析错误的是___________。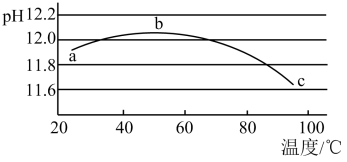
| A.c点水解程度最大 | B.水解是吸热过程 |
| C.a→b段水解平衡向右移动 | D.b点溶液中的 最大 最大 |
(6)用过量的
 溶液吸收
溶液吸收 的离子方程式:
的离子方程式:Ⅱ.水煤气还原法
已知:①

 ;
;②

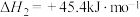 ;
;③CO的燃烧热
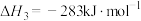 。
。(7)表示液态硫的燃烧热的热化学方程式为
(8)反应②中,正反应活化能

 。
。(9)在一定压强下,发生反应①。平衡时
 的转化率
的转化率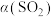 与投料比的比值
与投料比的比值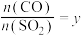 、温度T的关系如图所示。比较平衡时CO的转化率
、温度T的关系如图所示。比较平衡时CO的转化率 :N
:N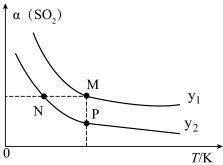
 、2molCO和
、2molCO和 发生反应①、②,第5min时达到平衡,测得混合气体中
发生反应①、②,第5min时达到平衡,测得混合气体中 、
、 的物质的量分别为1.6mol、1.8mol。
的物质的量分别为1.6mol、1.8mol。①该温度下,反应②的平衡常数K为
②其他条件不变,在第7min时缩小容器体积,
您最近一年使用:0次
解题方法
10 . 下列表达式书写不正确的是
A. 的水解方程式: 的水解方程式: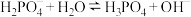 |
B.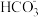 的电离方程式: 的电离方程式: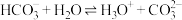 |
C.CaCO3的沉淀溶解平衡表达式: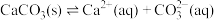 |
D.表示H2燃烧热的热化学方程式:2H2(g)+O2(g)=2H2O(l)  kJ⋅mol kJ⋅mol |
您最近一年使用:0次



