名校
解题方法
1 . 已知:2H2O(l)=2H2(g)+O2(g) ΔH=+571.0 kJ/mol。以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制H2的过程如下:
过程Ⅰ:2Fe3O4(s)=6FeO(s)+O2(g) ΔH=+313.2 kJ/mol
过程Ⅱ:…
过程Ⅰ:2Fe3O4(s)=6FeO(s)+O2(g) ΔH=+313.2 kJ/mol
过程Ⅱ:…
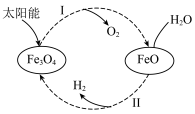
| A.过程Ⅰ中每消耗232 g Fe3O4转移2 mol电子 |
| B.过程Ⅱ的热化学方程式为3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=+128.9 kJ/mol |
| C.过程Ⅰ、Ⅱ中能量转化的形式依次是太阳能→化学能→热能 |
| D.铁氧化合物循环制H2具有成本低、产物易分离等优点 |
您最近一年使用:0次
2023-09-19更新
|
355次组卷
|
25卷引用:甘肃省天水市甘谷第一中学2019-2020学年高二下学期开学考试化学试题
甘肃省天水市甘谷第一中学2019-2020学年高二下学期开学考试化学试题【区级联考】北京市石景山区2019届高三第一学期期末考试化学试题辽宁省锦州市滨海实验中学2019-2020学年高三上学期期末考试化学试题海南省海南中学2019-2020学年高二上学期期末考试化学试题(已下线)《2020年新高考政策解读与配套资源》模拟试题10-2020年北京新高考化学模拟试题(已下线)专题九 化学能与热能(提分特训)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训鲁科版(2019)选择性必修1第1章 化学反应与能量转化 第1节综合训练高中必刷题高二选择性必修1第一章 化学反应的热效应 第二节 反应热的计算 第二节综合训练河北省沧州市泊头市第一中学2020-2021学年高二上学期第一次月考化学试题山东省德州市夏津第一中学2020-2021学年高二上学期9月月考化学试题辽源市第五中学2019-2020学年高一下学期第二次月考化学试题湖南省中方一中2020-2021学年高二上学期期中考试化学试题河北省沧州市黄骅中学2020-2021学年高二上学期第三次月考化学试题河南省鹤壁市高级中学2020-2021学年高二上学期尖子生联赛调研二化学试题河北省安平中学2020-2021学年高一下学期第四次月考(期末)化学试题(已下线)模块七 化学反应与能量(模块检测)-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第一单元培优练-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)贵州省黔西南州赛文高级中学 2021-2022学年高二上学期期中考试化学试题河北省沧州市泊头市第一中学2021-2022学年高二上学期第一次月考化学试题天津市第二中学2022-2023学年高二上学期期中检测化学试题(已下线)第七章 化学反应速率与化学平衡 热点强化12 化学反应历程、机理的分析应用(已下线)题型98 结合反应能量图示或物质循环图示书写热化学方程式山东省烟台市招远第一中学2022-2023学年高一下学期期中考试化学(等级考)试题(已下线)章末综合评价(六)河南省洛阳市宜阳县第一高级中学清北园2023-2024学年高一上学期第七次能力达标测试化学试卷
名校
解题方法
2 . 我国提出争取在2030年前实现碳达峰,2060年前实现碳中和。 的相关转化对解决环境问题、能源问题等有重要的意义。
的相关转化对解决环境问题、能源问题等有重要的意义。
Ⅰ.已知:①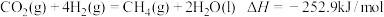
②
(1)

_______  。
。
Ⅱ.目前工业上有一种方法可以利用 生产燃料甲醇,发生的反应为:
生产燃料甲醇,发生的反应为: 。在800℃时,向体积为1L的密闭容器中,充入
。在800℃时,向体积为1L的密闭容器中,充入 和
和 ,测得
,测得 和
和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。 的平均反应速率为
的平均反应速率为_______  。
。
(3)反应达到平衡时,该反应的平衡常数
_______ ; 的转化率为
的转化率为_______ 。
(4)若在上述平衡体系中再充入 和
和 (保持温度不变),则此平衡将
(保持温度不变),则此平衡将_______ 移动(填“向正反应方向”、“不”、“向逆反应方向”)。
(5)若将温度升高到1000℃,测得反应平衡常数为1,则该反应的
_______ 0(填“>”或“<”)。
 的相关转化对解决环境问题、能源问题等有重要的意义。
的相关转化对解决环境问题、能源问题等有重要的意义。Ⅰ.已知:①
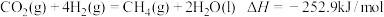
②

(1)


 。
。Ⅱ.目前工业上有一种方法可以利用
 生产燃料甲醇,发生的反应为:
生产燃料甲醇,发生的反应为: 。在800℃时,向体积为1L的密闭容器中,充入
。在800℃时,向体积为1L的密闭容器中,充入 和
和 ,测得
,测得 和
和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。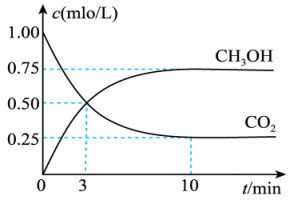
 的平均反应速率为
的平均反应速率为 。
。(3)反应达到平衡时,该反应的平衡常数

 的转化率为
的转化率为(4)若在上述平衡体系中再充入
 和
和 (保持温度不变),则此平衡将
(保持温度不变),则此平衡将(5)若将温度升高到1000℃,测得反应平衡常数为1,则该反应的

您最近一年使用:0次
2023-02-01更新
|
217次组卷
|
2卷引用:甘肃省白银市靖远县第四中学2023-2024学年高二下学期开学化学试题
3 . 已知: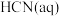 与
与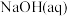 反应的
反应的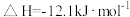 ;
;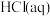 与
与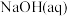 反应的
反应的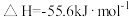 。则
。则 在水溶液中电离的
在水溶液中电离的 等于
等于
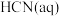 与
与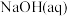 反应的
反应的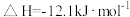 ;
;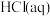 与
与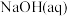 反应的
反应的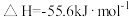 。则
。则 在水溶液中电离的
在水溶液中电离的 等于
等于A.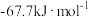 | B. |
C.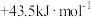 | D.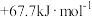 |
您最近一年使用:0次
2016-12-09更新
|
1943次组卷
|
72卷引用:甘肃省民勤县第一中学2020-2021学年高二下学期(理)开学考试化学试题
甘肃省民勤县第一中学2020-2021学年高二下学期(理)开学考试化学试题(已下线)2014-2015学年甘肃省兰州一中高二上学期期中考试化学卷山东省济南市历城第二中学2017-2018学年高二下学期开学考试化学试题福建省龙岩第一中学2021-2022学年高二上学期开学考试化学试题2010年普通高等学校招生全国统一考试理综化学部分(新课标全国I卷)2010年普通高等学校招生全国统一考试(课标Ⅰ卷)理综化学部分全解全析2010年普通高等学校招生全国统一考试(湖南卷)理综化学部分全解全析2010年高考化学试题分项专题七 化学反应中的能量变化(已下线)2010年长春外国语学校高二第一学期期末考试化学试卷(已下线)2012届贵州省遵义四中高三第一次月考理科综合试卷(化学部分)(已下线)2011-2012学年湖北省荆州中学高二上学期期中考试化学试卷(已下线)2011—2012学年黑龙江哈九中度高二上学期期中考试化学试卷(已下线)2012届山东省济宁一中高三上学期第二次定时练习化学试卷(已下线)2011-2012学年吉林省长春市十一高中高一下学期期末考试化学试卷(已下线)2013-2014广东汕头市金山中学第一学期期末高二化学试卷(已下线)2013-2014黑龙江省大庆铁人中学高一下学期期末考试化学试卷(已下线)2013-2014学年辽宁省抚顺市六校联合体高一下学期期末考试化学试卷(已下线)2015届安徽省黄山市徽州一中高三第一次月考化学试卷(已下线)2014秋湖北省武汉市部分重点中学高二上学期期中联考化学试卷2014-2015陕西省西安市庆安高级中学高二上学期期末化学试卷2014-2015陕西省西安市一中高二上学期期末化学试卷2014-2015陕西省西安市七十中高二上学期期末考试化学试卷2015-2016学年河北省行唐启明中学高二上学期第一次月考化学试卷2015-2016学年湖南省浏阳、攸县一中高二上期中联考化学试卷2016届河北省枣强中学高三上学期期中测试化学试卷2015-2016学年江西省丰城中学高二上学期期中考试化学试卷2015-2016学年广西宾阳县宾阳中学高二5月月考化学试卷2016-2017学年青海师大附中高二上期中化学试卷河南省中原名校(即豫南九校)2017-2018学年高二上学期第一次联考化学试题河南省八市2017-2018学年高二上学期第一次质量检测化学试题山西省大同市第一中学2017-2018学年高二上学期期中考试化学试题内蒙古巴彦淖尔市第一中学2017-2018学年高二上学期期中考试(A卷)化学试题高中化学人教版 选修四 第一章 化学反应与能量 第三节 化学反应热的计算 化学反应热的计算第二课时(反应热的计算)四川省南充高级中学2017-2018学年高二12月月考化学试题安徽省淮北市第一中学2017-2018学年高二下学期第一次月考化学试题1人教版高二化学选修四专题:化学反应热的计算同步练习卷【全国百强校】安徽省铜陵市第一中学2018-2019学年高二上学期10月月考化学试题【全国百强校】河南省信阳市高级中学2018-2019学年高二上学期10月月考化学试题2【校级联考】湖北省孝感市七校教学联盟2018-2019学年高二上学期期中联合考试化学试题河南省上蔡县第二高级中学2018-2019学年高二上学期期中考试化学试题福建省晋江市南侨中学2018-2019学年高二下学期第二次月考化学试题河北安平中学2018-2019学年高二下学期期末考试化学试题(已下线)2019年9月1日《每日一题》人教选修4—— 每周一测浙江省宁波诺丁汉大学附属中学2017-2018学年高二上学期期中考试化学试题云南省保山市第一中学2018-2019学年高二下学期期末化学试题福建省晋江市南侨中学2019-2020学年高二上学期第一阶段考试化学试题宁夏吴忠中学2019-2020学年高二上学期期中考试化学试题2020届高三化学选修4二轮专题练——盖斯定律的应用【选择精编25题】2020届高三化学知识点强化训练—盖斯定律河北省沧州市泊头市第一中学2019-2020学年高二月考检测化学试题四川省雅安市2019-2020学年高二上学期期末检测化学试题河北省泊头市第一中学2019-2020学年高二上学期期末模拟考试化学试卷陕西省榆林市绥德县绥德中学2019-2020高二下学期第一次阶段性测试化学试题河南省驻马店市2018-2019学年高二上学期期末考试化学试题吉林省白城市洮南市第一中学2020-2021学年高二上学期第一次月考化学试题河北省保定市唐县第一中学2020-2021学年高二9月月考化学试题(已下线)【全国百强校】广西桂林市第十八中学2018-2019学年高二下学期期中段考化学试题陕西省汉中市洋县中学2018-2019学年高二上学期第一次月考化学试题河南省豫北名校2020-2021学年高二上学期11月质量检测化学试题江苏省南京市第十二中学2020-2021学年高二上学期第一次学情调研测试化学试题广西南宁市上林县中学2020-2021学年高二上学期期末考试化学试题江苏省海安市实验中学2021-2022学年高二上学期第一次月考化学试题广西浦北中学2021-2022学年高二上学期第一次月考化学试题黑龙江省八校2022届高三上学期期中联合考试化学试题(已下线)必考点01 化学反应的热效应-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)重庆市第七中学校2021-2022学年高二上学期期中考试化学试题福建省龙岩第一中学2022-2023学年高二上学期第一次月考(普通班)化学试题山东省青岛第二中学2019-2020学年高二上学期期中考试化学试题四川省乐山沫若中学2022-2023学年高二上学期第二次月考(期中考试)化学试题天津市第二中学2022-2023学年高二上学期期中检测化学试题安徽省安庆二中2022-2023学年高一下学期5月月考化学试题安徽省合肥市肥东县综合高中2022-2023学年高二上学期11月期中考试化学试题



