解题方法
1 . 氢气在氧气中燃烧主要经历以下四步基元反应:
①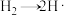 (慢反应)
(慢反应)
②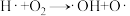 (快反应)
(快反应)
③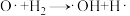 (快反应)
(快反应)
④ (快反应)
(快反应)
下列说法正确的是
①
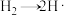 (慢反应)
(慢反应)②
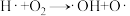 (快反应)
(快反应)③
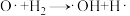 (快反应)
(快反应)④
 (快反应)
(快反应)下列说法正确的是
A. 的电子式是 的电子式是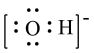 |
| B.在这四步反应中,第①步反应的活化能最高 |
C.第②步反应中 与 与 的每一次碰撞都为有效碰撞 的每一次碰撞都为有效碰撞 |
D. 和 和 是反应的中间产物,能在体系中稳定存在 是反应的中间产物,能在体系中稳定存在 |
您最近一年使用:0次
2022-01-19更新
|
389次组卷
|
2卷引用:辽宁省辽东南协作校2023-2024学年高二上学期10月月考化学试题
2 . 1,3-丁二烯(CH2=CH-CH=CH2)与HBr发生1,2-加成反应分两步进行:第一步H+进攻1,3-丁二烯生成碳正离子(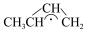 );第二步Br-进攻碳正离子完成1,2-加成反应,反应过程中的能量变化如下图所示。下列说法正确的是
);第二步Br-进攻碳正离子完成1,2-加成反应,反应过程中的能量变化如下图所示。下列说法正确的是
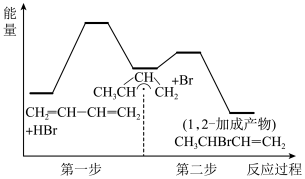
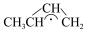 );第二步Br-进攻碳正离子完成1,2-加成反应,反应过程中的能量变化如下图所示。下列说法正确的是
);第二步Br-进攻碳正离子完成1,2-加成反应,反应过程中的能量变化如下图所示。下列说法正确的是
| A.两步均为放热反应 |
| B.该总反应为吸热反应 |
| C.第一步反应速率小于第二步反应速率 |
| D.加入催化剂可以改变该反应的反应热 |
您最近一年使用:0次
名校
3 . 某工业生产中发生反应: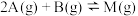
 。下列有关该工业生产的说法正确的是
。下列有关该工业生产的说法正确的是
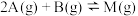
 。下列有关该工业生产的说法正确的是
。下列有关该工业生产的说法正确的是| A.工业上合成M时,一定采用高压条件,因为高压有利于M的生成 |
| B.若物质B廉价易得,工业上一般采用加入过量的B的方式来提高A和B的转化率 |
| C.工业上一般采用较高温度合成M,因温度越高,反应物的转化率越高 |
| D.工业生产中使用催化剂可提高M的日产量 |
您最近一年使用:0次
2022-09-04更新
|
297次组卷
|
10卷引用:辽宁省联合校2020-2021学年高二上学期第一次月考化学试题
辽宁省联合校2020-2021学年高二上学期第一次月考化学试题辽宁省实验中学东戴河分校2020-2021学年高二10月月考化学试题吉林省白城市第一中学2021-2022学年高二上学期9月阶段考试化学试题吉林省长春市十一高中2021-2022学年高二上学期第一学程考试化学试题第四节 化学反应的调控(已下线)【知识图鉴】单元讲练测选择性必修1第2单元01讲核心第二章 第四节 化学反应的调控(已下线)专题06 化学反应的方向及调控【考点清单】(讲+练)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)内蒙古赤峰实验中学2023-2024学年高二下学期开学化学试题(已下线)第04讲 化学反应的方向、化学反应的调控(讲义)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
名校
4 . 环状碳酸酯广泛用于极性非质子溶剂、电池的电解质等,离子液体研究团队近期报道了一种环氧乙烷衍生物与二氧化碳催化合成环状碳酸酯的反应历程如图所示。已知:R表示烃基。下列说法错误的是
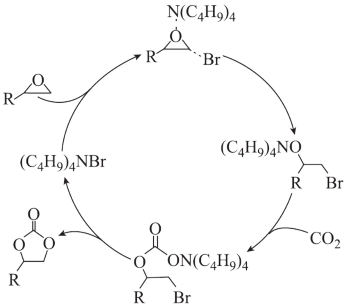

| A.(C4H9)4NBr是反应的催化剂 |
| B.反应过程存在极性键的断裂和形成 |
| C.反应过程中有4种中间体 |
| D.使用催化剂可以改变反应路径,降低反应活化能,加快反应速率 |
您最近一年使用:0次
名校
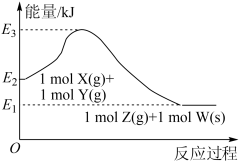
5 . X(g)+Y(g) Z(g)+W(s)反应过程中能量变化如图,下列说法正确的是
Z(g)+W(s)反应过程中能量变化如图,下列说法正确的是
 Z(g)+W(s)反应过程中能量变化如图,下列说法正确的是
Z(g)+W(s)反应过程中能量变化如图,下列说法正确的是
| A.该反应正反应的活化能小于逆反应的活化能 |
| B.该反应的△H=(E2-E1)kJ·mol-1 |
| C.若加入催化剂,(E3-E2)的值不变 |
| D.高温下有利于该反应正向进行 |
您最近一年使用:0次
名校
解题方法
6 . 如图所示为CFCl3破坏臭氧层的过程,下列说法不正确的是
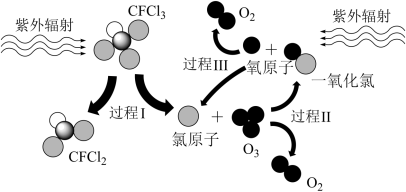
| A.过程Ⅰ中断裂C—Cl键 | B.过程Ⅱ可表示为O3+Cl=ClO+O2 |
| C.过程Ⅲ中O+O=O2是吸热过程 | D.上述过程说明CFCl3中的氯原子是破坏臭氧层的催化剂 |
您最近一年使用:0次
2023-09-13更新
|
283次组卷
|
63卷引用:辽宁省葫芦岛市第八高级中学2021–2022学年高二上学期期中考试化学试题
辽宁省葫芦岛市第八高级中学2021–2022学年高二上学期期中考试化学试题辽宁省大连育明高级中学2018届高三人教版选修四同步周测三化学试题北京市海淀区101中学2018-2019学年下学期高二期中考试化学试题河北省张家口第一中学2019-2020学年高二9月月考化学试题陕西省西安中学2019-2020学年高二上学期期中考试化学试题四川省攀枝花市第十五中学2019-2020学年高二上学期第二次月考化学试题湖南省岳阳市2019-2020学年高二下学期期末考试化学试题河北省张家口市宣化区宣化第一中学2020-2021学年高二上学期9月月考化学试题江西省南昌市第二中学2020-2021学年高二上学期第一次月考化学试题河北省沧州市泊头市第一中学2020-2021学年高二上学期第一次月考化学试题山西省长治市第二中学校2020-2021学年高二上学期第一次月考化学试题山东省济宁市曲阜市第一中学2020-2021学年高二上学期阶段性检测(9月月考)化学试题海南儋州市第一中学2020-2021学年高二上学期第一次月考化学试题河北省唐山市一中2020-2021学年高二下学期期中考试化学试题江西省名校2021-2022学年高二上学期第一次月考化学试题江西省南昌八一中学2021-2022学年高二上学期10月份月考化学试题安徽省淮北市树人高级中学2021-2022学年高二上学期第一次月考化学试题广东省普宁市第二中学2021-2022学年高二上学期9月份第一次月考化学试题福建省莆田市第二中学2021-2022学年高二上学期10月阶段检测化学试题广东省执信中学番禺附属学校2021-2022学年高二上学期期中考试化学试题浙江省S9联盟2021-2022学年高二上学期期中联考化学试题浙江省金衢六校联盟2021-2022学年高二上学期期末联考化学试题广东省佛山市第一中学2021-2022学年高二上学期第一次段考化学试题 吉林省松原市长岭县第三中学2021-2022学年高二上学期第三次考试化学试题河北省沧州市泊头市第一中学2021-2022学年高二上学期第一次月考化学试题新疆柯坪县柯坪湖州国庆中学2021-2022学年高二下学期期末考试化学试题四川省成都外国语学校2022-2023学年高二上学期期中考试化学试题北京市第三十五中学2022-2023学年高二上学期10月月考化学试题广西柳州地区民族高级中学2022-2023学年高二下学期期中考试化学试题河南省洛阳市2022-2023学年高二下学期质量检测化学试题河南省洛阳市 洛宁县第一高级中学2022-2023学年高二下学期5月质量检测化学试题江苏省连云港市东海县石榴高级中学2022-2023学年高二上学期第一次学情测试化学试题广东省佛山市三水中学2022-2023学年高二上学期10月第一次统测化学试题广西防城港市实验高级中学2023-2024学年高二下学期期中考试化学试题河南省林州市第一中学2018届高三8月调研考试化学试题河南省豫南豫北名校2018届高三精英联赛化学试题1陕西省陕师大附中2018届高三第五次月考化学试题河南省豫南豫北名校2018届高三精英联赛化学试题2北京市第十中学2019届高三第一学期10月月考化学试题北京市昌平区新学道临川学校2020届高三上学期期中考试化学试题山东省济南市历城二中2020届高三一轮复习验收化学试题(已下线)《2020年新高考政策解读与配套资源》模拟试题11-2020年北京新高考化学模拟试题(已下线)考点06 化学能与热能-2020年高考化学命题预测与模拟试题分类精编北京市通州区2020届高三第一次模拟考试化学试题宁夏回族自治区银川一中2020届高三下学期第五次模拟考试理综化学试题安徽省六安市舒城中学2019-2020学年高一下学期第一次月考化学试题内蒙古自治区乌兰察布市集宁一中2019-2020学年高一下学期第三次月考化学试题鲁科版(2019)高一必修第二册 第2章 化学键 反应规律 章末综合检测卷北京首都师范大学第二附属中学2021届高三10月月考化学试题山东省烟台市中英文学校2021届高三上学期冬学竞赛化学试题(人教版2019)必修第二册 第六章 化学反应与能量 第一节 化学反应与能量变化湖南省炎德英才大联考长沙市第一中学2021届高三上学期第五次月考化学试题宁夏六盘山市高级中学2020-2021学年高三下学期第二次模拟测试理综化学试题河北省衡水市安平中学2020-2021学年高一下学期第一次月考化学试题山东省日照市莒县2020-2021学年高一下学期期中考试化学试题福建省厦门双十中学2021-2022学年高一下学期期中考试化学试题福建省厦门双十中学2021-2022学年高一下学期期中考试化学试题山东省新泰市第一中学2021-2022学年高一下学期期中考试化学试题河北省藁城新冀明中学2021-2022学年高三上学期第一次月考化学试题山东省滨州市博兴第二中学2022-2023学年高一下学期第二次月考化学试题(已下线)2023年湖南卷高考真题变式题(选择题6-10)北京市首都师范大学附属中学2023-2024学年高三下学期3月月考化学试题江西省南昌市2023-2024学年高一下学期7月期末调研检测化学试题
7 . H2S是一种高毒性、高腐蚀性的气体污染物。最新研究表明,在多孔炭材料上搭载活性组分催化氧化脱硫效果明显优于传统的吸附法,其反应机理如图所示,此时H2S在水中浓度为0.34g/L。下列有关说法不正确的是
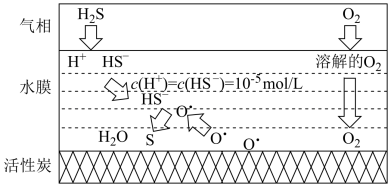

| A.活性炭的作用为吸附剂和降低反应的活化能 |
| B.H2S的一级电离常数为10-8 |
C.该反应的总反应方程式为: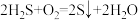 |
| D.温度愈高,多孔炭材料催化氧化脱硫的效果一定愈好 |
您最近一年使用:0次
2022-02-28更新
|
413次组卷
|
5卷引用:辽宁省朝阳市建平县实验中学2022-2023学年高二上学期第一次月考化学试题
名校
8 . 对于反应2N2O5(g)→4NO2(g)+O2(g)的反应历程如下:
第一步:N2O5 NO2+NO3 快速平衡
NO2+NO3 快速平衡
第二步:NO2+NO3→NO+NO2+O2 慢反应
第三步:NO+NO3→2NO2 快反应
其中可近似认为第二步反应不影响第一步的平衡。下列表述错误的是
第一步:N2O5
 NO2+NO3 快速平衡
NO2+NO3 快速平衡第二步:NO2+NO3→NO+NO2+O2 慢反应
第三步:NO+NO3→2NO2 快反应
其中可近似认为第二步反应不影响第一步的平衡。下列表述错误的是
| A.v(第一步的逆反应)>v(第二步反应) |
| B.反应的中间产物只有NO3 |
| C.第二步中NO2与NO3的碰撞仅部分有效 |
| D.第二步反应活化能较高 |
您最近一年使用:0次
2022-01-10更新
|
241次组卷
|
2卷引用:辽宁师范大学附属中学2021-2022学年高二上学期10月月考化学试题
名校
9 . 雾霾已经成为城市发展的障碍。雾霾形成的最主要原因是人为排放,其中汽车尾气污染对雾霾的“贡献”逐年增加。为了减轻大气污染,可在汽车尾气排放处加装“催化净化器”装置。
(1)已知:C(s)+O2(g)=CO2(g) ΔH1=-393.0kJ/mol;C(s)+ O2(g)=CO(g) ΔH2=-110.0kJ/mol;N2(g)+O2(g)=2NO(g) ΔH3=+180.0kJ/mol。通过汽车“催化净化器”的CO、NO在催化剂和高温作用下可发生可逆反应,转化为参与大气循环的无毒混合气体,写出该反应的热化学方程式:
O2(g)=CO(g) ΔH2=-110.0kJ/mol;N2(g)+O2(g)=2NO(g) ΔH3=+180.0kJ/mol。通过汽车“催化净化器”的CO、NO在催化剂和高温作用下可发生可逆反应,转化为参与大气循环的无毒混合气体,写出该反应的热化学方程式:___ 。
(2)一定条件下进行上述反应,测得CO的平衡转化率与温度、起始投料比m[m=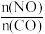 ]的关系如图所示。
]的关系如图所示。
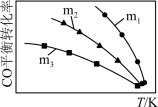
回答下列问题:
①投料比m1、m2、m3中,最大的是___ 。
②随着温度的升高,不同投料比下CO平衡转化率趋于相近的原因是___ 。
(3)为研究气缸中NO的生成,在体积可变的恒压密闭容器中,高温下充入物质的量均为1mol的氮气和氧气,发生反应N2(g)+O2(g) 2NO(g)。
2NO(g)。
①为减小平衡混合气中NO的体积分数,可采取的措施是___ (填“升高温度”或“降低温度”)。
②对于气缸中NO的生成,化学家提出了如下反应历程:第一步O2 2O慢反应,第二步O+N2
2O慢反应,第二步O+N2 NO+N较快平衡,第三步N+O2
NO+N较快平衡,第三步N+O2 NO+O快速平衡。下列说法正确的是
NO+O快速平衡。下列说法正确的是___ (填序号)。.
A.N、O原子均为该反应的催化剂
B.第一步反应不从N2分解开始,是因为N2比O2稳定
C.三步反应中第一步反应活化能最小
D.三步反应的速率都随温度升高而增大
(4)氢能源是绿色燃料,可以减少汽车尾气的排放,利用甲醇与水蒸气反应可以制备氢气:CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH1,如图是该反应的能量变化图:
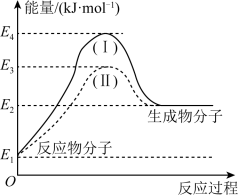
①通过图中信息可判断反应CH3OH(g)+H2O(g)↑=CO2(g)+3H2(g)的ΔH1___ (选填“>”“=”或“<”)0。
②图中途径(II)使用了催化剂。则途径(II)的活化能___ (选填“>”“=”或“<”)途径(I)的活化能。
(1)已知:C(s)+O2(g)=CO2(g) ΔH1=-393.0kJ/mol;C(s)+
 O2(g)=CO(g) ΔH2=-110.0kJ/mol;N2(g)+O2(g)=2NO(g) ΔH3=+180.0kJ/mol。通过汽车“催化净化器”的CO、NO在催化剂和高温作用下可发生可逆反应,转化为参与大气循环的无毒混合气体,写出该反应的热化学方程式:
O2(g)=CO(g) ΔH2=-110.0kJ/mol;N2(g)+O2(g)=2NO(g) ΔH3=+180.0kJ/mol。通过汽车“催化净化器”的CO、NO在催化剂和高温作用下可发生可逆反应,转化为参与大气循环的无毒混合气体,写出该反应的热化学方程式:(2)一定条件下进行上述反应,测得CO的平衡转化率与温度、起始投料比m[m=
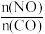 ]的关系如图所示。
]的关系如图所示。
回答下列问题:
①投料比m1、m2、m3中,最大的是
②随着温度的升高,不同投料比下CO平衡转化率趋于相近的原因是
(3)为研究气缸中NO的生成,在体积可变的恒压密闭容器中,高温下充入物质的量均为1mol的氮气和氧气,发生反应N2(g)+O2(g)
 2NO(g)。
2NO(g)。①为减小平衡混合气中NO的体积分数,可采取的措施是
②对于气缸中NO的生成,化学家提出了如下反应历程:第一步O2
 2O慢反应,第二步O+N2
2O慢反应,第二步O+N2 NO+N较快平衡,第三步N+O2
NO+N较快平衡,第三步N+O2 NO+O快速平衡。下列说法正确的是
NO+O快速平衡。下列说法正确的是A.N、O原子均为该反应的催化剂
B.第一步反应不从N2分解开始,是因为N2比O2稳定
C.三步反应中第一步反应活化能最小
D.三步反应的速率都随温度升高而增大
(4)氢能源是绿色燃料,可以减少汽车尾气的排放,利用甲醇与水蒸气反应可以制备氢气:CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH1,如图是该反应的能量变化图:

①通过图中信息可判断反应CH3OH(g)+H2O(g)↑=CO2(g)+3H2(g)的ΔH1
②图中途径(II)使用了催化剂。则途径(II)的活化能
您最近一年使用:0次
2022-01-05更新
|
144次组卷
|
3卷引用:辽宁省渤海大学附属高级中学2021-2022学年高二上学期期中考试化学试题
名校
10 . 我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器因受到环境腐蚀,对其进行修复和防护具有重要意义。研究发现,腐蚀严重的青铜器表面大都存在CuCl。下列关于CuCl在青铜器腐蚀过程中的催化作用的叙述错误的是
| A.降低了反应的活化能 | B.增大了反应的速率 |
| C.增大了反应的平衡常数 | D.增大了单位体积内活化分子百分数 |
您最近一年使用:0次
2022-01-01更新
|
363次组卷
|
5卷引用:辽宁省朝阳市建平县实验中学2022-2023学年高二上学期第一次月考化学试题



