江西师范大学附属中学2022届高三下学期三模理科综合化学试题
江西
高三
三模
2022-07-09
1320次
整体难度:
适中
考查范围:
常见无机物及其应用、有机化学基础、化学与STSE、认识化学科学、化学反应原理、物质结构与性质、化学实验基础
江西师范大学附属中学2022届高三下学期三模理科综合化学试题
江西
高三
三模
2022-07-09
1320次
整体难度:
适中
考查范围:
常见无机物及其应用、有机化学基础、化学与STSE、认识化学科学、化学反应原理、物质结构与性质、化学实验基础
一、单选题 添加题型下试题
单选题
|
适中(0.65)
名校
解题方法
1. 历史文物本身蕴含着许多化学知识,下列说法错误的是
| A.我国古老的马家窑青铜刀属于青铜制品,青铜是一种合金 |
| B.范宽的《溪山行旅图》属于绢本水墨画,其中作画用的墨的主要成分为炭黑 |
| C.中国古代专为皇宫烧制的细料方砖,质地密实,敲之作金石之声,称之“金砖”,属于硅酸盐产品 |
| D.享誉世界的中国丝绸,其主要成分为天然纤维,在元素组成上与纤维素完全相同 |
【知识点】 含硅的无机非金属材料解读 蛋白质组成结构 常见合金的组成解读
您最近一年使用:0次
2022-04-13更新
|
1566次组卷
|
7卷引用:卷01 化学与STSE-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)
(已下线)卷01 化学与STSE-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)微专题01 “话”中有“化”—化学与传统文化-备战2023年高考化学一轮复习考点微专题江西师范大学附属中学2022届高三下学期三模理科综合化学试题(已下线)2023年高考山东卷化学真题变式题(选择题1-5)(已下线)2023年湖南卷高考真题变式题(选择题1-5)湖南师范大学附属中学2023-2024学年高二上学期入学考试化学试题 河北省承德市部分高中2023-2024学年高三上学期12月期中考试化学试题
单选题
|
适中(0.65)
名校
解题方法
2. 下列离子方程式书写正确的是
A.强碱性溶液中NaClO与Fe(OH)3反应生成Na2FeO4: 3ClO- +4OH- + 2Fe(OH)3= 3Cl-+ 5H2O+ 2 |
B.用银电极电解AgNO3溶液: 4Ag++2H2O 4Ag+O2↑+4H+ 4Ag+O2↑+4H+ |
C.过量SO2通入苯酚钠溶液中: 2C6H5O- + SO2+H2O= 2C6H5OH+  |
| D.Ca(ClO)2 溶液中通入少量SO2: Ca2++ ClO-+ SO2+ H2O= CaSO4+Cl -+ 2H+ |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
3. 化合物Z是合成抗多发性骨髓瘤药物帕比司他的重要中间体,可由下列反应制得。

下列有关X、Y、Z的说法不正确的是

下列有关X、Y、Z的说法不正确的是
| A.Y既可以发生加聚反应,也可以发生缩聚反应 |
| B.X、Y、Z分别与足量酸性KMnO4溶液反应所得芳香族化合物相同 |
| C.Y在水中的溶解度比Z在水中的溶解度大 |
| D.Y与足量H2反应生成的有机化合物中含2个手性碳原子 |
您最近一年使用:0次
2022-06-27更新
|
528次组卷
|
3卷引用:江西师范大学附属中学2022届高三下学期三模理科综合化学试题
单选题
|
适中(0.65)
4. H2S是一种高毒性、高腐蚀性的气体污染物。最新研究表明,在多孔炭材料上搭载活性组分催化氧化脱硫效果明显优于传统的吸附法,其反应机理如图所示,此时H2S在水中浓度为0.34g/L。下列有关说法不正确的是
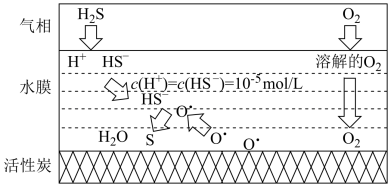

| A.活性炭的作用为吸附剂和降低反应的活化能 |
| B.H2S的一级电离常数为10-8 |
C.该反应的总反应方程式为: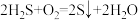 |
| D.温度愈高,多孔炭材料催化氧化脱硫的效果一定愈好 |
您最近一年使用:0次
2022-02-28更新
|
401次组卷
|
5卷引用:湖南省长沙市雅礼中学2021-2022学年高三上学期月考卷(三)化学试题
单选题
|
适中(0.65)
名校
5. 原子序数依次增大的同一短周期主族元素W、X、Y、Z与锂组成的盐是一种新型锂离子电池的电解质,其结构如图所示,→表示配位键,表示共用电子对全部由Z原子单独提供,其中Y的一种单质可用作消毒剂。下列有关说法正确的是
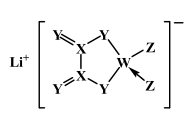

| A.简单离子半径: Z>Y>Li+ |
| B.含X元素的二元弱酸不止1种 |
| C.W最高氧化物对应的水化物是一种三元弱酸 |
| D.该物质中所有粒子均满足8电子相对稳定结构 |
【知识点】 元素周期律、元素周期表的推断 微粒半径大小的比较方法解读
您最近一年使用:0次
单选题
|
适中(0.65)
名校
6. 近日,南开大学陈军院士团队以KSn合金为负极,以含羧基多壁碳纳米管(MWCNTs—COOH)为正极催化剂构建了可充电K—CO2电池(如图所示),电池反应为4KSn+3CO2 2K2CO3+C+4Sn,其中生成的K2CO3附着在正极上。该成果对改善环境和缓解能源问题具有巨大潜力。下列说法正确的是
2K2CO3+C+4Sn,其中生成的K2CO3附着在正极上。该成果对改善环境和缓解能源问题具有巨大潜力。下列说法正确的是

 2K2CO3+C+4Sn,其中生成的K2CO3附着在正极上。该成果对改善环境和缓解能源问题具有巨大潜力。下列说法正确的是
2K2CO3+C+4Sn,其中生成的K2CO3附着在正极上。该成果对改善环境和缓解能源问题具有巨大潜力。下列说法正确的是
| A.放电时,电子由KSn合金经酯基电解质流向MWCNTs—COOH |
| B.电池每吸收22.4LCO2,电路中转移4mole- |
| C.充电时,阳极电极反应式为:C-4e-+2K2CO3=3CO2↑+4K+ |
| D.为了更好的吸收温室气体CO2,可用适当浓度的KOH溶液代替酯基电解质 |
【知识点】 原电池原理的综合应用解读 二次电池
您最近一年使用:0次
2021-06-12更新
|
794次组卷
|
5卷引用:【一飞冲天】6.芦台一中一模
(已下线)【一飞冲天】6.芦台一中一模(已下线)专题讲座(四)新型电源及电极反应式的书写(练) — 2022年高考化学一轮复习讲练测(新教材新高考)浙江省安吉高级中学2022届高三上学期1月首考仿真考模拟化学试题江西师范大学附属中学2022届高三下学期三模理科综合化学试题天津市南开中学2023-2024学年高三上学期统练5化学试题
单选题
|
适中(0.65)
名校
7. 已知SrF2属于难溶于水、可溶于酸的盐。常温下,用HCl调节SrF2浊液的pH,测得在不同pH条件下,体系中-1gc(X)(X为Sr2+或F-)与1g[ ]的关系如图所示。
]的关系如图所示。

下列说法错误的是
 ]的关系如图所示。
]的关系如图所示。
下列说法错误的是
A.L1代表-lgc(Sr2+)与lg[ ]的变化曲线 ]的变化曲线 |
| B.Ksp(SrF2)的数量级为10-9 |
| C.a、c两点的溶液中均存在2c(Sr2+)=c(F-)+c(HF) |
| D.c点的溶液中存在c(Cl-)>c(Sr2+)=c(HF)>c(H+) |
您最近一年使用:0次
2022-03-11更新
|
2215次组卷
|
7卷引用:河北省石家庄市2021-2022学年下学期高中毕业班教学质量检测(一)化学试题
河北省石家庄市2021-2022学年下学期高中毕业班教学质量检测(一)化学试题山东省泰安市2022届高三二轮验收考试化学试题江西师范大学附属中学2022届高三下学期三模理科综合化学试题(已下线)专题13 水溶液中的离子平衡-备战2023年高考化学母题题源解密(全国通用)山东省鄄城县第一中学2022-2023学年高二上学期期末考试化学试题广东省茂名市第一中学2022-2023学年高二上学期期中考试化学试题(已下线)T13-溶液中的离子平衡
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
名校
8. 碳酸镧La2(CO3)3(Mr=458)为白色粉末、难溶于水、分解温度900℃,可用于治疗高磷酸盐血症。在溶液中制备时,形成水合碳酸镧La2(CO3)3·xH2O,如果溶液碱性太强,易生成受热分解的碱式碳酸镧La(OH)CO3,已知酒精喷灯温度可达1000℃。回答下列问题:
(1)用如图装置模拟制备水合碳酸镧:
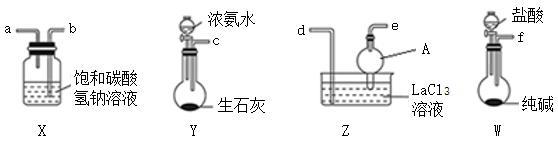
①仪器A的名称为___________ 。
②装置接口的连接顺序为f→___________ →c。
③Z中应先通入___________ ,后通入过量的另一种气体,该气体需要过量的原因是___________ 。
④该反应中生成副产物氯化铵,请写出生成水合碳酸镧[La2(CO3)3·xH2O]的化学方程式:___________ 。
(2)甲小组通过以下实验验证制得的样品中不含La(OH)CO3,并测定水合碳酸镧La2(CO3)3·xH2O中结晶水的含量,将石英玻璃A管称重,记为m1g,将样品装入石英玻璃管中,再次将装置A称重,记为m2g,将装有试剂的装置C称重,记为m3g,按图示连接好装置进行实验。
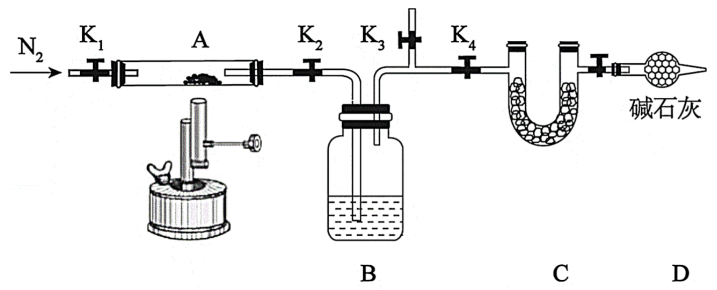
实验步骤:
①打开K1、K2和K3,缓缓通入N2;
②数分钟后关闭K1,K3,打开K4,点燃酒精喷灯,加热A中样品;
③一段时间后,熄灭酒精灯,打开K1,通入N2数分钟后关闭K1和K2,冷却到室温,称量A.重复上述操作步骤,直至A恒重,记为m4g(此时装置A中为La2O3Mr=326)。称重装置C,记为m5g。
①实验中第二次通入N2的目的为___________ 。D中碱石灰的作用___________ 。
②根据实验记录,当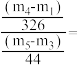
___________ ,说明制得的样品中不含有La(OH)CO3;计算水合碳酸镧化学式中结晶水数目x=___________ (用含m1、m2、m4的式子表示,不用化简)。
(1)用如图装置模拟制备水合碳酸镧:

①仪器A的名称为
②装置接口的连接顺序为f→
③Z中应先通入
④该反应中生成副产物氯化铵,请写出生成水合碳酸镧[La2(CO3)3·xH2O]的化学方程式:
(2)甲小组通过以下实验验证制得的样品中不含La(OH)CO3,并测定水合碳酸镧La2(CO3)3·xH2O中结晶水的含量,将石英玻璃A管称重,记为m1g,将样品装入石英玻璃管中,再次将装置A称重,记为m2g,将装有试剂的装置C称重,记为m3g,按图示连接好装置进行实验。

实验步骤:
①打开K1、K2和K3,缓缓通入N2;
②数分钟后关闭K1,K3,打开K4,点燃酒精喷灯,加热A中样品;
③一段时间后,熄灭酒精灯,打开K1,通入N2数分钟后关闭K1和K2,冷却到室温,称量A.重复上述操作步骤,直至A恒重,记为m4g(此时装置A中为La2O3Mr=326)。称重装置C,记为m5g。
①实验中第二次通入N2的目的为
②根据实验记录,当
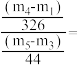
您最近一年使用:0次
2021-05-21更新
|
562次组卷
|
2卷引用:黑龙江省哈尔滨第六中学2021届高三第四次模拟理综化学试题
9. 北京时间2021年10月16日上午,神舟十三号航天员顺利进驻“天和”核心舱,开启为期6个月的航天飞行任务。航天员生活、工作于其中的“天和”核心舱是利用三结砷化镓太阳能电池作为其动力。一种由砷化家废料(主要成分为GaAs,含Fe2O3、SiO2等杂质)制备镓的工艺流程如图:
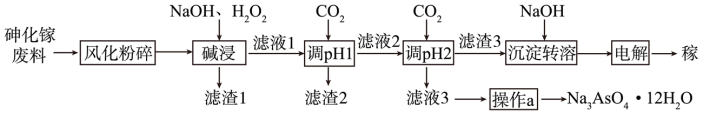
已知:①Ga在周期表中位于Al的正下方,性质与Al相似;
②离子完全沉淀的pH值: 为8,
为8,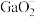 为5.5。
为5.5。
回答下列问题:
(1)“风化粉碎”的目的是_______ 。
(2)“碱浸”温度控制在70℃左右,温度不能过高或过低的原因是_______ 。
(3)“碱浸”时,GaAs中Ga以 的形式进入溶液中,该反应的离子方程式是
的形式进入溶液中,该反应的离子方程式是_______ 。
(4)“滤渣1”的成分为_______ (填化学式),“操作a”为_______ 、过滤、洗涤、干燥。
(5)“调pH1”时,不能通入过量的 ,其原因是
,其原因是_______ 。
(6)若用240kg含7.25%砷化镓的废料回收家,得到纯度为96%的镓7.0kg,则家的回收率为_______ %(保留3位有效数字)。

已知:①Ga在周期表中位于Al的正下方,性质与Al相似;
②离子完全沉淀的pH值:
 为8,
为8,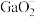 为5.5。
为5.5。回答下列问题:
(1)“风化粉碎”的目的是
(2)“碱浸”温度控制在70℃左右,温度不能过高或过低的原因是
(3)“碱浸”时,GaAs中Ga以
 的形式进入溶液中,该反应的离子方程式是
的形式进入溶液中,该反应的离子方程式是(4)“滤渣1”的成分为
(5)“调pH1”时,不能通入过量的
 ,其原因是
,其原因是(6)若用240kg含7.25%砷化镓的废料回收家,得到纯度为96%的镓7.0kg,则家的回收率为
您最近一年使用:0次
2022-03-22更新
|
878次组卷
|
3卷引用:湖南省长郡中学2021-2022学年高三上学期第四次月考化学试题
解答题-原理综合题
|
较难(0.4)
名校
解题方法
10. 晶体硅材料是最主要的光伏材料,随当前信息工程的发展,硅主要用于微电子技术。工业上将粗硅氯化、精馏后得到SiCl4和SiHCl3的混合物然后用H2还原得到高纯硅。还原过程中发生的主要反应为:
i.SiCl4(g)+2H2(g) Si(s)+4HCl(g) △H1=akJ/mol
Si(s)+4HCl(g) △H1=akJ/mol
ii.SiHCl3(g)+H2(g) Si(s)+3HCl(g) △H2=bkJ/mol
Si(s)+3HCl(g) △H2=bkJ/mol
回答下列问题:
(1)已知:2SiHCl3(g) SiCl4(g)+SiH2Cl2(g) △H3=48kJ/mol
SiCl4(g)+SiH2Cl2(g) △H3=48kJ/mol
H2(g)还原SiCl4(g)生成SiH2Cl2(g)的热化学方程式为_______ 。
(2)在T1、T2温度下,将1molSiCl4(g)、1molSiHCl3(g)和3molH2(g)加入体积固定的密闭容器中,在催化条件下发生反应i、ii。测得H2的转化率及体系内的压强随时间的变化关系如图所示。
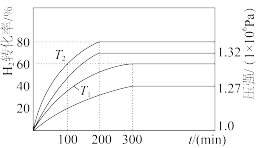
①T2温度下,反应达到平衡时SiHCl3(g)的转化率_______ 。
②T2温度下,反应i的标准平衡常数Kθ的计算式为_______ 。
(已知:分压=总压×该组分物质的量分数,对于反应dD(g)+eE(g) gG(g)+hH(g)的Kθ=
gG(g)+hH(g)的Kθ=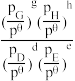 ,其中pθ=106Pa,pG、pH、pD、pE为各组分的平衡分压)。
,其中pθ=106Pa,pG、pH、pD、pE为各组分的平衡分压)。
③△H2_______ 0(填“>”或“<”),写出推理过程_______ 。
④要增大SiCl4(g)的转化率可以采取的措施有_______ (写其中的一条即可)。
(3)研究发现,反应SiCl4(g)+SiH2Cl2(g) 2SiHCl3(g)的活化能Ea=100kJ/mol。反应的活化能Ea、速率常数k、温度T满足关系:ln
2SiHCl3(g)的活化能Ea=100kJ/mol。反应的活化能Ea、速率常数k、温度T满足关系:ln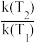 =
=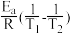 =-
=- 。
。
已知:R=8.3×10-3kJ/(mol·K);ln10=2.3
①若T1=300K,通过升高温度到595K,才能满足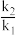 =108以加快反应速率;
=108以加快反应速率;
②若T=300K,使用催化剂使活化能降低,满足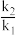 =108以加快反应速率,Ea应减小。
=108以加快反应速率,Ea应减小。
上述②中Ea应减小_______ kJ/mol(保留1位小数);对比①和②你得到的结论是_______ 。
i.SiCl4(g)+2H2(g)
 Si(s)+4HCl(g) △H1=akJ/mol
Si(s)+4HCl(g) △H1=akJ/molii.SiHCl3(g)+H2(g)
 Si(s)+3HCl(g) △H2=bkJ/mol
Si(s)+3HCl(g) △H2=bkJ/mol回答下列问题:
(1)已知:2SiHCl3(g)
 SiCl4(g)+SiH2Cl2(g) △H3=48kJ/mol
SiCl4(g)+SiH2Cl2(g) △H3=48kJ/molH2(g)还原SiCl4(g)生成SiH2Cl2(g)的热化学方程式为
(2)在T1、T2温度下,将1molSiCl4(g)、1molSiHCl3(g)和3molH2(g)加入体积固定的密闭容器中,在催化条件下发生反应i、ii。测得H2的转化率及体系内的压强随时间的变化关系如图所示。

①T2温度下,反应达到平衡时SiHCl3(g)的转化率
②T2温度下,反应i的标准平衡常数Kθ的计算式为
(已知:分压=总压×该组分物质的量分数,对于反应dD(g)+eE(g)
 gG(g)+hH(g)的Kθ=
gG(g)+hH(g)的Kθ=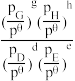 ,其中pθ=106Pa,pG、pH、pD、pE为各组分的平衡分压)。
,其中pθ=106Pa,pG、pH、pD、pE为各组分的平衡分压)。③△H2
④要增大SiCl4(g)的转化率可以采取的措施有
(3)研究发现,反应SiCl4(g)+SiH2Cl2(g)
 2SiHCl3(g)的活化能Ea=100kJ/mol。反应的活化能Ea、速率常数k、温度T满足关系:ln
2SiHCl3(g)的活化能Ea=100kJ/mol。反应的活化能Ea、速率常数k、温度T满足关系:ln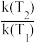 =
=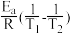 =-
=- 。
。已知:R=8.3×10-3kJ/(mol·K);ln10=2.3
①若T1=300K,通过升高温度到595K,才能满足
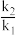 =108以加快反应速率;
=108以加快反应速率;②若T=300K,使用催化剂使活化能降低,满足
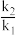 =108以加快反应速率,Ea应减小。
=108以加快反应速率,Ea应减小。上述②中Ea应减小
您最近一年使用:0次
2022-05-04更新
|
891次组卷
|
3卷引用:山东省潍坊市2022届高三二模考试化学试题
解答题-结构与性质
|
适中(0.65)
名校
解题方法
11. 我国科学家首次用砷化镉纳米片观察到三维量子霍尔效应,并在碲化锆(ZrTe5)上发现了金属-绝缘体的转换,此项研究成果对红外探测等的研究具有应用价值。回答下列问题:
(1)基态As原子价电子排布图为_______ ,电子占据最高能级的电子云轮廓图形状为_______ 。
(2)AsH3的空间构型为_______ ;H3PO4分子中P的杂化轨道与O的_______ 轨道形成_______ 键。
(3)ZnS熔点为2830℃,CdS熔点为1750℃,ZnS熔点更高的原因是_______ 。
(4)碱式碳酸锆(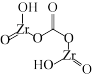 )中C原子的杂化方式为
)中C原子的杂化方式为_______ ;该化合物中非金属元素的第一电离能大小关系为_______ 。
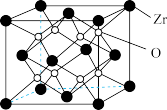
(5)氧化锆晶胞结构如图所示,其硬度极高,可用于陶瓷和耐火材料。晶胞中Zr原子的配位数为_______ ;已知阿伏加德罗常数的值为NA,若晶体的密度为ρg/cm3,则该晶胞中距离最近的两个锆原子之间的距离为_______ cm(列出计算式)。
(1)基态As原子价电子排布图为
(2)AsH3的空间构型为
(3)ZnS熔点为2830℃,CdS熔点为1750℃,ZnS熔点更高的原因是
(4)碱式碳酸锆(
 )中C原子的杂化方式为
)中C原子的杂化方式为(5)氧化锆晶胞结构如图所示,其硬度极高,可用于陶瓷和耐火材料。晶胞中Zr原子的配位数为

您最近一年使用:0次
2022-04-24更新
|
894次组卷
|
2卷引用:广西壮族自治区南宁市2022届高三第二次适应性测试理综化学试题
解答题-有机推断题
|
较难(0.4)
名校
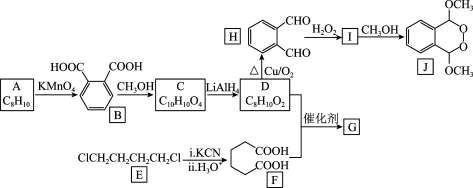
12. 高聚物G是一种合成纤维,由A与E为原料制备J和G的一种合成路线如下:
已知:①酯能被LiAlH4还原为醇
②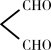
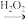

回答下列问题:
(1)A的结构简式为___________ ,B生成C的反应条件为___________ 。
(2)H的名称是___________ ,J中含有的官能团名称为过氧键和___________ 。
(3)D生成H和I生成J反应类型分别为___________ 、___________ 。
(4)写出F+D→G的化学方程式:___________ 。
(5)芳香化合物M是C的同分异构体,符合下列要求的M有___________ 种(不考虑立体异构)
①与碳酸钠溶液反应产生气体 ②只有1种官能团 ③苯环上有2个取代基
其中核磁共振氢谱显示有4种不同化学环境的氢,峰面积之比1∶1∶1∶2的结构简式为___________ 。
(6)参照上述合成路线,写出用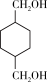 为原料制备化合物
为原料制备化合物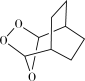 的合成路线(其他无机试剂任选)。
的合成路线(其他无机试剂任选)。___________

已知:①酯能被LiAlH4还原为醇
②

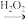

回答下列问题:
(1)A的结构简式为
(2)H的名称是
(3)D生成H和I生成J反应类型分别为
(4)写出F+D→G的化学方程式:
(5)芳香化合物M是C的同分异构体,符合下列要求的M有
①与碳酸钠溶液反应产生气体 ②只有1种官能团 ③苯环上有2个取代基
其中核磁共振氢谱显示有4种不同化学环境的氢,峰面积之比1∶1∶1∶2的结构简式为
(6)参照上述合成路线,写出用
 为原料制备化合物
为原料制备化合物 的合成路线(其他无机试剂任选)。
的合成路线(其他无机试剂任选)。【知识点】 缩聚反应 有机物的推断 根据题给物质选择合适合成路线解读
您最近一年使用:0次
2021-09-03更新
|
728次组卷
|
4卷引用:湖南省株洲市第二中学2022届高三上学期入学考试化学试题
湖南省株洲市第二中学2022届高三上学期入学考试化学试题江西师范大学附属中学2022届高三下学期三模理科综合化学试题(已下线)第九章 有机化学基础 第62练 有机合成推断及合成路线设计(已下线)第6讲 有机推断与有机合成
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、有机化学基础、化学与STSE、认识化学科学、化学反应原理、物质结构与性质、化学实验基础
试卷题型(共 12题)
题型
数量
单选题
7
解答题
5
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 含硅的无机非金属材料 蛋白质组成结构 常见合金的组成 | |
| 2 | 0.65 | 离子方程式的正误判断 漂白粉和漂粉精 电解池电极反应式及化学方程式的书写与判断 苯酚的弱酸性 | |
| 3 | 0.65 | 含碳碳双键物质的性质的推断 缩聚反应 多官能团有机物的结构与性质 | |
| 4 | 0.65 | 活化能及其对反应速率的影响 催化剂对化学反应速率的影响 弱电解质的电离平衡常数 | |
| 5 | 0.65 | 元素周期律、元素周期表的推断 微粒半径大小的比较方法 | |
| 6 | 0.65 | 原电池原理的综合应用 二次电池 | |
| 7 | 0.65 | 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 难溶电解质的溶解平衡 沉淀溶解平衡的应用 溶度积常数相关计算 | |
| 二、解答题 | |||
| 8 | 0.65 | 中和滴定 综合实验设计与评价 | 实验探究题 |
| 9 | 0.4 | 氧化还原反应方程式的配平 有关铁及其化合物转化的流程题型 物质分离、提纯综合应用 常见无机物的制备 | 工业流程题 |
| 10 | 0.4 | 盖斯定律及其有关计算 化学平衡的移动及其影响因素 化学平衡的有关计算 化学平衡图像分析 | 原理综合题 |
| 11 | 0.65 | 轨道表示式 电离能变化规律 利用杂化轨道理论判断分子的空间构型 晶胞的有关计算 | 结构与性质 |
| 12 | 0.4 | 缩聚反应 有机物的推断 根据题给物质选择合适合成路线 | 有机推断题 |



