雾霾已经成为城市发展的障碍。雾霾形成的最主要原因是人为排放,其中汽车尾气污染对雾霾的“贡献”逐年增加。为了减轻大气污染,可在汽车尾气排放处加装“催化净化器”装置。
(1)已知:C(s)+O2(g)=CO2(g) ΔH1=-393.0kJ/mol;C(s)+ O2(g)=CO(g) ΔH2=-110.0kJ/mol;N2(g)+O2(g)=2NO(g) ΔH3=+180.0kJ/mol。通过汽车“催化净化器”的CO、NO在催化剂和高温作用下可发生可逆反应,转化为参与大气循环的无毒混合气体,写出该反应的热化学方程式:
O2(g)=CO(g) ΔH2=-110.0kJ/mol;N2(g)+O2(g)=2NO(g) ΔH3=+180.0kJ/mol。通过汽车“催化净化器”的CO、NO在催化剂和高温作用下可发生可逆反应,转化为参与大气循环的无毒混合气体,写出该反应的热化学方程式:___ 。
(2)一定条件下进行上述反应,测得CO的平衡转化率与温度、起始投料比m[m=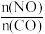 ]的关系如图所示。
]的关系如图所示。
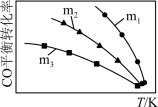
回答下列问题:
①投料比m1、m2、m3中,最大的是___ 。
②随着温度的升高,不同投料比下CO平衡转化率趋于相近的原因是___ 。
(3)为研究气缸中NO的生成,在体积可变的恒压密闭容器中,高温下充入物质的量均为1mol的氮气和氧气,发生反应N2(g)+O2(g) 2NO(g)。
2NO(g)。
①为减小平衡混合气中NO的体积分数,可采取的措施是___ (填“升高温度”或“降低温度”)。
②对于气缸中NO的生成,化学家提出了如下反应历程:第一步O2 2O慢反应,第二步O+N2
2O慢反应,第二步O+N2 NO+N较快平衡,第三步N+O2
NO+N较快平衡,第三步N+O2 NO+O快速平衡。下列说法正确的是
NO+O快速平衡。下列说法正确的是___ (填序号)。.
A.N、O原子均为该反应的催化剂
B.第一步反应不从N2分解开始,是因为N2比O2稳定
C.三步反应中第一步反应活化能最小
D.三步反应的速率都随温度升高而增大
(4)氢能源是绿色燃料,可以减少汽车尾气的排放,利用甲醇与水蒸气反应可以制备氢气:CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH1,如图是该反应的能量变化图:
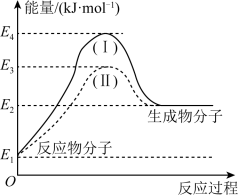
①通过图中信息可判断反应CH3OH(g)+H2O(g)↑=CO2(g)+3H2(g)的ΔH1___ (选填“>”“=”或“<”)0。
②图中途径(II)使用了催化剂。则途径(II)的活化能___ (选填“>”“=”或“<”)途径(I)的活化能。
(1)已知:C(s)+O2(g)=CO2(g) ΔH1=-393.0kJ/mol;C(s)+
 O2(g)=CO(g) ΔH2=-110.0kJ/mol;N2(g)+O2(g)=2NO(g) ΔH3=+180.0kJ/mol。通过汽车“催化净化器”的CO、NO在催化剂和高温作用下可发生可逆反应,转化为参与大气循环的无毒混合气体,写出该反应的热化学方程式:
O2(g)=CO(g) ΔH2=-110.0kJ/mol;N2(g)+O2(g)=2NO(g) ΔH3=+180.0kJ/mol。通过汽车“催化净化器”的CO、NO在催化剂和高温作用下可发生可逆反应,转化为参与大气循环的无毒混合气体,写出该反应的热化学方程式:(2)一定条件下进行上述反应,测得CO的平衡转化率与温度、起始投料比m[m=
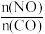 ]的关系如图所示。
]的关系如图所示。
回答下列问题:
①投料比m1、m2、m3中,最大的是
②随着温度的升高,不同投料比下CO平衡转化率趋于相近的原因是
(3)为研究气缸中NO的生成,在体积可变的恒压密闭容器中,高温下充入物质的量均为1mol的氮气和氧气,发生反应N2(g)+O2(g)
 2NO(g)。
2NO(g)。①为减小平衡混合气中NO的体积分数,可采取的措施是
②对于气缸中NO的生成,化学家提出了如下反应历程:第一步O2
 2O慢反应,第二步O+N2
2O慢反应,第二步O+N2 NO+N较快平衡,第三步N+O2
NO+N较快平衡,第三步N+O2 NO+O快速平衡。下列说法正确的是
NO+O快速平衡。下列说法正确的是A.N、O原子均为该反应的催化剂
B.第一步反应不从N2分解开始,是因为N2比O2稳定
C.三步反应中第一步反应活化能最小
D.三步反应的速率都随温度升高而增大
(4)氢能源是绿色燃料,可以减少汽车尾气的排放,利用甲醇与水蒸气反应可以制备氢气:CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH1,如图是该反应的能量变化图:

①通过图中信息可判断反应CH3OH(g)+H2O(g)↑=CO2(g)+3H2(g)的ΔH1
②图中途径(II)使用了催化剂。则途径(II)的活化能
更新时间:2022/01/05 16:14:31
|
相似题推荐
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐1】随着科学技术的发展和环保要求不断提高, 的捕集利用技术成为研究的重点。
的捕集利用技术成为研究的重点。
Ⅰ.完成下列问题
(1)工业上使用的捕碳剂有 和
和 ,它们与
,它们与 可发生如下可逆反应:
可发生如下可逆反应:
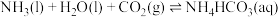

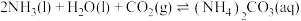

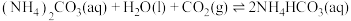

则
_______ (用含 、
、 的代表式表示)
的代表式表示)
(2)目前国际空间站处理 的一个重要方法是将
的一个重要方法是将 还原,所涉及的化学反应方程式为:
还原,所涉及的化学反应方程式为: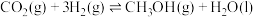 ,已知:
,已知: 的体积分数随温度的升高而增加。
的体积分数随温度的升高而增加。
①该反应的
_______ 0(填“>”、“=”、“<”),该反应的
_______ 0(填“>”、“<”)
②在体积为1L的密闭容器中,充入1mol 和3mol
和3mol ,测得
,测得 和
和 的浓度随时间变化如图所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率
的浓度随时间变化如图所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率
_______

Ⅱ.在298K时,将0.1mol 气体充入1L抽空的密闭容器中,回答下列问题:
气体充入1L抽空的密闭容器中,回答下列问题:
(3)当反应达到平衡时,对于反应 ,改变某一条件后,下列说法中,一定能说明化学平衡向正反应方向移动的是
,改变某一条件后,下列说法中,一定能说明化学平衡向正反应方向移动的是_______ 填序号)
①气体颜色加深
② 的体积分数增加
的体积分数增加
③单位时间内消耗 和
和 的物质的量之比大于1∶2
的物质的量之比大于1∶2
④恒温恒压充入惰性气体He
(4)在固定体积的密闭容器中,发生可逆反应: 。已知
。已知 对
对 的分解具有催化作用。利用如图(a)和(b)中的信息,按图(c)装置(连通的A、B瓶中已充有
的分解具有催化作用。利用如图(a)和(b)中的信息,按图(c)装置(连通的A、B瓶中已充有 气体)进行实验,可观察到B瓶中气体颜色比A瓶中的
气体)进行实验,可观察到B瓶中气体颜色比A瓶中的_______ (填“深”或“浅”)

 的捕集利用技术成为研究的重点。
的捕集利用技术成为研究的重点。Ⅰ.完成下列问题
(1)工业上使用的捕碳剂有
 和
和 ,它们与
,它们与 可发生如下可逆反应:
可发生如下可逆反应: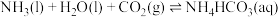

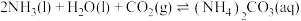

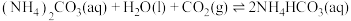

则

 、
、 的代表式表示)
的代表式表示)(2)目前国际空间站处理
 的一个重要方法是将
的一个重要方法是将 还原,所涉及的化学反应方程式为:
还原,所涉及的化学反应方程式为: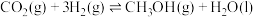 ,已知:
,已知: 的体积分数随温度的升高而增加。
的体积分数随温度的升高而增加。①该反应的


②在体积为1L的密闭容器中,充入1mol
 和3mol
和3mol ,测得
,测得 和
和 的浓度随时间变化如图所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率
的浓度随时间变化如图所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率

Ⅱ.在298K时,将0.1mol
 气体充入1L抽空的密闭容器中,回答下列问题:
气体充入1L抽空的密闭容器中,回答下列问题:(3)当反应达到平衡时,对于反应
 ,改变某一条件后,下列说法中,一定能说明化学平衡向正反应方向移动的是
,改变某一条件后,下列说法中,一定能说明化学平衡向正反应方向移动的是①气体颜色加深
②
 的体积分数增加
的体积分数增加③单位时间内消耗
 和
和 的物质的量之比大于1∶2
的物质的量之比大于1∶2④恒温恒压充入惰性气体He
(4)在固定体积的密闭容器中,发生可逆反应:
 。已知
。已知 对
对 的分解具有催化作用。利用如图(a)和(b)中的信息,按图(c)装置(连通的A、B瓶中已充有
的分解具有催化作用。利用如图(a)和(b)中的信息,按图(c)装置(连通的A、B瓶中已充有 气体)进行实验,可观察到B瓶中气体颜色比A瓶中的
气体)进行实验,可观察到B瓶中气体颜色比A瓶中的
您最近一年使用:0次
【推荐2】CH4-CO2催化重整不仅可以得到合成气(CO和H2),还对温室气体的减排具有重要意义。回答下列问题:
(1)CH4-CO2催化重整反应为:CH4(g)+CO2(g) 2CO(g)+2H2(g)ΔH。
2CO(g)+2H2(g)ΔH。
已知:C(s)+2H2(g)=CH4(g)ΔH=-75kJ·mol−1
C(s)+O2(g)=CO2(g)ΔH=-394kJ·mol−1
C(s)+ O2(g)=CO(g)ΔH=-111kJ·mol−1
O2(g)=CO(g)ΔH=-111kJ·mol−1
该催化重整反应的ΔH=________ kJ·mol−1。有利于提高CH4平衡转化率的条件是____ (填标号)。
A.高温低压B.低温高压C.高温高压D.低温低压
某温度下,在体积为2L的容器中加入2molCH4、1molCO2以及催化剂进行重整反应,达到平衡时CO2的转化率是50%,其平衡常数为___________________________ 。
素材1:研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源。该电池以金属锂和钢板为电极材料,以LiOH为电解质,使用时加入水即可放电。总反应为:2Li+2H2O===2LiOH+H2↑。根据以上素材回答下列问题:
(2)该电池的负极是________ ,负极反应式是_____________________________ 。
(3)正极现象是_______________________________________________ 。
(4)放电时OH-向_____________ (填“正极”或“负极”)移动。
(1)CH4-CO2催化重整反应为:CH4(g)+CO2(g)
 2CO(g)+2H2(g)ΔH。
2CO(g)+2H2(g)ΔH。已知:C(s)+2H2(g)=CH4(g)ΔH=-75kJ·mol−1
C(s)+O2(g)=CO2(g)ΔH=-394kJ·mol−1
C(s)+
 O2(g)=CO(g)ΔH=-111kJ·mol−1
O2(g)=CO(g)ΔH=-111kJ·mol−1该催化重整反应的ΔH=
A.高温低压B.低温高压C.高温高压D.低温低压
某温度下,在体积为2L的容器中加入2molCH4、1molCO2以及催化剂进行重整反应,达到平衡时CO2的转化率是50%,其平衡常数为
素材1:研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源。该电池以金属锂和钢板为电极材料,以LiOH为电解质,使用时加入水即可放电。总反应为:2Li+2H2O===2LiOH+H2↑。根据以上素材回答下列问题:
(2)该电池的负极是
(3)正极现象是
(4)放电时OH-向
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐3】环境治理依然是当今的热点问题。研究相关问题具有重要意义。回答下列问题:
(1)2NO(g)+O2(g) 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:
①2NO(g) N2O2(g) 快 ΔH1<0
N2O2(g) 快 ΔH1<0
②N2O2(g)+O2(g) 2NO2(g) 慢 ΔH2<0
2NO2(g) 慢 ΔH2<0
反应2NO(g)+O2(g) 2NO2(g)的∆H=
2NO2(g)的∆H=__ (用含∆H1和∆H2的式子表示)。反应①的活化能E1与反应②的活化能E2的大小关系为E1__ E2(填“>”、“<”或“=”)。
(2)工业上常利用CH4来吸收CO2生成CO和H2,再用H2和CO合成甲醇。如在恒容密闭容器中通入物质的量浓度均为1.0mol·L-1的CH4与CO2,在一定条件下仅发生反应:CO2(g)+CH4(g) 2CO(g)+2H2(g),测得CH4的平衡转化率与温度及压强的关系如图1所示:
2CO(g)+2H2(g),测得CH4的平衡转化率与温度及压强的关系如图1所示:
则:①该反应的ΔH___ (填“<”“=”或“>”)0。
②压强p1、p2、p3、p4由大到小的关系为___ 。判断的理由是______ 。压强为p4时,在b点:v(正)___ (填“<”“=”或“>”)v(逆)。

③对于气相反应,用某组分(B)的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数(记作Kp),当p4=0.36MPa,则a点的平衡常数Kp=___ (保留3位有效数字,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
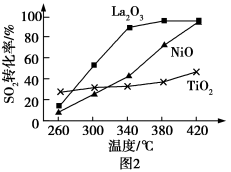
(3)燃煤烟气中硫的回收反应为2CO(g)+SO2(g)=2CO2(g)+S(l)。在其他条件相同、催化剂不同时,硫的回收反应中SO2的转化率随反应温度的变化如图2所示。260℃时,____ (填“La2O3”NiO”或“TiO2”)的催化效率最高。La2O3和NiO作催化剂均可能使SO2的转化率达到很高,不考虑价格因素,选择La2O3的主要优点是__ 。
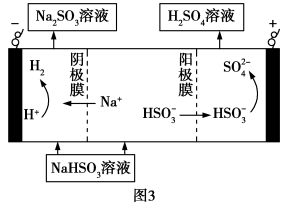
(4)该小组用Na2SO3溶液充分吸收SO2得到NaHSO3溶液,然后电解该溶液制得了硫酸。原理如图3,写出开始电解时阳极的电极反应式__ 。
(1)2NO(g)+O2(g)
 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:①2NO(g)
 N2O2(g) 快 ΔH1<0
N2O2(g) 快 ΔH1<0②N2O2(g)+O2(g)
 2NO2(g) 慢 ΔH2<0
2NO2(g) 慢 ΔH2<0反应2NO(g)+O2(g)
 2NO2(g)的∆H=
2NO2(g)的∆H=(2)工业上常利用CH4来吸收CO2生成CO和H2,再用H2和CO合成甲醇。如在恒容密闭容器中通入物质的量浓度均为1.0mol·L-1的CH4与CO2,在一定条件下仅发生反应:CO2(g)+CH4(g)
 2CO(g)+2H2(g),测得CH4的平衡转化率与温度及压强的关系如图1所示:
2CO(g)+2H2(g),测得CH4的平衡转化率与温度及压强的关系如图1所示:则:①该反应的ΔH
②压强p1、p2、p3、p4由大到小的关系为


③对于气相反应,用某组分(B)的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数(记作Kp),当p4=0.36MPa,则a点的平衡常数Kp=
(3)燃煤烟气中硫的回收反应为2CO(g)+SO2(g)=2CO2(g)+S(l)。在其他条件相同、催化剂不同时,硫的回收反应中SO2的转化率随反应温度的变化如图2所示。260℃时,
(4)该小组用Na2SO3溶液充分吸收SO2得到NaHSO3溶液,然后电解该溶液制得了硫酸。原理如图3,写出开始电解时阳极的电极反应式

您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐1】(1)如图是1mol NO2(g)和1mol CO(g)反应生成CO2和NO过程中的能量变化示意图,已知E1=+134kJ·mol-1、E2=+368kJ·mol-1, 若在反应体系中加入催化剂,反应速率增大,E1的变化是________ (填“增大”“减小”或“不变”,下同),ΔH的变化是________ 。请写出NO2和CO反应的热化学方程式:________ 。

(2)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。
已知:
a: 2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-159.5kJ·mol-1
b: NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH=+116.5kJ·mol-1
c: H2O(l)=H2O(g) ΔH=+44.0kJ·mol-1
①对于a反应来说,________ (填“高温”“低温”或“无影响”)更有利于该反应的自发。
②写出CO2与NH3合成尿素和液态水的热化学反应方程式:________ 。

(2)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。
已知:
a: 2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-159.5kJ·mol-1
b: NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH=+116.5kJ·mol-1
c: H2O(l)=H2O(g) ΔH=+44.0kJ·mol-1
①对于a反应来说,
②写出CO2与NH3合成尿素和液态水的热化学反应方程式:
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
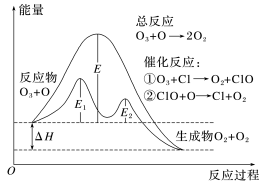
【推荐2】臭氧层中O3分解过程如图所示,回答下列问题。________ (填“>”或“<”)0。
(2)催化反应①是________ (填“吸热”或“放热”,下同)反应,催化反应②是________ 反应。
(3)总反应的活化能是________ ,催化反应①的活化能是________ ,催化反应②对应的逆反应的活化能是___________ ,总反应对应的逆反应活化能为_________ 。
(2)催化反应①是
(3)总反应的活化能是
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐3】氨是氮循环过程中的重要物质,氨的合成是目前普遍使用的人工固氮方法。
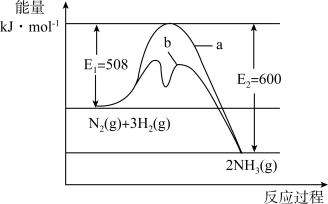
(1)根据图提供的信息,写出该反应的热化学方程式___________ ,在图中曲线___________ (填“a”或“b”)表示加入铁触媒的能量变化曲线,判断理由是___________ 。
(2)在恒容容器中,下列描述中能说明上述反应已达平衡的是___________
(3)一定温度下,向2 L密闭容器中充入1 mol N2和3 mol H2,保持体积不变,0.5 min后达到平衡,测得容器中有0.4 mol NH3,则平均反应速率v(N2)=___________ ,该温度下的平衡常数K=___________ 。(小数点后保留3位有效数字)
(4)保持温度和体积不变,向上述平衡体系中再加入1 mol N2、1 mol H2 、1 mol NH3 后该反应的速率大小关系为v正___________ v逆(填“大于”、“小于”或“等于”)。

(1)根据图提供的信息,写出该反应的热化学方程式
(2)在恒容容器中,下列描述中能说明上述反应已达平衡的是___________
| A.3v(H2)正=2v(NH3)逆 |
| B.单位时间内生成n mol N2的同时生成2n mol NH3 |
| C.混合气体的密度不再改变 |
| D.容器内压强不随时间的变化而变化 |
(3)一定温度下,向2 L密闭容器中充入1 mol N2和3 mol H2,保持体积不变,0.5 min后达到平衡,测得容器中有0.4 mol NH3,则平均反应速率v(N2)=
(4)保持温度和体积不变,向上述平衡体系中再加入1 mol N2、1 mol H2 、1 mol NH3 后该反应的速率大小关系为v正
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐1】臭氧层中O3分解过程如图所示,回答下列问题。________ (填“>”或“<”)0。
(2)催化反应①是________ (填“吸热”或“放热”,下同)反应,催化反应②是________ 反应。
(3)总反应的活化能是________ ,催化反应①的活化能是________ ,催化反应②对应的逆反应的活化能是___________ ,总反应对应的逆反应活化能为_________ 。

(2)催化反应①是
(3)总反应的活化能是
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】我国学者分别使用Fe2O3和Fe3O4作催化剂对燃煤烟气脱硝脱硫进行了研究。
(1)催化剂制备。在60~100℃条件下,向足量NaOH溶液中通入N2一段时间,再加入适量新制FeSO4溶液,充分反应后得到混合物X;向混合物X中加入NaNO3溶液,充分反应后经磁铁吸附、洗涤、真空干燥,制得Fe3O4催化剂。
①通入N2的目的是___ 。
②混合物X与NaNO3反应生成Fe3O4和NH3,该反应的化学方程式为___ 。
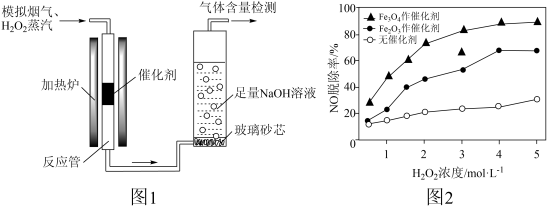
(2)催化剂性能研究。如图1所示,当其他条件一定时,分别在无催化剂、Fe2O3作催化剂、Fe3O4作催化剂的条件下,测定H2O2浓度对模拟烟气(含一定比例的NO、SO2、O2、N2)中NO和SO2脱除率的影响,NO脱除率与H2O2浓度的关系如图2所示。
反应Ⅰ:Fe3++H2O2=Fe2++•OOH+H+(慢反应)
反应Ⅱ:Fe2++H2O2=Fe3++•OH+OH-(快反应)
①与Fe2O3作催化剂相比,相同条件下Fe3O4作催化剂时NO脱除率更高,其原因是___ 。
②NO部分被氧化成NO2。NO2被NaOH溶液吸收生成两种含氧酸钠盐,该反应的离子方程式为___ 。
③实验表明•OH氧化SO2的速率比氧化NO速率慢。但在无催化剂、Fe2O3作催化剂、Fe3O4作催化剂的条件下,测得SO2脱除率几乎均为100%的原因是___ 。
(1)催化剂制备。在60~100℃条件下,向足量NaOH溶液中通入N2一段时间,再加入适量新制FeSO4溶液,充分反应后得到混合物X;向混合物X中加入NaNO3溶液,充分反应后经磁铁吸附、洗涤、真空干燥,制得Fe3O4催化剂。
①通入N2的目的是
②混合物X与NaNO3反应生成Fe3O4和NH3,该反应的化学方程式为
(2)催化剂性能研究。如图1所示,当其他条件一定时,分别在无催化剂、Fe2O3作催化剂、Fe3O4作催化剂的条件下,测定H2O2浓度对模拟烟气(含一定比例的NO、SO2、O2、N2)中NO和SO2脱除率的影响,NO脱除率与H2O2浓度的关系如图2所示。
反应Ⅰ:Fe3++H2O2=Fe2++•OOH+H+(慢反应)
反应Ⅱ:Fe2++H2O2=Fe3++•OH+OH-(快反应)
①与Fe2O3作催化剂相比,相同条件下Fe3O4作催化剂时NO脱除率更高,其原因是
②NO部分被氧化成NO2。NO2被NaOH溶液吸收生成两种含氧酸钠盐,该反应的离子方程式为
③实验表明•OH氧化SO2的速率比氧化NO速率慢。但在无催化剂、Fe2O3作催化剂、Fe3O4作催化剂的条件下,测得SO2脱除率几乎均为100%的原因是
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】反应A(g)+B(g) C(g)+D(g)过程中的能量变化如图所示,回答下列问题:
C(g)+D(g)过程中的能量变化如图所示,回答下列问题:
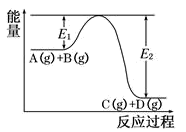
(1)该反应是________ 反应(填“吸热”“放热”)。
(2)反应体系中加入催化剂对反应热是否有影响?__________ 。
(3)在反应体系中加入催化剂,反应速率增大,E1的变化是:E1_________ (填“增大”“减小”“不变”)。
(4)由氢气和氧气反应生成1mol水蒸气放热241.8kJ·mol-1,写出其热化学方程式:____________ 。
(5)反应3Fe(s)+4H2O(g) Fe3O4+4H2(g),在一可变的容积的密闭容器中进行。
Fe3O4+4H2(g),在一可变的容积的密闭容器中进行。
①增加Fe的量, 其正反应速率的变化是_______ (填“增大”、“不变”或“减小”,以下相同)。
②保持体积不变,充入N2使体系压强增大,其正反应速率_______ 。
③保持压强不变,充入N2使容器的体积增大,逆反应速率_______ 。
 C(g)+D(g)过程中的能量变化如图所示,回答下列问题:
C(g)+D(g)过程中的能量变化如图所示,回答下列问题:
(1)该反应是
(2)反应体系中加入催化剂对反应热是否有影响?
(3)在反应体系中加入催化剂,反应速率增大,E1的变化是:E1
(4)由氢气和氧气反应生成1mol水蒸气放热241.8kJ·mol-1,写出其热化学方程式:
(5)反应3Fe(s)+4H2O(g)
 Fe3O4+4H2(g),在一可变的容积的密闭容器中进行。
Fe3O4+4H2(g),在一可变的容积的密闭容器中进行。①增加Fe的量, 其正反应速率的变化是
②保持体积不变,充入N2使体系压强增大,其正反应速率
③保持压强不变,充入N2使容器的体积增大,逆反应速率
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐1】化学家德海韦西溶解了诺贝尔金质奖章,躲过了纳粹的搜捕。我们知道金不易被硝酸氧化,但在浓硝酸中加入浓盐酸配成王水溶液后,金就容易被硝酸氧化生成相应的配合物,德海韦西就是用了这个方法。
已知:①Au(s)+ (aq)+4H+(aq)
(aq)+4H+(aq) Au3+(aq)+NO(aq)+2H2O(aq) ΔH1=+akJ/mol
Au3+(aq)+NO(aq)+2H2O(aq) ΔH1=+akJ/mol
②Au3+(aq)+4Cl-(aq) [AuCl4]-(aq) ΔH2=-bkJ/mol
[AuCl4]-(aq) ΔH2=-bkJ/mol
③Au(s)+ (aq)+4H+(aq)+4Cl-(aq)
(aq)+4H+(aq)+4Cl-(aq) [AuCl4]-(aq)+NO(aq)+2H2O(aq) ΔH3
[AuCl4]-(aq)+NO(aq)+2H2O(aq) ΔH3
上述a、b均大于0,回答下列问题:
(1)从平衡移动和能量的角度,说明为什么加入盐酸后Au易被硝酸氧化_____ 。
(2)写出反应②的平衡常数的表达式_____ 。
(3)下列哪些操作可以加快金在王水中的溶解速率_____ 。
已知:①Au(s)+
 (aq)+4H+(aq)
(aq)+4H+(aq) Au3+(aq)+NO(aq)+2H2O(aq) ΔH1=+akJ/mol
Au3+(aq)+NO(aq)+2H2O(aq) ΔH1=+akJ/mol②Au3+(aq)+4Cl-(aq)
 [AuCl4]-(aq) ΔH2=-bkJ/mol
[AuCl4]-(aq) ΔH2=-bkJ/mol③Au(s)+
 (aq)+4H+(aq)+4Cl-(aq)
(aq)+4H+(aq)+4Cl-(aq) [AuCl4]-(aq)+NO(aq)+2H2O(aq) ΔH3
[AuCl4]-(aq)+NO(aq)+2H2O(aq) ΔH3上述a、b均大于0,回答下列问题:
(1)从平衡移动和能量的角度,说明为什么加入盐酸后Au易被硝酸氧化
(2)写出反应②的平衡常数的表达式
(3)下列哪些操作可以加快金在王水中的溶解速率
| A.升高温度 | B.适当提高硝酸浓度 | C.增大溶液的pH | D.投入金块 |
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐2】含碳化合物在国民经济有着重要的作用。
(1)甲烷是一种重要的化工原料和清洁能源,研究其相关反应并合理利用具重要意义。
①已知:a.工业上甲烷可用于制造合成气,常温常压下其反应为CH4(g)+ H2O(l)=CO(g) +3H2(g) △H= +250.1 kJ∙mol−1
b. CO(g)、H2(g)的燃烧热依次为283.0 kJ∙mol−1、285.8 kJ∙mol−1
常温常压下8 g甲烷完全燃烧生成液态水时放出的热量为_______ kJ;
②在一密闭容器中充入H2S和CH4,且n(H2S):n(CH4)=2:1,发生反应:CH4(g)+ 2H2S(g)=CS2(g) +4H2(g)。 0.11MPa时,温度变化对平衡时产物的物质的量分数的影响如图所示:
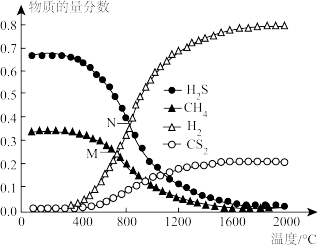
为提高H2S的平衡转化率,除改变温度外,还可采取的措施是_______ (列举一条)。N点对应温度下,该反应的Kp=_______ (MPa)2(Kp为以分压表示的平衡常数)。
(2)甲酸被认为是理想的氢能载体,我国科技工作者运用DFT计算研究单分子HCOOH在催化剂表面分解产生H2的反应历程如图所示,其中吸附在催化剂表面的物种用※标注。
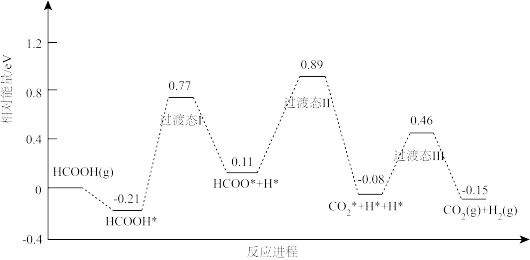
回答下列问题:
①该历程中决定正反应速率步骤的能垒(活化能)E正=_______ eV,该步骤的反应方程式为_______
②该历程甲酸分解制氢气的热化学方程式为_______ 。
③甲酸作为直接燃料电池的燃料具有能量密度高的优点。若电解质溶液显酸性,甲酸直接燃料电池的负极反应式为_______ ,该电池的理论输出电压为2.30V,能量密度E=_______ kW·h/kg(能量密度=电池输出电能/燃料质量,1kW·h=3.6×106J)
(1)甲烷是一种重要的化工原料和清洁能源,研究其相关反应并合理利用具重要意义。
①已知:a.工业上甲烷可用于制造合成气,常温常压下其反应为CH4(g)+ H2O(l)=CO(g) +3H2(g) △H= +250.1 kJ∙mol−1
b. CO(g)、H2(g)的燃烧热依次为283.0 kJ∙mol−1、285.8 kJ∙mol−1
常温常压下8 g甲烷完全燃烧生成液态水时放出的热量为
②在一密闭容器中充入H2S和CH4,且n(H2S):n(CH4)=2:1,发生反应:CH4(g)+ 2H2S(g)=CS2(g) +4H2(g)。 0.11MPa时,温度变化对平衡时产物的物质的量分数的影响如图所示:

为提高H2S的平衡转化率,除改变温度外,还可采取的措施是
(2)甲酸被认为是理想的氢能载体,我国科技工作者运用DFT计算研究单分子HCOOH在催化剂表面分解产生H2的反应历程如图所示,其中吸附在催化剂表面的物种用※标注。

回答下列问题:
①该历程中决定正反应速率步骤的能垒(活化能)E正=
②该历程甲酸分解制氢气的热化学方程式为
③甲酸作为直接燃料电池的燃料具有能量密度高的优点。若电解质溶液显酸性,甲酸直接燃料电池的负极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】2018年是合成氨工业先驱哈珀获得诺贝尔奖100周年,合成氨工业对化学工业和国防工业具有重要意义。
I.N2和H2生成NH3的反应为: N2(g)+
N2(g)+ H2(g)
H2(g) NH3(g) ΔH(298K)=-46.2kJ·mol-1, 在Fe催化剂作用下的反应历程如下(*表示吸附态)
NH3(g) ΔH(298K)=-46.2kJ·mol-1, 在Fe催化剂作用下的反应历程如下(*表示吸附态)
化学吸附:N2(g)→2N* , H2(g)→2H*
表面反应:N*+H*→NH* ,NH*+H*→NH2 * ,NH2 *+H*→NH3*
脱附: NH3* NH3(g)
NH3(g)
其中,N2的吸附分解反应活化能高、速率慢,决定合成氨的整体反应速率
(1)利于提高合成氨平衡产率的条件有_______ 。
A.高温 B.低温 C.低压 D.高压 E.催化剂
(2)实际生产中常用工艺条件:Fe作催化剂。控制温度773K,压强3.0×107Pa,原料气中N2和H2物质的量之比为1:2.8。
①分析说明原料气中N2过量的理由(任写一条)_______ 。
②关于合成氨工艺的下列理解,正确的是_______ (填选项字母)。
A.合成氨反应在不同温度下的ΔH和ΔS都小于零
B.当温度、压强一定时,在原料气(N2和H2的比例不变)中添加少量惰性气体,有利于提高平衡转化率
C.迅速冷却可将NH3液化,不断将液态氨移去,有利于反应正向进行
D.分离空气可得到N2,通过天然气和水蒸气转化可得H2,原料气须经过净化处理,以防止催化剂中毒和安全事故发生
II.工业合成氨生产示意图如图所示:
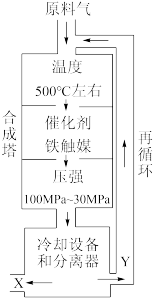
(3)X的化学式为_______ 。
(4)图中条件选定的主要原因是_______ (填字母)。
A.温度、压强对化学平衡的影响
B.铁触媒在该温度时活性大
C.工业生产受动力、材料、设备等条件的限制
(5)当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和 NH3的量),反应速率与时间的关系如图所示。图中t1时引起平衡移动的条件可能是_______ 。其中表示平衡混合物中NH3的含量最高的一段时间是_______ (填字母)。
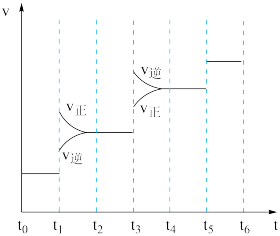
A.0~t1 B.t2~t3 C.t4~t5 D.t5~t6
I.N2和H2生成NH3的反应为:
 N2(g)+
N2(g)+ H2(g)
H2(g) NH3(g) ΔH(298K)=-46.2kJ·mol-1, 在Fe催化剂作用下的反应历程如下(*表示吸附态)
NH3(g) ΔH(298K)=-46.2kJ·mol-1, 在Fe催化剂作用下的反应历程如下(*表示吸附态)化学吸附:N2(g)→2N* , H2(g)→2H*
表面反应:N*+H*→NH* ,NH*+H*→NH2 * ,NH2 *+H*→NH3*
脱附: NH3*
 NH3(g)
NH3(g)其中,N2的吸附分解反应活化能高、速率慢,决定合成氨的整体反应速率
(1)利于提高合成氨平衡产率的条件有
A.高温 B.低温 C.低压 D.高压 E.催化剂
(2)实际生产中常用工艺条件:Fe作催化剂。控制温度773K,压强3.0×107Pa,原料气中N2和H2物质的量之比为1:2.8。
①分析说明原料气中N2过量的理由(任写一条)
②关于合成氨工艺的下列理解,正确的是
A.合成氨反应在不同温度下的ΔH和ΔS都小于零
B.当温度、压强一定时,在原料气(N2和H2的比例不变)中添加少量惰性气体,有利于提高平衡转化率
C.迅速冷却可将NH3液化,不断将液态氨移去,有利于反应正向进行
D.分离空气可得到N2,通过天然气和水蒸气转化可得H2,原料气须经过净化处理,以防止催化剂中毒和安全事故发生
II.工业合成氨生产示意图如图所示:

(3)X的化学式为
(4)图中条件选定的主要原因是
A.温度、压强对化学平衡的影响
B.铁触媒在该温度时活性大
C.工业生产受动力、材料、设备等条件的限制
(5)当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和 NH3的量),反应速率与时间的关系如图所示。图中t1时引起平衡移动的条件可能是

A.0~t1 B.t2~t3 C.t4~t5 D.t5~t6
您最近一年使用:0次



