解题方法
1 . I.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
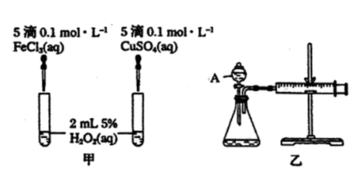
(1)定性分析:如图甲可通过观察___ 的快慢,定性比较得出结论。有同学提出将FeCl3改为0. 05mol·L-1 Fe2 (SO4)3更为合理,其理由是_____ 。
(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是____ 。
II.某温度时,在一个2L的密闭容器中,A、B、C三种气体物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
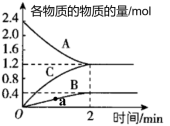
(1)该反应的化学方程式为____ ;
(2)从开始至2min,A的平均反应速率为____ ;在图中a点处:υ正(B) _____ υ逆(B)(填 “大于”“小于”或“等于”)。
(3)下列叙述能说明该反应已达到化学平衡状态的是_______ (填序号);
A.A、B、C的物质的量之比为3:1:3
B.相同时间内消耗3molA,同时生成3molC
C.υ正(A)=2υ逆(B)
D. 混合气体的平均相对分子质量不再改变的状态
E.B的体积分数不再发生变化
(4)在某一时刻采取下列措施能使该反应速率减小的是_______ (填序号)。
A.加催化剂 B.降低温度
C.容积不变,充入A D.容积不变,从容器中分离出A

(1)定性分析:如图甲可通过观察
(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是
II.某温度时,在一个2L的密闭容器中,A、B、C三种气体物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

(1)该反应的化学方程式为
(2)从开始至2min,A的平均反应速率为
(3)下列叙述能说明该反应已达到化学平衡状态的是
A.A、B、C的物质的量之比为3:1:3
B.相同时间内消耗3molA,同时生成3molC
C.υ正(A)=2υ逆(B)
D. 混合气体的平均相对分子质量不再改变的状态
E.B的体积分数不再发生变化
(4)在某一时刻采取下列措施能使该反应速率减小的是
A.加催化剂 B.降低温度
C.容积不变,充入A D.容积不变,从容器中分离出A
您最近一年使用:0次
名校
2 . 下列有关化学反应速率和限度的说法中,不正确的是
| A.“新冠疫苗”一般应冷藏存放,可降低蛋白质变性的反应速率 |
B.2SO2+O2 2SO3反应中加入18O2,达到平衡后SO2中不可能有18O 2SO3反应中加入18O2,达到平衡后SO2中不可能有18O |
| C.实验室用H2O2分解制O2,加入MnO2作催化剂后,反应速率明显加快 |
| D.炼铁高炉尾气之谜告诉我们,“二氧化碳与焦炭生成一氧化碳”是一个可逆反应不能全部转化 |
您最近一年使用:0次
2021-05-07更新
|
173次组卷
|
2卷引用:山东省临沂市部分县区2020-2021学年高一下学期期中考试化学试题
名校
3 . 某可逆反应在体积为5L的密闭容器中进行,0~3min内各物质的物质的量的变化情况如图所示(A、B、C均为气体)。
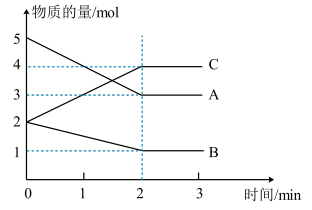
(1)该反应的化学方程式为___ 。
(2)反应开始至2min时,B的平均反应速率为___ 。
(3)能说明该反应已达到平衡状态的是___ (填字母)。
A.v(A)=2v(B)
B.容器内压强保持不变
C.2v逆(A)=v正(B)
D.容器内混合气体的密度保持不变
(4)在密闭容器里,通入amolA(g)、bmolB(g)、cmolC(g),发生上述反应,当改变下列条件时,反应速率会减小的是___ (填序号)。
①降低温度 ②加入催化剂(正) ③增大容器容积

(1)该反应的化学方程式为
(2)反应开始至2min时,B的平均反应速率为
(3)能说明该反应已达到平衡状态的是
A.v(A)=2v(B)
B.容器内压强保持不变
C.2v逆(A)=v正(B)
D.容器内混合气体的密度保持不变
(4)在密闭容器里,通入amolA(g)、bmolB(g)、cmolC(g),发生上述反应,当改变下列条件时,反应速率会减小的是
①降低温度 ②加入催化剂(正) ③增大容器容积
您最近一年使用:0次
2021-04-28更新
|
284次组卷
|
4卷引用:山东省菏泽思源学校2019-2020学年高一下学期6月月考化学试题
名校
4 . 为探究 对
对 分解是否有催化作用,分别取10mL 30%
分解是否有催化作用,分别取10mL 30% (约10
(约10 )于四支试管中,控制其它条件相同,进行实验获得如下表数据(氧气为标准状况下的体积):
)于四支试管中,控制其它条件相同,进行实验获得如下表数据(氧气为标准状况下的体积):
下列有关说法不正确的是
 对
对 分解是否有催化作用,分别取10mL 30%
分解是否有催化作用,分别取10mL 30% (约10
(约10 )于四支试管中,控制其它条件相同,进行实验获得如下表数据(氧气为标准状况下的体积):
)于四支试管中,控制其它条件相同,进行实验获得如下表数据(氧气为标准状况下的体积):| 实验编号 | 所加药品 | 控制温度/℃ | 生成氧气平均速率( ) ) | ||
| 第1个3min | 第2个3min | 第3个3min | |||
| ① | 1mL 1.0  | 20 | 2.4 | 2.7 | 2.8 |
| ② | 30 | 9 | 10 | 10 | |
| ③ | 40 | 90 | 63 | 28 | |
| ④ | 1mL  | 40 | 1.0 | 1.2 | 1.3 |
A. 对 对 分解有催化作用 分解有催化作用 |
B. 对 对 分解催化效率可能随温度升高而提高 分解催化效率可能随温度升高而提高 |
C.实验③第1个3min  的平均反应速率约为 的平均反应速率约为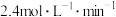 |
D.为得到更可靠的结论,实验①②③还需排除 |
您最近一年使用:0次
2021-04-23更新
|
600次组卷
|
10卷引用:山东省济宁市邹城二中2020-2021学年高一下学期6月月考化学试题
山东省济宁市邹城二中2020-2021学年高一下学期6月月考化学试题(已下线)2021年高考化学押题预测卷(山东卷)02(含考试版、答题卡、参考答案、全解全析)(已下线)押山东卷第14题 化学反应速率和平衡-备战2021年高考化学临考题号押题(山东卷)广东省梅州兴宁市沐彬中学2021-2022学年高一下学期 3月月考化学试题浙江省稽阳联谊学校2021届高三4月联考化学试题(已下线)【浙江新东方】高中化学20210621-010【2021】【高三下】(已下线)2021年秋季高三化学开学摸底考试卷01(浙江专用)(已下线)课时35 化学反应速率及影响因素-2022年高考化学一轮复习小题多维练(全国通用)(已下线)专题21 化学反应速率(热点讲义)-2022年高三毕业班化学常考点归纳与变式演练(已下线)三轮冲刺卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(浙江专用)
名校
5 . 控制变量思想在探究实验中有重要应用,下列实验对影响化学反应速率的因素进行探究。
Ⅰ.催化剂对速率的影响
探究Fe3+和Cu2+对H2O2分解的催化效果:在两支试管中各加入2 mL 5%的H2O2溶液,再向其中分别滴入1 mL浓度均为0.1 mol·L-1 的FeCl3溶液和CuSO4溶液。
(1)H2O2分解的化学方程式是_____ 。
(2)有同学建议将CuSO4改为CuCl2溶液,理由是______ ;还有同学认为即使改用了 CuCl2溶液,仍不严谨,建议补做对比实验:向2 mL 5%的H2O2溶液中滴入的试剂及其用量是____ 。
Ⅱ.浓度对速率的影响
实验方案:混合试剂1和试剂2,记录溶液褪色所需的时间。
(3)配平下列化学方程式:
____ KMnO4+____ H2C2O4+____ =____ K2SO4+____ MnSO4+____ CO2↑+____ H2O
(4)实验1中t min 时溶液褪色,用草酸表示的反应速率v(H2C2O4)=___ mol·L-1· min-1。
联系实验1、2,预期结论是_________ 。
(5)n(CO2)随时间的变化如下图1所示,其变化的原因是________ 。

(6)研究发现KMnO4溶液的酸化程度对反应的速率也有较大影响,用不同浓度的硫酸进行酸化,其余条件均相同时,测得反应溶液的透光率(溶液颜色越浅,透光率越高)随时间变化如图2所示,由此得出的结论是_______ 。
Ⅰ.催化剂对速率的影响
探究Fe3+和Cu2+对H2O2分解的催化效果:在两支试管中各加入2 mL 5%的H2O2溶液,再向其中分别滴入1 mL浓度均为0.1 mol·L-1 的FeCl3溶液和CuSO4溶液。
(1)H2O2分解的化学方程式是
(2)有同学建议将CuSO4改为CuCl2溶液,理由是
Ⅱ.浓度对速率的影响
实验方案:混合试剂1和试剂2,记录溶液褪色所需的时间。
| 实验1 | 实验2 | |
| 试剂1 | 2 mL 0.1mol·L-1的草酸溶液 | 2 mL 0.2mol·L-1的草酸溶液 |
| 试剂2 | 4 mL 0.01 mol·L-1的高锰酸钾酸性溶液 | 4 mL 0.01 mol·L-1的高锰酸钾酸性溶液 |
(3)配平下列化学方程式:
(4)实验1中t min 时溶液褪色,用草酸表示的反应速率v(H2C2O4)=
联系实验1、2,预期结论是
(5)n(CO2)随时间的变化如下图1所示,其变化的原因是

(6)研究发现KMnO4溶液的酸化程度对反应的速率也有较大影响,用不同浓度的硫酸进行酸化,其余条件均相同时,测得反应溶液的透光率(溶液颜色越浅,透光率越高)随时间变化如图2所示,由此得出的结论是
您最近一年使用:0次
2020-11-16更新
|
374次组卷
|
3卷引用:山东省烟台市第二中学2021-2022学年高一下学期4月月考化学试题
名校
解题方法
6 . 2SO2(g)+O2(g)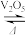 2SO3(g)是制备硫酸的重要反应。下列叙述
2SO3(g)是制备硫酸的重要反应。下列叙述不正确 的是
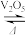 2SO3(g)是制备硫酸的重要反应。下列叙述
2SO3(g)是制备硫酸的重要反应。下列叙述| A.催化剂V2O5不改变该反应的逆反应速率 |
| B.若该反应在恒温恒容体系中进行,充入氦气正反应速率保持不变 |
| C.该反应是放热反应,升高温度将缩短反应达到平衡的时间 |
D.在t1、t2时刻,SO3(g)的浓度分别是c1、c2,则时间间隔t1~t2内,SO3(g)生成的平均速率为v=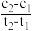 |
您最近一年使用:0次
名校
解题方法
7 . 2SO2(g)+O2(g) 2SO3(g)是制备硫酸的重要反应。下列叙述正确的是
2SO3(g)是制备硫酸的重要反应。下列叙述正确的是
 2SO3(g)是制备硫酸的重要反应。下列叙述正确的是
2SO3(g)是制备硫酸的重要反应。下列叙述正确的是| A.催化剂V2O5不改变该反应的逆反应速率 |
B.在t1、t2时刻,SO3(g)的浓度分别是c1,c2,则时间间隔t1~t2内,SO3(g)生成的平均速率为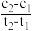 |
| C.该反应是放热反应,降低温度将缩短反应达到平衡的时间 |
| D.增大容器体积,反应速率一定增大 |
您最近一年使用:0次
2020-08-26更新
|
81次组卷
|
2卷引用:山东省鄄城县第一中学2022-2023学年高一下学期5月月考化学试题
解题方法
8 . 下列各项中“操作或现象”能达到预期“实验目的”的是
| 选项 | 实验目的 | 操作或现象 |
| A | 检验碳与浓硫酸反应后的气体产物 | 将产生的气体依次通过无水 、澄清石灰水和品红溶液 、澄清石灰水和品红溶液 |
| B | 检验酸性条件下蔗糖水解产物中是否含有葡萄糖 | 向适量水解后的溶液中加入新制的 悬浊液,观察是否有砖红色沉淀生成 悬浊液,观察是否有砖红色沉淀生成 |
| C | 鉴别溴蒸气和 | 分别通入 溶液中,产生浅黄色沉淀的是溴蒸气 溶液中,产生浅黄色沉淀的是溴蒸气 |
| D | 探究 、 、 溶液对 溶液对 分解速率的影响 分解速率的影响 | 相同温度下,将少量 粉末和2滴 粉末和2滴 溶液分别加入到盛有 溶液分别加入到盛有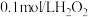 溶液和 溶液和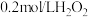 溶液的两支试管中 溶液的两支试管中 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . 速率与限度是研究化学反应的重要视角,下列叙述错误的是
A.对于反应 ,其他条件不变,增加木炭的量,反应速率不变 ,其他条件不变,增加木炭的量,反应速率不变 |
B.某物质化学反应速率为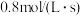 是指 是指 时该物质的浓度为 时该物质的浓度为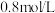 |
| C.氯酸钾分解制取氧气时添加少量二氧化锰,可增大反应速率 |
| D.在给定条件下,达到平衡时,可逆反应完成程度达到最大 |
您最近一年使用:0次
2020-08-11更新
|
813次组卷
|
10卷引用:山东省聊城市2019-2020学年高一下学期期末考试化学试题
山东省聊城市2019-2020学年高一下学期期末考试化学试题山东省泰安市第一中学2021-2022学年高一下学期期中考试(等级考)化学试题山东省实验中学2021届高三上学期第一次诊断考试化学试题山东省菏泽市2022-2023学年高二上学期期中考试(B)化学试题山东省蓬莱第二中学2021-2022学年高三上学期第一次月考化学试题浙江省宁波市五校2023-2024学年高一下学期4月期中联考化学试题湖南省长沙市雅礼中学2020-2021学年度高二上学期入学考试化学试题(已下线)第02章 化学反应的方向、限度与速率(B卷能力提升卷)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材鲁科版)(已下线)第二章 化学反应速率与化学平衡(基础过关)-2020-2021学年高二化学单元测试定心卷(人教版2019选择性必修一)甘肃省武威第一中学2020-2021学年高二上学期期中考试化学试题
解题方法
10 . 为探究影响化学反应速率的因素,某研究小组设计了如下五个实验。按要求回答下列问题 (已知:Cu2+、Fe3+对H2O2的分解起催化作用) 。
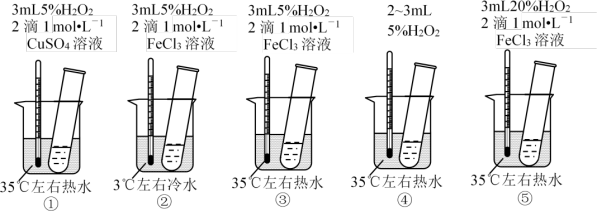
(1)为探究温度对化学反应速率的影响,应选择实验___________ (填序号,下同) ,选择的依据是_______________________ 。
(2)为探究催化剂对化学反应速率的影响,同时探究催化剂不同催化效果不同,应选择实验___________ 。
(3)通过观察发现实验⑤比实验③现象明显,其原因是____________________ 。
(4)根据上述实验,用H2O2快速制取少量O2,可采取的三条措施为___________ 。

(1)为探究温度对化学反应速率的影响,应选择实验
(2)为探究催化剂对化学反应速率的影响,同时探究催化剂不同催化效果不同,应选择实验
(3)通过观察发现实验⑤比实验③现象明显,其原因是
(4)根据上述实验,用H2O2快速制取少量O2,可采取的三条措施为
您最近一年使用:0次



