名校
解题方法
1 . 我国科研人员提出了由 和
和 转化为高附加值产品
转化为高附加值产品 的催化反应历程,该历程示意如下。则下列说法不正确的是
的催化反应历程,该历程示意如下。则下列说法不正确的是
 和
和 转化为高附加值产品
转化为高附加值产品 的催化反应历程,该历程示意如下。则下列说法不正确的是
的催化反应历程,该历程示意如下。则下列说法不正确的是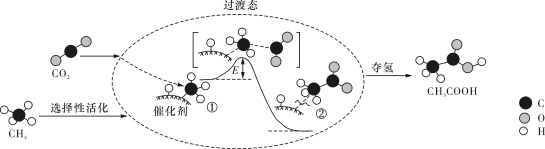
A.在 和 和 反应生成 反应生成 的总反应中,原子利用率为100% 的总反应中,原子利用率为100% |
B. 过程中,形成的键只有非极性共价键 过程中,形成的键只有非极性共价键 |
C. 过程中,有极性共价键发生断裂 过程中,有极性共价键发生断裂 |
D.①→②过程形成了 键 键 |
您最近一年使用:0次
2023-03-24更新
|
797次组卷
|
6卷引用:山东省淄博市部分学校联考2022-2023学年高一下学期4月期中考试化学试题
2 . 理论研究表明,在 和
和 下,
下, 异构化反应过程的能量变化如图所示。下列说法错误的是
异构化反应过程的能量变化如图所示。下列说法错误的是
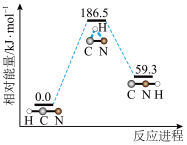
 和
和 下,
下, 异构化反应过程的能量变化如图所示。下列说法错误的是
异构化反应过程的能量变化如图所示。下列说法错误的是
A.该异构化反应的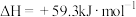 | B. 比 比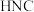 稳定 稳定 |
| C.使用催化剂,可以降低反应的反应热 | D.该异构化过程属于化学变化 |
您最近一年使用:0次
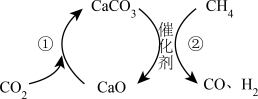
3 . 碳捕集技术是减少 排放的一种途径,下图所示可捕获和转化
排放的一种途径,下图所示可捕获和转化 ,减少排放并实现资源利用。反应①完成之后通入
,减少排放并实现资源利用。反应①完成之后通入 ,反应过程中在催化剂上有积碳。下列说法错误的是
,反应过程中在催化剂上有积碳。下列说法错误的是
 排放的一种途径,下图所示可捕获和转化
排放的一种途径,下图所示可捕获和转化 ,减少排放并实现资源利用。反应①完成之后通入
,减少排放并实现资源利用。反应①完成之后通入 ,反应过程中在催化剂上有积碳。下列说法错误的是
,反应过程中在催化剂上有积碳。下列说法错误的是
| A.反应①属于化合反应 |
| B.反应过程中需添加CaO |
C.反应②的化学方程式为 |
D.反应②过程中可能有反应 发生 发生 |
您最近一年使用:0次
2022-11-13更新
|
156次组卷
|
2卷引用:山东省日照市2022-2023学年高一上学期期中校际联考化学试题
解题方法
4 . 某化学课外兴趣小组探究过氧化钠与水的反应,探究过程如下:
(1)实验1:向包有过氧化钠粉末的脱脂棉上滴水,脱脂棉燃烧起来。请分析脱脂棉燃烧的原因_______ 。
(2)实验2:取一支试管,向其中加入少量过氧化钠固体,然后加入少量蒸馏水,有气泡冒出,充分振荡后再滴入酚酞试液,溶液先变红后褪色。
提出问题:溶液为什么先变红,过了一会,红色又褪去了呢?
猜想:甲同学认为是氢氧化钠溶液与空气中的二氧化碳反应的缘故,乙同学认为甲同学的猜想不正确,理由是碳酸钠溶液显碱性,也能使酚酞试液变红色。
查阅资料:
i.H2O2可以破坏酚酞的结构,使酚酞在碱性溶液中不能再显红色;
ii.NaOH溶液浓度过高,酚酞不变色或变色后迅速褪色。
设计实验方案:
①取少量褪色后的溶液于试管中,加入MnO2固体,若有气泡冒出,用_______ 检验该气体,则证明该反应过程中生成了_______ (填化学式)使溶液褪色。
②另取少量褪色后的溶液于试管中,加入蒸馏水稀释,若溶液变红,则证明溶液褪色原因可能为_______ 。
(3)为进一步探究过氧化钠与水反应的实质,运用pH传感器、温度传感器、氧气传感器等仪器进行实验探究,得到如下图象。
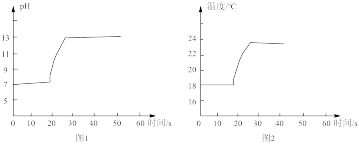
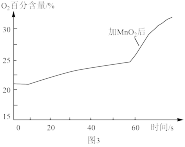
根据图象,得出结论:过氧化钠与水反应过程的方程式为_______ 、_______ 。
(1)实验1:向包有过氧化钠粉末的脱脂棉上滴水,脱脂棉燃烧起来。请分析脱脂棉燃烧的原因
(2)实验2:取一支试管,向其中加入少量过氧化钠固体,然后加入少量蒸馏水,有气泡冒出,充分振荡后再滴入酚酞试液,溶液先变红后褪色。
提出问题:溶液为什么先变红,过了一会,红色又褪去了呢?
猜想:甲同学认为是氢氧化钠溶液与空气中的二氧化碳反应的缘故,乙同学认为甲同学的猜想不正确,理由是碳酸钠溶液显碱性,也能使酚酞试液变红色。
查阅资料:
i.H2O2可以破坏酚酞的结构,使酚酞在碱性溶液中不能再显红色;
ii.NaOH溶液浓度过高,酚酞不变色或变色后迅速褪色。
设计实验方案:
①取少量褪色后的溶液于试管中,加入MnO2固体,若有气泡冒出,用
②另取少量褪色后的溶液于试管中,加入蒸馏水稀释,若溶液变红,则证明溶液褪色原因可能为
(3)为进一步探究过氧化钠与水反应的实质,运用pH传感器、温度传感器、氧气传感器等仪器进行实验探究,得到如下图象。


根据图象,得出结论:过氧化钠与水反应过程的方程式为
您最近一年使用:0次
名校
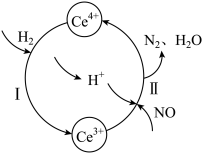
5 . 用还原法可以将硝酸厂烟气中的大量氮氧化物( )转化为无害物质。常温下,将NO与
)转化为无害物质。常温下,将NO与 的混合气体通入
的混合气体通入 与
与 的混合溶液中,其转化过程如图所示。下列说法不正确的是
的混合溶液中,其转化过程如图所示。下列说法不正确的是
 )转化为无害物质。常温下,将NO与
)转化为无害物质。常温下,将NO与 的混合气体通入
的混合气体通入 与
与 的混合溶液中,其转化过程如图所示。下列说法不正确的是
的混合溶液中,其转化过程如图所示。下列说法不正确的是
A.转化过程的总反应方程式为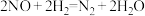 |
B.反应II中氧化剂与还原剂的个数之比为 |
C.转化反应前后混合溶液内 和 和 的总数一定保持不变 的总数一定保持不变 |
D. 是该转化反应的催化剂 是该转化反应的催化剂 |
您最近一年使用:0次
2022-09-15更新
|
349次组卷
|
3卷引用:山东省青岛第十五中学2023-2024学年高一上学期期中考试化学试卷
6 . 研究化学反应的快慢和限度在实际生产中具有重要意义。
I.取等物质的量浓度等体积 溶液分别进行下列实验,实验报告如下表所示。
溶液分别进行下列实验,实验报告如下表所示。
(1)实验1、2研究的是_______ 对 分解速率的影响。
分解速率的影响。
(2)实验2、3的目的是_______ 。
II.经研究知 对
对 分解也具有催化作用,为比较
分解也具有催化作用,为比较 和
和 对
对 分解的催化效果,某研究小组的同学分别设计了如图甲、乙所示的实验。
分解的催化效果,某研究小组的同学分别设计了如图甲、乙所示的实验。

(3)定性分析:如图甲可通过观察_______ ,定性比较得出结论。有同学提出将 改为
改为 更为合理,其理由是
更为合理,其理由是_______ 。
(4)定量分析:如图乙所示,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为_______ ,实验中需要测量的数据是_______ 。
III.现有试剂:① 溶液 ②
溶液 ②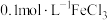 溶液 ③
溶液 ③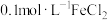 溶液
溶液
④ 盐酸 ⑤
盐酸 ⑤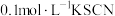 溶液 ⑥
溶液 ⑥
现以KI和 反应为例设计实验,探究此反应存在一定的限度。
反应为例设计实验,探究此反应存在一定的限度。
实验步骤如下:向 溶液中,滴加
溶液中,滴加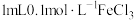 溶液;充分反应后,将溶液分成三份。
溶液;充分反应后,将溶液分成三份。
(5)取其中一份加试剂⑥,充分振荡后,下层是_______ 溶液,颜色为_______ 色。
(6)另取一份,加试剂_______ (填序号),现象是_______ ,说明此反应存在一定的限度。
I.取等物质的量浓度等体积
 溶液分别进行下列实验,实验报告如下表所示。
溶液分别进行下列实验,实验报告如下表所示。| 序号 | 条件 | 现象 | 结论 | |
| 温度/℃ | 催化剂 | |||
| 1 | 40 |  | ||
| 2 | 20 |  | ||
| 3 | 20 |  | ||
| 4 | 20 | 无 | ||
 分解速率的影响。
分解速率的影响。(2)实验2、3的目的是
II.经研究知
 对
对 分解也具有催化作用,为比较
分解也具有催化作用,为比较 和
和 对
对 分解的催化效果,某研究小组的同学分别设计了如图甲、乙所示的实验。
分解的催化效果,某研究小组的同学分别设计了如图甲、乙所示的实验。
(3)定性分析:如图甲可通过观察
 改为
改为 更为合理,其理由是
更为合理,其理由是(4)定量分析:如图乙所示,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为
III.现有试剂:①
 溶液 ②
溶液 ②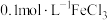 溶液 ③
溶液 ③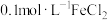 溶液
溶液④
 盐酸 ⑤
盐酸 ⑤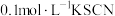 溶液 ⑥
溶液 ⑥
现以KI和
 反应为例设计实验,探究此反应存在一定的限度。
反应为例设计实验,探究此反应存在一定的限度。实验步骤如下:向
 溶液中,滴加
溶液中,滴加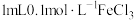 溶液;充分反应后,将溶液分成三份。
溶液;充分反应后,将溶液分成三份。(5)取其中一份加试剂⑥,充分振荡后,下层是
(6)另取一份,加试剂
您最近一年使用:0次
名校
7 . 碘及其化合物在生产生活中有重要作用。
(1)单质碘可与氢气反应生成碘化氢。将物质的量比为2:1的氢气和碘蒸气放入密闭容器中进行反应:H2(g)+I2(g) 2HI(g),反应经过5分钟测得碘化氢的浓度为 0.1 mol•L-1,碘蒸气的浓度为0.05mol•L-1。
2HI(g),反应经过5分钟测得碘化氢的浓度为 0.1 mol•L-1,碘蒸气的浓度为0.05mol•L-1。
①前5分钟平均反应速率 (H2) =
(H2) =___________ ,H2的初始浓度是___________ 。
②下列能说明反应已达平衡状态的是___________ (填序号)。
a. 混合体系总压强保持不变
b. 单位时间内断裂的H-H键数目与断裂的H-I键数目相等
c. c(H2):c(I2):c(HI) =1:1:2
d. 2 (I2)正=
(I2)正= (HI)逆
(HI)逆
e. 反应混合体系的颜色不再发生变化
(2)某小组同学在室温下进行“碘钟实验”:将浓度均为0.01 mol•L-1的H2O2、H2SO4、KI、Na2S2O3溶液及淀粉混合,一定时间后溶液变为蓝色。
已知:“碘钟实验”的总反应的离子方程式为H2O2 +2 +2H+ =
+2H+ =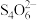 + 2H2O
+ 2H2O
反应分两步进行:
反应A: …… 反应B: I2+2 = 2I- +
= 2I- +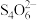
①反应A的离子方程式是___________ 。对于总反应,I-的作用是___________ 。
②为探究溶液变蓝快慢的影响因素,进行实验I、Ⅱ(溶液浓度均为0.0l mol•L-1)
溶液从混合时的无色变为蓝色的时间:实验I是30 min、实验II是40 min。实验II中,x、y、z所对应的数值分别是___________ 、___________ 、___________ ;对比实验I、II,可得出的实验结论是___________ 。
(1)单质碘可与氢气反应生成碘化氢。将物质的量比为2:1的氢气和碘蒸气放入密闭容器中进行反应:H2(g)+I2(g)
 2HI(g),反应经过5分钟测得碘化氢的浓度为 0.1 mol•L-1,碘蒸气的浓度为0.05mol•L-1。
2HI(g),反应经过5分钟测得碘化氢的浓度为 0.1 mol•L-1,碘蒸气的浓度为0.05mol•L-1。①前5分钟平均反应速率
 (H2) =
(H2) =②下列能说明反应已达平衡状态的是
a. 混合体系总压强保持不变
b. 单位时间内断裂的H-H键数目与断裂的H-I键数目相等
c. c(H2):c(I2):c(HI) =1:1:2
d. 2
 (I2)正=
(I2)正= (HI)逆
(HI)逆e. 反应混合体系的颜色不再发生变化
(2)某小组同学在室温下进行“碘钟实验”:将浓度均为0.01 mol•L-1的H2O2、H2SO4、KI、Na2S2O3溶液及淀粉混合,一定时间后溶液变为蓝色。
已知:“碘钟实验”的总反应的离子方程式为H2O2 +2
 +2H+ =
+2H+ =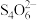 + 2H2O
+ 2H2O反应分两步进行:
反应A: …… 反应B: I2+2
 = 2I- +
= 2I- +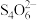
①反应A的离子方程式是
②为探究溶液变蓝快慢的影响因素,进行实验I、Ⅱ(溶液浓度均为0.0l mol•L-1)
| 用量试剂 | H2O2溶液 | H2SO4溶液 | Na2S2O3溶液 | KI溶液 (含淀粉) | H2O |
| 实验I | 5 | 4 | 8 | 3 | 0 |
| 实验II | 5 | 2 | x | y | z |
溶液从混合时的无色变为蓝色的时间:实验I是30 min、实验II是40 min。实验II中,x、y、z所对应的数值分别是
您最近一年使用:0次
解题方法
8 . 某种含铜的催化剂 可用于汽车尾气脱氮,催化机理如图所示。下列说法错误的是
可用于汽车尾气脱氮,催化机理如图所示。下列说法错误的是

 可用于汽车尾气脱氮,催化机理如图所示。下列说法错误的是
可用于汽车尾气脱氮,催化机理如图所示。下列说法错误的是
| A.该催化循环中Cu的化合价没有发生变化 |
| B.反应①→②不是氧化还原反应 |
C.总反应的化学方程式为 |
D.实验室模拟此过程时,可用浓氨水与碱石灰反应提供 |
您最近一年使用:0次
9 . 多相催化反应是反应物分子在催化剂表面通过吸附、解吸过程进行的反应。我国学者发现在T℃时,甲醇( )在铜基催化剂上的反应机理如下(该反应为可逆反应)
)在铜基催化剂上的反应机理如下(该反应为可逆反应)

下列说法正确的是
 )在铜基催化剂上的反应机理如下(该反应为可逆反应)
)在铜基催化剂上的反应机理如下(该反应为可逆反应)
下列说法正确的是
| A.过程Ⅰ是放热过程,过程Ⅱ是吸热过程 |
B.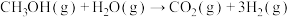 是热能转化为化学能的过程 是热能转化为化学能的过程 |
| C.铜基催化剂可以改变反应速率,但不参与反应 |
| D.CO(g)在反应中生成又消耗,CO(g)可认为是催化剂 |
您最近一年使用:0次
10 . 我国科学家使用双功能催化剂(能吸附不同粒子)催化水煤气变换反应:
 ,反应过程示意图如下:
,反应过程示意图如下:
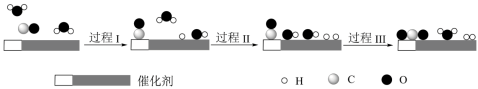
下列说法错误的是

 ,反应过程示意图如下:
,反应过程示意图如下:
下列说法错误的是
| A.过程I、过程II均为吸热过程 |
| B.使用催化剂提高了该反应的反应速率 |
C.该反应中,CO(g)和 的总能量高于 的总能量高于 和 和 的总能量 的总能量 |
D.示意图中:起始时的2个 在反应过程中并未都参与了反应 在反应过程中并未都参与了反应 |
您最近一年使用:0次
2022-07-14更新
|
369次组卷
|
3卷引用:山东省菏泽市2021-2022学年高一下学期期末教学质量检测化学试题



