1 . 我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程,如图所示。
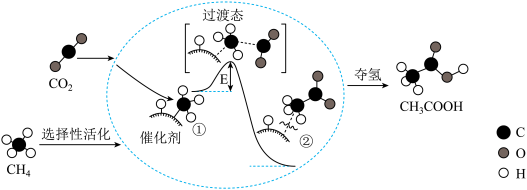
下列说法错误的是

下列说法错误的是
| A.催化剂参加了化学反应过程 |
| B.CH4→CH3COOH反应过程中,有C-H键的断裂和形成 |
| C.①→②过程中,放出能量并形成了C-C键 |
| D.生成CH3COOH总反应的类型是加成反应 |
您最近一年使用:0次
解题方法
2 . 环状碳酸酯广泛用作极性非质子溶剂、电池的离子导体等,某研究团队以环氧乙烷衍生物(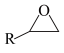 ,R表示烃基)和二氧化碳为原料催化合成环状碳酸酯,反应历程如图所示。下列说法错误的是
,R表示烃基)和二氧化碳为原料催化合成环状碳酸酯,反应历程如图所示。下列说法错误的是

 ,R表示烃基)和二氧化碳为原料催化合成环状碳酸酯,反应历程如图所示。下列说法错误的是
,R表示烃基)和二氧化碳为原料催化合成环状碳酸酯,反应历程如图所示。下列说法错误的是
A.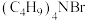 是反应的催化剂 是反应的催化剂 |
| B.反应过程中有极性键的断裂,无极性键的形成 |
| C.反应过程中有4种中间体 |
D.总反应方程式为 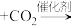 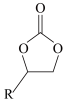 |
您最近一年使用:0次
名校
解题方法
3 . 某科研团队报道了一种新“光合作用”,即借助光将二氧化碳转化为甲烷的新型催化方法,其催化机理如图所示。下列说法错误的是
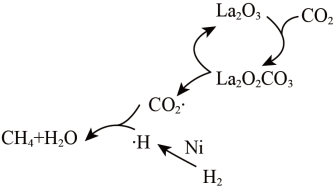

| A.La2O2CO3是中间产物 |
| B.该历程实现了化学能转化为光能 |
| C.该历程只有共价键的断裂与形成 |
D.该历程的总反应方程式为 |
您最近一年使用:0次
名校
4 . 某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
为了探究浓度对反应速率的影响,小组成员设计了三组平行实验,实验时,溶液迅速混合并开始计时通过溶液褪色所需时间来判断反应快慢。(控制反应过程中溶液温度为室温)
【实验原理】
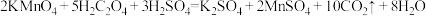
【实验内容及记录】
请回答下列问题:
(1)第三组实验中,所加蒸馏水的体积为x=___________ mL
(2)利用实验2中数据计算,
___________ 。
(3)根据上表中的实验数据,可以得到的结论是___________ 。
(4)该化学小组同学根据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。

①该小组同学提出的假设是___________ 。
②请你帮助该小组同学完成实验方案,并填写表中空白。
实验4中向试管中加入少量固体___________ 。
③若该小组同学提出的假设成立,室温下溶液颜色褪至无色所需时间___________ (填大于、等于或小于)4 min。
为了探究浓度对反应速率的影响,小组成员设计了三组平行实验,实验时,溶液迅速混合并开始计时通过溶液褪色所需时间来判断反应快慢。(控制反应过程中溶液温度为室温)
【实验原理】
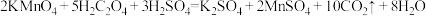
【实验内容及记录】
| 编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | 调控溶液温度 | |||
| 0.6 mol/L H2C2O4溶液 | H2O | 0.2 mol/LKMnO4溶液 | 3 mol/L稀硫酸 | |||
| 1 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 | 298K |
| 2 | 3.0 | 3.0 | 2.0 | 2.0 | 5.0 | 298K |
| 3 | 3.0 | x | 1.0 | 2.0 | 6.4 | 298K |
(1)第三组实验中,所加蒸馏水的体积为x=
(2)利用实验2中数据计算,

(3)根据上表中的实验数据,可以得到的结论是
(4)该化学小组同学根据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。

①该小组同学提出的假设是
②请你帮助该小组同学完成实验方案,并填写表中空白。
| 编号 | 室温下,试管中所加试剂及其用量/mL | 再向试管中加入少量固体 | 室温下溶液颜色褪至无色所需时间/min | |||
| 0.6 mol/L H2C2O4溶液 | H2O | 0.2 mol/LKMnO4溶液 |  稀硫酸 稀硫酸 | |||
| 4 | 3.0 | 2.0 | 3.0 | 2.0 | ___________ | ___________ |
③若该小组同学提出的假设成立,室温下溶液颜色褪至无色所需时间
您最近一年使用:0次
2023-05-30更新
|
112次组卷
|
4卷引用:山东省滨州市部分学校2022-2023学年高一下学期5月联考化学试题
名校
5 . 研究表明 与CO在一定条件作用下发生反应的能量变化及反应过程如图所示,下列说法正确的是
与CO在一定条件作用下发生反应的能量变化及反应过程如图所示,下列说法正确的是
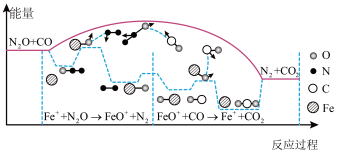
 与CO在一定条件作用下发生反应的能量变化及反应过程如图所示,下列说法正确的是
与CO在一定条件作用下发生反应的能量变化及反应过程如图所示,下列说法正确的是
| A.在反应过程中,存在极性共价键和非极性键的断裂与生成 |
B.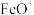 使反应更容易发生,是该反应的催化剂 使反应更容易发生,是该反应的催化剂 |
C.该反应的总反应方程式为 |
D. 、 、 两步反应均为放热反应 两步反应均为放热反应 |
您最近一年使用:0次
2023-05-30更新
|
70次组卷
|
2卷引用:山东省滨州市部分学校2022-2023学年高一下学期5月联考化学试题
名校
6 . 下列实验操作及现象正确,且与解释或结论存在对应关系是
| 选项 | 实验操作及现象 | 解释或结论 |
| A | 向双氧水中滴加酸性 溶液,迅速有气泡生成 溶液,迅速有气泡生成 |  对 对 分解具有催化作用 分解具有催化作用 |
| B | 向 溶液中滴入足量氯水和 溶液中滴入足量氯水和 ,振荡、静置、分层;再向上层溶液中加入KSCN溶液,下层溶液呈紫红色,上层溶液变为血红色。 ,振荡、静置、分层;再向上层溶液中加入KSCN溶液,下层溶液呈紫红色,上层溶液变为血红色。 | 证明还原性: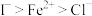 |
| C | 向硫酸酸化的食盐溶液中加入KI溶液和几滴淀粉溶液,溶液未变蓝色 | 该食盐不是含碘盐 |
| D | 向 溶液中滴入稀盐酸,出现白色凝胶 溶液中滴入稀盐酸,出现白色凝胶 | 非金属性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-30更新
|
82次组卷
|
2卷引用:山东省滨州市部分学校2022-2023学年高一下学期5月联考化学试题
名校
7 .  在水中易分解。一定条件下,起始浓度均为
在水中易分解。一定条件下,起始浓度均为 的
的 溶液,在不同的
溶液,在不同的 、温度下,发生分解反应,测得
、温度下,发生分解反应,测得 浓度减少一半所需的时间(t)如表所示:下列判断不正确的是
浓度减少一半所需的时间(t)如表所示:下列判断不正确的是
 在水中易分解。一定条件下,起始浓度均为
在水中易分解。一定条件下,起始浓度均为 的
的 溶液,在不同的
溶液,在不同的 、温度下,发生分解反应,测得
、温度下,发生分解反应,测得 浓度减少一半所需的时间(t)如表所示:下列判断不正确的是
浓度减少一半所需的时间(t)如表所示:下列判断不正确的是| pH t/min T/℃ | 3.0 | 4.0 | 5.0 | 6.0 |
| 20 | 301 | 231 | 169 | 58 |
| 30 | 158 | 108 | 48 | 15 |
| 50 | 31 | 26 | 15 | 7 |
A.实验表明,升高温度能加快 的分解速率 的分解速率 |
B. 增大能加速 增大能加速 分解,表明 分解,表明 可能对 可能对 的分解起催化作用 的分解起催化作用 |
C.据表中的规律可推知, 在下列条件下的分解速率 在下列条件下的分解速率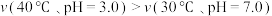 |
D.在30℃、 时, 时, 的分解速率为 的分解速率为 |
您最近一年使用:0次
名校
解题方法
8 . 下列图中的实验方案,能达到实验目的的是
| A | B | C | D | |
| 实验 方案 |
|
|
|
|
| 实验 目的 | 验证 对 对 分解反应有催化作用 分解反应有催化作用 | 实验室利用该装置制备少量氯气 | 验证非金属性: | 从碘的四氯化碳溶液中分离出碘单质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-12更新
|
125次组卷
|
2卷引用:山东省滨州市沾化区、阳信县2022-2023学年高一下学期期中联考化学(A)试题
9 . 某学生为探究锌与稀盐酸反应的速率变化,用排水集气法收集反应放出的氢气。所用稀盐酸浓度有1.00mol·L-1、2.00mol·L-1两种浓度,每次实验稀盐酸的用量为25.00mL,锌有细颗粒与粗颗粒两种规格,用量为6.50g。实验温度为25℃、35℃。(已知Zn2+对该反应的反应速率无影响)
(1)请在实验目的一栏中的空白项处填出对应的实验编号:
(2)实验①记录如下(换算成标况):
①计算在30~40s范围内盐酸的平均反应速率ν(HCl)=_______ (忽略溶液体积变化);
②反应速率最大的时间段(如0~10s)为_______ ,可能原因是_______ ;
③反应速率后段明显下降的主要影响因素是_______ 。
(3)测量氢气体积时,在不影响产生H2气体总量的情况下,往往在盐酸中分别加入相同体积的下列溶液以减慢反应速率,你认为可行的是_______(填序号)。
(4)某化学研究小组的同学为比较Fe3+和Cu2+对H2O2分解的催化效果,设计了如图所示的实验。
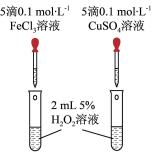
①如图可通过观察_______ 现象,比较得出Fe3+和Cu2+对H2O2分解的催化效果结论;
②某同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是_______ 。
(1)请在实验目的一栏中的空白项处填出对应的实验编号:
| 编号 | t/℃ | 锌规格 | 盐酸浓度/mol·L-1 | 实验目的 |
| ① | 25 | 粗颗粒 | 2.00 | I.实验①和②探究盐酸浓度对该反应速率的影响; II.实验 III.实验 |
| ② | 25 | 粗颗粒 | 1.00 | |
| ③ | 35 | 粗颗粒 | 2.00 | |
| ④ | 25 | 细颗粒 | 2.00 |
| 时间/s | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| 氢气体积/mL | 16.8 | 39.2 | 67.2 | 224 | 420 | 492.8 | 520.8 | 543.2 | 554.4 | 560 |
②反应速率最大的时间段(如0~10s)为
③反应速率后段明显下降的主要影响因素是
(3)测量氢气体积时,在不影响产生H2气体总量的情况下,往往在盐酸中分别加入相同体积的下列溶液以减慢反应速率,你认为可行的是_______(填序号)。
| A.NaNO3溶液 | B.NaCl溶液 | C.CuSO4溶液 | D.Na2CO3溶液 |

①如图可通过观察
②某同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是
您最近一年使用:0次
名校
10 . 如图所示为CFCl3破坏臭氧层的过程。下列说法错误的是


| A.过程Ⅰ可表示为:CFCl3→CFCl2+Cl | B.过程Ⅲ中O+O→O2是吸热过程 |
| C.紫外辐射为过程Ⅰ断裂化学键提供能量 | D.CFCl3是破坏臭氧层的催化剂 |
您最近一年使用:0次
2023-05-12更新
|
106次组卷
|
2卷引用: 山东省泰安肥城市2022-2023学年高一下学期期中考试化学试题