名校
解题方法
1 . 学习小组在实验室探究催化剂对双氧水分解的作用,查阅资料得知催化剂参与化学反应,通过改变反应历程以改变化学反应速率。回答下列问题:

(1)设计实验探究 对
对 分解反应的催化效果。
分解反应的催化效果。
①结合图中实验,补充操作证明 是
是 分解反应的催化剂
分解反应的催化剂_____________ 。
②分别量取50mL 3% 于三支洁净干燥的试管中,分别加入不同质量的
于三支洁净干燥的试管中,分别加入不同质量的 粉末,40s后测量所得气体体积,数据如下:
粉末,40s后测量所得气体体积,数据如下:
分析数据得出的实验结论是_____ ,分析三支试管中 分解速率不同的可能原因是
分解速率不同的可能原因是______ 。
(2)设计如下实验探究 和
和 对
对 分解反应的催化效果。
分解反应的催化效果。
①试管I、II、III中均盛有10mL 5% :
:
试管I中反应速率大于试管II中反应速率的原因可能是:
ⅰ. 做催化剂且试管I中
做催化剂且试管I中 大
大
ⅱ.__________________________
经查阅资料知 无催化作用,请设计实验证明
无催化作用,请设计实验证明_______________________________________ 。
② 溶液加入
溶液加入 溶液后,溶液中会发生两个氧化还原反应,且两个反应中
溶液后,溶液中会发生两个氧化还原反应,且两个反应中 均参加了反应,从催化剂的角度分析两个氧化还原反应的离子方程式分别是
均参加了反应,从催化剂的角度分析两个氧化还原反应的离子方程式分别是__________________________ 和___________________________________________ (按反应发生的顺序写)。

(1)设计实验探究
 对
对 分解反应的催化效果。
分解反应的催化效果。①结合图中实验,补充操作证明
 是
是 分解反应的催化剂
分解反应的催化剂②分别量取50mL 3%
 于三支洁净干燥的试管中,分别加入不同质量的
于三支洁净干燥的试管中,分别加入不同质量的 粉末,40s后测量所得气体体积,数据如下:
粉末,40s后测量所得气体体积,数据如下:
| 0.1 | 0.2 | 0.4 |
40s时 | 49 | 61 | 86 |
 分解速率不同的可能原因是
分解速率不同的可能原因是(2)设计如下实验探究
 和
和 对
对 分解反应的催化效果。
分解反应的催化效果。①试管I、II、III中均盛有10mL 5%
 :
:试管 | I | II | III |
滴加试剂 | 5滴0.1 | 5滴0.1 | 5滴蒸馏水 |
现象 | 较快产生细小气泡 | 缓慢产生细小气泡 | 无明显现象 |
ⅰ.
 做催化剂且试管I中
做催化剂且试管I中 大
大ⅱ.
经查阅资料知
 无催化作用,请设计实验证明
无催化作用,请设计实验证明②
 溶液加入
溶液加入 溶液后,溶液中会发生两个氧化还原反应,且两个反应中
溶液后,溶液中会发生两个氧化还原反应,且两个反应中 均参加了反应,从催化剂的角度分析两个氧化还原反应的离子方程式分别是
均参加了反应,从催化剂的角度分析两个氧化还原反应的离子方程式分别是
您最近一年使用:0次
名校
2 . 我国科学家研究了活性炭催化条件下煤气中H2S和Hg的协同脱除,部分反应机理如图所示(吸附在催化剂表面的物种用*标注)。下列说法正确的是
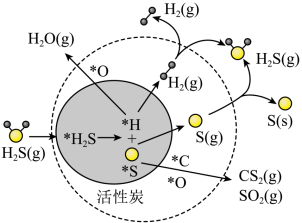
| A.图示反应过程中有极性共价键的断裂,没有非极性共价键的生成 |
| B.H2S活性炭分解生成H2(g)和S(s)的过程释放能量 |
| C.整个脱硫过程中硫元素既表现出氧化性又表现出还原性 |
| D.该机理由于活性炭的参与降低了H2S分解的热效应,使反应更易进行 |
您最近一年使用:0次
2023-04-29更新
|
257次组卷
|
5卷引用:山东省菏泽市2022-2023学年高一下学期期中考试化学(A)试题
名校
解题方法
3 . 中国科学家研究的复合光催化剂[碳纳米点(CQDs)/氮化碳(C3N4)纳米复合物]可以利用太阳光高效分解水,其原理如图所示。制备的H2用于还原CO2合成甲醇(CH3OH),可实现资源的再利用。下列有关说法错误的是

| A.太阳光高效分解水的过程中将光能转化成化学能 |
B.过程I发生的反应为2H2O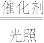 H2↑+H2O2 H2↑+H2O2 |
| C.H2还原CO2合成甲醇过程中原子利用率100% |
| D.整个光解过程中催化剂与反应物之间存在化学键的生成与断裂 |
您最近一年使用:0次
2023-04-29更新
|
208次组卷
|
3卷引用:山东省菏泽市2022-2023学年高一下学期期中考试化学(A)试题
解题方法
4 . 下列有关化学反应速率和化学反应限度的叙述正确的是
A. 与水反应时,增加水的质量,能明显增大反应速率 与水反应时,增加水的质量,能明显增大反应速率 |
B.使用 漂白时,加入适量稀盐酸可增大反应速率 漂白时,加入适量稀盐酸可增大反应速率 |
C. 分解制取 分解制取 时,添加少量 时,添加少量 可以提高 可以提高 产量 产量 |
D.将稀硫酸改为98%的浓硫酸能加快 与 与 反应产生 反应产生 的速率 的速率 |
您最近一年使用:0次
名校
5 . 某学习小组为了探究影响高锰酸钾酸性溶液与NaHSO3溶液反应速率的因素,该小组设计如表实验方案。
下列说法正确的是
| 实验 | V(NaHSO3)/mL c=0.1 mol/L | V(KMnO4)/mL c=0.6 mol/L | V(H2SO4)/mL c=0.1 mol/L | V(MnSO4)/mL c=0.1 mol/L | V(H2O)/mL | 褪色时间t/min |
| 1 | 3.0 | 2.0 | 1.0 | 0.0 | 2.0 | 8 |
| 2 | 3.0 | 2.0 | 2.0 | 0.0 | a | 6 |
| 3 | 4.0 | 2.0 | 2.0 | 0.0 | 0.0 | 4 |
| 4 | 4.0 | 2.0 | 1.0 | 0.5 | b | 3 |
A.该反应的离子方程式为:5 +2 +2 +6H+=2Mn2++5 +6H+=2Mn2++5 +3H2O +3H2O |
| B.a=1.0,b=0.5 |
C.实验3从反应开始到反应结束这段时间内反应速率v( )=0.025 mol/(L∙min) )=0.025 mol/(L∙min) |
D.实验证明 可能是该反应的催化剂 可能是该反应的催化剂 |
您最近一年使用:0次
2023-04-25更新
|
427次组卷
|
14卷引用:山东省东营市利津县高级中学2022-2023学年高一下学期5月月考化学试题
山东省东营市利津县高级中学2022-2023学年高一下学期5月月考化学试题 山西省吕梁市临县第一中学2021-2022学年高一下学期5月月考化学试题广西玉林市普通高中2021-2022学年高一下学期期末考试化学试题重庆市西南大学附属中学校2021-2022学年高一下学期期末考试化学试题(已下线)【2023】【高一下】【其他】【余高2】【高中化学】【刘尼尼收集】新疆生产建设兵团第一师高级中学2022-2023学年高一下学期4月月考化学试题贵州省遵义市仁怀市高中教育联盟2022-2023学年高一下学期5月期中考试化学试题(已下线)第05练 化学反应的速率与限度-2023年【暑假分层作业】高一化学(人教版2019必修第二册)四川省射洪中学2022—2023学年高一下学期(强基班)第三次月考化学试题四川省射洪中学校强基班2023-2024学年高一下学期4月第一次月考化学试题(已下线)清单04 化学反应的速率和限度(考点清单)(讲+练)-2023-2024学年高一化学下学期期末考点大串讲(人教版2019必修第二册)河南省开封市五县2021-2022学年高二下学期期末考试化学试题(已下线)2.1.2 影响化学反应速率的因素 活化能 -2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)(已下线)化学反应速率与化学平衡——课时2化学反应速率的影响因素
名校
解题方法
6 . 合成氨对解决粮食问题贡献巨大,反应如下: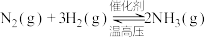 。该反应的能量变化及微观历程的示意图如图所示
。该反应的能量变化及微观历程的示意图如图所示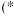 表示物质吸附在催化剂表面的形态)。下列说法错误的是
表示物质吸附在催化剂表面的形态)。下列说法错误的是
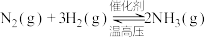 。该反应的能量变化及微观历程的示意图如图所示
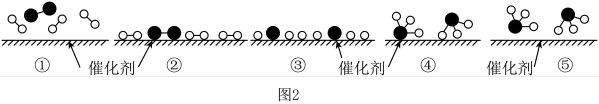
。该反应的能量变化及微观历程的示意图如图所示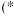 表示物质吸附在催化剂表面的形态)。下列说法错误的是
表示物质吸附在催化剂表面的形态)。下列说法错误的是
A.在催化剂表面只存在 的断裂,不存在 的断裂,不存在 的形成 的形成 |
B.图2中② ③的过程吸收能量 ③的过程吸收能量 |
C.③ ④的过程可表示为: ④的过程可表示为: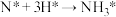 |
| D.其他条件相同,使用催化剂可以减少合成氨反应放出的热量 |
您最近一年使用:0次
2023-04-24更新
|
217次组卷
|
4卷引用:山东省济宁市兖州区2022-2023学年高一下学期期中化学试题
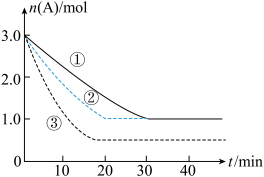
7 . 某化学反应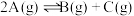 在三种不同条件下进行,2L的密闭容器中只充入3.0molA,A的物质的量随反应时间的变化情况如图所示。下列说法正确的是
在三种不同条件下进行,2L的密闭容器中只充入3.0molA,A的物质的量随反应时间的变化情况如图所示。下列说法正确的是
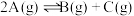 在三种不同条件下进行,2L的密闭容器中只充入3.0molA,A的物质的量随反应时间的变化情况如图所示。下列说法正确的是
在三种不同条件下进行,2L的密闭容器中只充入3.0molA,A的物质的量随反应时间的变化情况如图所示。下列说法正确的是
| A.与实验①相比,②可能使用了催化剂 |
| B.与实验①相比,实验③增大了压强 |
| C.适当升高温度可以使平衡正向移动 |
| D.0~20min,实验②中B的平均反应速率是0.05 mol·L-1·min-1 |
您最近一年使用:0次
解题方法
8 . 三元催化器是重要的汽车尾气净化装置,其工作原理如图所示。下列说法错误的是


A.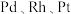 能加快反应速率 能加快反应速率 |
| B.三元催化器的使用可以降低光化学烟雾 |
C.催化转化反应中,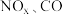 、碳氢化合物均作还原剂 、碳氢化合物均作还原剂 |
D.该催化转化器中可能发生反应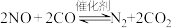 |
您最近一年使用:0次
9 . I.某研究性学习小组利用草酸(H2C2O4)溶液和酸性KMnO4溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
(1)草酸为弱酸,写出草酸与高锰酸钾反应的离子方程式___________ 。
(2)通过实验A、B,可探究出___________ (填外部因素)的改变对化学反应速率的影响,其中V1=___________ 、T1=___________ ;通过实验___________ (填实验序号)可探究出温度变化对化学反应速率的影响。
(3)若t1<8,则由此实验可以得出的结论是___________ ;忽略溶液体积的变化,利用实验B中数据计算,0-8s内,用KMnO4的浓度变化表示的反应速率v(KMnO4) ___________ 。
Ⅱ.催化剂在生产和科技领域起到重大作用。某化学研究小组的同学分别设计了如图1所示的实验,用控制变量法比较和对分解的催化效果。请回答相关问题;
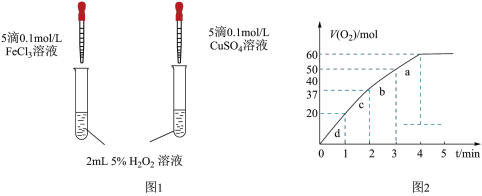
(4)定性分析:某同学通过观察甲中两支试管产生气泡的快慢,由此得出Fe3+和Cu2+对H2O2分解的催化效果,该结论___________ 填(“合理”或“不合理”),原因___________ 。
| 实验序号 | 实验 温度 | 有关物质 | 溶液颜色褪至无色所需时间/s | ||||
酸性KMnO4溶液 | H2C2O4溶液 | H2O | |||||
| V/mL | c/ mol∙L-1 | V/mL | c/ mol∙L-1 | V/mL | |||
| A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
| B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
| C | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
(2)通过实验A、B,可探究出
(3)若t1<8,则由此实验可以得出的结论是
Ⅱ.催化剂在生产和科技领域起到重大作用。某化学研究小组的同学分别设计了如图1所示的实验,用控制变量法比较和对分解的催化效果。请回答相关问题;

(4)定性分析:某同学通过观察甲中两支试管产生气泡的快慢,由此得出Fe3+和Cu2+对H2O2分解的催化效果,该结论
您最近一年使用:0次
2023-04-17更新
|
212次组卷
|
2卷引用:山东省日照市莒县第一中学2022-2023学年高一下学期4月月考化学试题
10 . 为实现“碳达峰”及“碳中和”,二氧化碳甲烷化技术是CO2循环再利用最有效的技术之一。
(1)二氧化碳甲烷化时发生的反应为:CO2(g)+4H2(g) CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
①298K时,已知相关物质的相对能量如图,则该反应的ΔH=___________ kJ·mol-1。

②能判断该过程反应已达化学平衡状态的标志是___________ (填标号)。
A.CO2体积分数保持不变
B.容器中混合气体的质量保持不变
C.混合气体的平均相对分子质量保持不变
D.CO2的生成速率与H2O的生成速率相等
③有利于提高体系中CO2平衡转化率的措施是___________ (填标号)。
A.使用高效催化剂B.增加CO2投入量C.延长反应时间D.及时分离CH4
(2)催化剂的选择是CO2甲烷化的核心,金属Ni或Ni-CeO2均可作为催化剂。反应相同时间,测得CO2转化率和CH4选择性随温度的变化如图所示。高于320°C,以Ni-CeO2为催化剂,CO2转化率略有下降,而以Ni为催化剂,CO2转化率却仍在上升,其原因是___________ 。(CH4的选择性公式:CH4的选择性=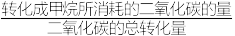 ×100%)
×100%)

(3)Ni-CeO2催化CO2加H2生成CH4的反应历程如图所示(吸附在催化剂表面的物种用*标注),则发生的副反应的方程式为___________ 。

(4)CO2甲烷化发生反应CO2(g)+4H2(g) CH4(g)+2H2O(g),由于该反应存在副反应,反应的CO2不能100%转化为CH4,生成的CH4须依据CH4的选择性公式进行计算。某温度,在体积为1L的恒容密闭容器中加入1molCO2和4molH2,10min后达到平衡,CO2的平衡转化率和CH4的选择性分别为80%、90%,则CH4的反应速率为
CH4(g)+2H2O(g),由于该反应存在副反应,反应的CO2不能100%转化为CH4,生成的CH4须依据CH4的选择性公式进行计算。某温度,在体积为1L的恒容密闭容器中加入1molCO2和4molH2,10min后达到平衡,CO2的平衡转化率和CH4的选择性分别为80%、90%,则CH4的反应速率为___________ 。
(1)二氧化碳甲烷化时发生的反应为:CO2(g)+4H2(g)
 CH4(g)+2H2O(g)
CH4(g)+2H2O(g)①298K时,已知相关物质的相对能量如图,则该反应的ΔH=

②能判断该过程反应已达化学平衡状态的标志是
A.CO2体积分数保持不变
B.容器中混合气体的质量保持不变
C.混合气体的平均相对分子质量保持不变
D.CO2的生成速率与H2O的生成速率相等
③有利于提高体系中CO2平衡转化率的措施是
A.使用高效催化剂B.增加CO2投入量C.延长反应时间D.及时分离CH4
(2)催化剂的选择是CO2甲烷化的核心,金属Ni或Ni-CeO2均可作为催化剂。反应相同时间,测得CO2转化率和CH4选择性随温度的变化如图所示。高于320°C,以Ni-CeO2为催化剂,CO2转化率略有下降,而以Ni为催化剂,CO2转化率却仍在上升,其原因是
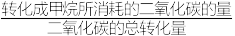 ×100%)
×100%)
(3)Ni-CeO2催化CO2加H2生成CH4的反应历程如图所示(吸附在催化剂表面的物种用*标注),则发生的副反应的方程式为

(4)CO2甲烷化发生反应CO2(g)+4H2(g)
 CH4(g)+2H2O(g),由于该反应存在副反应,反应的CO2不能100%转化为CH4,生成的CH4须依据CH4的选择性公式进行计算。某温度,在体积为1L的恒容密闭容器中加入1molCO2和4molH2,10min后达到平衡,CO2的平衡转化率和CH4的选择性分别为80%、90%,则CH4的反应速率为
CH4(g)+2H2O(g),由于该反应存在副反应,反应的CO2不能100%转化为CH4,生成的CH4须依据CH4的选择性公式进行计算。某温度,在体积为1L的恒容密闭容器中加入1molCO2和4molH2,10min后达到平衡,CO2的平衡转化率和CH4的选择性分别为80%、90%,则CH4的反应速率为
您最近一年使用:0次

 体积/mL
体积/mL


