解题方法
1 . 氨是人科学技术发史上的一项重大突,目前工业上用氢气和氨气直接合成氨。
(1)固氮一直是科学家致力研究的要课题,有关热力学数据如下:
常温下,大气固氮的倾向_______ 工业固氮(填“大于”或“小于”)
(2)N2(g)与H2(g) 反应的能量变化如图所示,则N2(g)与H2(g) 反应制备NH3(g) 的热化学方程式为:_______ ;

(3)T℃时,在2L恒容密闭容器中加入1.2mol N2和2mol H2模拟一定条件下工业固氮[N2(g)+3H2(g) 2NH3(g)],体系中n(NH3)随时间的变化如图所示;
2NH3(g)],体系中n(NH3)随时间的变化如图所示;

①前2分钟内的平均反应速率v(NH3)=_______ mol·L-1·min-1;
②有关工业固氮的说法正确的是_______ (选填序号) 。
A.使用化剂可提高反应物的转化率
B.循环使用N2、H2可提高NH3的产率
C.温度控制在500℃左右有利于反应向正方向行
D.增大压强有利于加快反应速率,所以压强大越好
③T℃时,该反应的平衡常数为_______ ;
(4)研究表明某些过渡金属催化剂可以加速氨气的分解,某温度下,用等质量的不同金属分别催化等浓度的氨气,测得氨气分解的初始速率(单位: mmol/min)与化剂的对应关系如表所示。
在不同催化剂的催化作用下,氨气分解反应中的活化能最大的催化剂是 _______ (填化学式)
(1)固氮一直是科学家致力研究的要课题,有关热力学数据如下:
| 反应 | 大气固氮N2(g)+O2(g)  2NO(g) 2NO(g) | 工业固氮N2(g)+3H2(g)  2NH3(g) 2NH3(g) | ||||
| 温度/℃ | 25 | 2000 | 25 | 350 | 400 | 450 |
| 平衡常数K | 3.84×10-31 | 0.1 | 5×108 | 1.847 | 0.504 | 0.152 |
(2)N2(g)与H2(g) 反应的能量变化如图所示,则N2(g)与H2(g) 反应制备NH3(g) 的热化学方程式为:

(3)T℃时,在2L恒容密闭容器中加入1.2mol N2和2mol H2模拟一定条件下工业固氮[N2(g)+3H2(g)
 2NH3(g)],体系中n(NH3)随时间的变化如图所示;
2NH3(g)],体系中n(NH3)随时间的变化如图所示;
①前2分钟内的平均反应速率v(NH3)=
②有关工业固氮的说法正确的是
A.使用化剂可提高反应物的转化率
B.循环使用N2、H2可提高NH3的产率
C.温度控制在500℃左右有利于反应向正方向行
D.增大压强有利于加快反应速率,所以压强大越好
③T℃时,该反应的平衡常数为
(4)研究表明某些过渡金属催化剂可以加速氨气的分解,某温度下,用等质量的不同金属分别催化等浓度的氨气,测得氨气分解的初始速率(单位: mmol/min)与化剂的对应关系如表所示。
| 催化剂 | Fe | Pd | Ru | Rh | Pt | Ni |
| 初始速率 | 0.5 | 1.8 | 7.9 | 4.0 | 2.2 | 3.0 |
您最近一年使用:0次
名校
2 . 如图表示某可逆反应在使用和未使用催化剂时,反应过程和能量的对应关系。下列说法正确的是
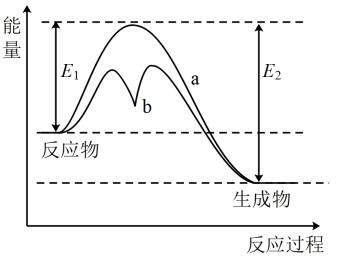

| A.反应为吸热反应 |
| B.a与b相比,a的反应速率更快 |
| C.a与b相比,反应的平衡常数一定不同 |
| D.反应物断键吸收的总能量小于生成物成键释放的总能量 |
您最近一年使用:0次
2022-02-18更新
|
211次组卷
|
2卷引用:广东省广州真光中学2021-2022学年高二上学期12月月考化学试题
名校
解题方法
3 . 如图,这种具有不同能量的分子百分数和能量的对应关系图,叫做一定温度下分子能量分布曲线图。图中E表示分子平均能量,Ec是活化分子具有的最低能量。下列说法不正确的是
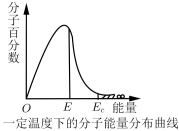

| A.图中Ec与E之差表示活化能 |
| B.升高温度,图中阴影部分面积会增大 |
| C.使用合适的催化剂,E不变,Ec变小 |
| D.能量大于Ec的分子间发生的碰撞一定是有效碰撞 |
您最近一年使用:0次
2020-03-05更新
|
258次组卷
|
3卷引用:湖北省荆州市2020届高三上学期质量检测(一) 化学试题
12-13高二上·河南许昌·期末
4 . 下图表示某可逆反应在使用和未使用催化剂时,反应过程和能量的对应关系。下列说法一定正确的是
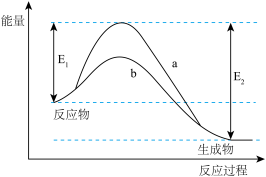

| A.该反应为吸热反应 |
| B.a与b相比,a的反应速率更快 |
| C.a与b相比,反应的平衡常数一定不同 |
| D.反应物吸收的总能量小于生成物释放的总能量 |
您最近一年使用:0次
2019-04-14更新
|
354次组卷
|
3卷引用:2011-2012学年河南省许昌部分学校高二上学期期末联考化学试卷
(已下线)2011-2012学年河南省许昌部分学校高二上学期期末联考化学试卷【区级联考】上海市黄浦区2019届高三下学期等级考二模试卷化学试题2019-2020学年新人教版必修2同步练习题:6.1化学反应与能量变化
名校
5 . “氧来乐”是鱼塘养殖户的“救命药”,其标签如下表:

(1)“氧来乐”可以给鱼塘增氧的化学反应方程式:___________ 。有学生认为 也可以给鱼塘增氧,你认为可以吗?并简述理由:
也可以给鱼塘增氧,你认为可以吗?并简述理由:___________ 。
(2) 分解速率受多种因素影响。学生甲通过数字化实验测得
分解速率受多种因素影响。学生甲通过数字化实验测得 时,
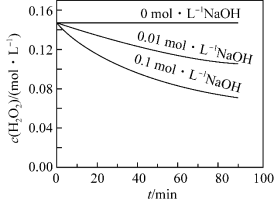
时, 浓度随时间的变化如图所示,从下图中可得出的结论是:其他条件相同时,
浓度随时间的变化如图所示,从下图中可得出的结论是:其他条件相同时,___________ 。
(3)学生乙利用实验室提供的仪器和试剂进行了教材上的实验。
步骤:分别向①、②两支试管中加入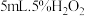 溶液,同时分别向两试管中加入2滴
溶液,同时分别向两试管中加入2滴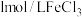 溶液(作催化剂)。待试管中均有适量气泡出现时,将试管①放入
溶液(作催化剂)。待试管中均有适量气泡出现时,将试管①放入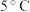 水浴中,将试管②放入
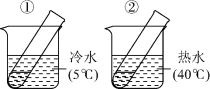
水浴中,将试管②放入 水浴中,观察实验现象。如下图。该实验是为了探究
水浴中,观察实验现象。如下图。该实验是为了探究___________ 对 分解速率的影响;
分解速率的影响;
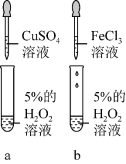
(4)学生丙为探究 两种催化剂对
两种催化剂对 分解速率的影响。
分解速率的影响。
设计了如下实验(如下图):分别向 两支试管中加入
两支试管中加入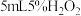 溶液,向试管a中加入2滴
溶液,向试管a中加入2滴 ,向试管b中加入2滴
,向试管b中加入2滴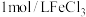 溶液,观察实验现象。该方案存在不严谨之处。请你改进:
溶液,观察实验现象。该方案存在不严谨之处。请你改进:___________ 。

| 主要成分 | 过氧化氢 |
| 含量规格 |  |
| 作用与用途 | 本品在分解过程中释放出活泼的新生态氧,用于养殖池塘的增氧,药性温和,使用方便,无残留,绿色环保。 |
| 用法 | 将本品以1000倍水稀释后直接泼洒于养殖池塘中 |
| 用量 | 每亩水深1米用本品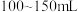 ,病情严重可加量使用,并可使用催化剂 ,病情严重可加量使用,并可使用催化剂 |
 也可以给鱼塘增氧,你认为可以吗?并简述理由:
也可以给鱼塘增氧,你认为可以吗?并简述理由:(2)
 分解速率受多种因素影响。学生甲通过数字化实验测得
分解速率受多种因素影响。学生甲通过数字化实验测得 时,
时, 浓度随时间的变化如图所示,从下图中可得出的结论是:其他条件相同时,
浓度随时间的变化如图所示,从下图中可得出的结论是:其他条件相同时,
(3)学生乙利用实验室提供的仪器和试剂进行了教材上的实验。
步骤:分别向①、②两支试管中加入
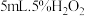 溶液,同时分别向两试管中加入2滴
溶液,同时分别向两试管中加入2滴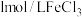 溶液(作催化剂)。待试管中均有适量气泡出现时,将试管①放入
溶液(作催化剂)。待试管中均有适量气泡出现时,将试管①放入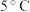 水浴中,将试管②放入
水浴中,将试管②放入 水浴中,观察实验现象。如下图。该实验是为了探究
水浴中,观察实验现象。如下图。该实验是为了探究 分解速率的影响;
分解速率的影响;
(4)学生丙为探究
 两种催化剂对
两种催化剂对 分解速率的影响。
分解速率的影响。设计了如下实验(如下图):分别向
 两支试管中加入
两支试管中加入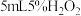 溶液,向试管a中加入2滴
溶液,向试管a中加入2滴 ,向试管b中加入2滴
,向试管b中加入2滴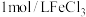 溶液,观察实验现象。该方案存在不严谨之处。请你改进:
溶液,观察实验现象。该方案存在不严谨之处。请你改进:
您最近一年使用:0次
解题方法
6 . 氢气在实验室和工业上有着广泛的用途。请回答:
(1)氢气可以与煤在催化剂作用下制备乙炔,已知部分反应如下:
Ⅰ.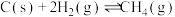

Ⅱ.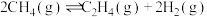

Ⅲ.
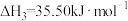
Ⅳ.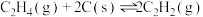

通过计算说明反应Ⅳ自发进行的条件_______ 。
(2)利用氢气与二氧化碳催化反应合成乙烯,是实现低碳转型的一条途径。在0.1MPa、120℃条件下,以 的投料比充入体积固定的密闭容器中,发生反应:
的投料比充入体积固定的密闭容器中,发生反应:
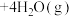 ,平衡时水蒸气的物质的量百分数为50.0%。请回答:
,平衡时水蒸气的物质的量百分数为50.0%。请回答:
①反应的平衡常数表达式为_______ 。
②达到平衡时, 的转化率为
的转化率为_______ 。
(3)氢气可合成氨气,氨气与二氧化碳可以合成尿素,反应为:
 ,分为两步:
,分为两步:
已知投料的组成为 、
、 和水蒸气(有助于分离尿素),一定条件下,氨基甲酸铵(
和水蒸气(有助于分离尿素),一定条件下,氨基甲酸铵( )物质的量与时间的关系图(图甲,t1后物质的量不再改变),以及不同氨碳比(
)物质的量与时间的关系图(图甲,t1后物质的量不再改变),以及不同氨碳比(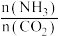 )与水碳比(
)与水碳比(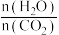 )投料时
)投料时 平衡转化率图象(图乙,a、b代表水碳比):
平衡转化率图象(图乙,a、b代表水碳比):
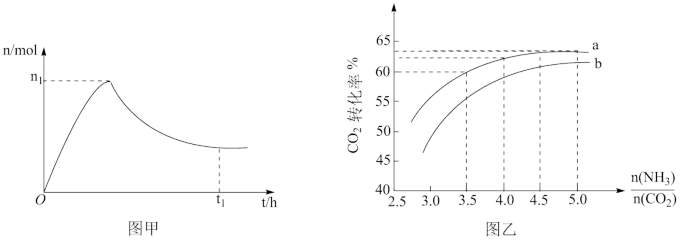
回答下列问题:
①已知反应I又可以分成两步:_______、 ,请写出第一步的化学方程式
,请写出第一步的化学方程式_______ 。
②下列叙述正确的是_______ 。
A.反应Ⅰ的活化能大于反应Ⅱ,
B.增大氨碳比有利于提高尿素产率,原因之一是过量氨气与反应Ⅱ生成的水反应,促进平衡正移
C.实际生产中若选择曲线a,则氨碳比应控制在4.0左右
D.曲线a的水碳比大于曲线b,减小水碳比有利于尿素生成
③如果某催化剂可以同等程度地加速反应Ⅰ和Ⅱ,请在图甲中画出保持其他条件不变,加入该催化剂后从0h到t1时的氨基甲酸铵物质的量变化曲线_______ 。
(1)氢气可以与煤在催化剂作用下制备乙炔,已知部分反应如下:
Ⅰ.
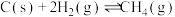

Ⅱ.
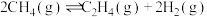

Ⅲ.

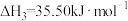
Ⅳ.
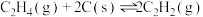

通过计算说明反应Ⅳ自发进行的条件
(2)利用氢气与二氧化碳催化反应合成乙烯,是实现低碳转型的一条途径。在0.1MPa、120℃条件下,以
 的投料比充入体积固定的密闭容器中,发生反应:
的投料比充入体积固定的密闭容器中,发生反应:
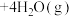 ,平衡时水蒸气的物质的量百分数为50.0%。请回答:
,平衡时水蒸气的物质的量百分数为50.0%。请回答:①反应的平衡常数表达式为
②达到平衡时,
 的转化率为
的转化率为(3)氢气可合成氨气,氨气与二氧化碳可以合成尿素,反应为:

 ,分为两步:
,分为两步:反应步骤 | 反应方程式 |
|
| Ⅰ | 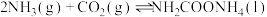  | 快速放热 |
| Ⅱ |  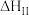 | 慢速吸热 |
已知投料的组成为
 、
、 和水蒸气(有助于分离尿素),一定条件下,氨基甲酸铵(
和水蒸气(有助于分离尿素),一定条件下,氨基甲酸铵( )物质的量与时间的关系图(图甲,t1后物质的量不再改变),以及不同氨碳比(
)物质的量与时间的关系图(图甲,t1后物质的量不再改变),以及不同氨碳比(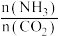 )与水碳比(
)与水碳比(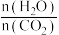 )投料时
)投料时 平衡转化率图象(图乙,a、b代表水碳比):
平衡转化率图象(图乙,a、b代表水碳比):
回答下列问题:
①已知反应I又可以分成两步:_______、
 ,请写出第一步的化学方程式
,请写出第一步的化学方程式②下列叙述正确的是
A.反应Ⅰ的活化能大于反应Ⅱ,

B.增大氨碳比有利于提高尿素产率,原因之一是过量氨气与反应Ⅱ生成的水反应,促进平衡正移
C.实际生产中若选择曲线a,则氨碳比应控制在4.0左右
D.曲线a的水碳比大于曲线b,减小水碳比有利于尿素生成
③如果某催化剂可以同等程度地加速反应Ⅰ和Ⅱ,请在图甲中画出保持其他条件不变,加入该催化剂后从0h到t1时的氨基甲酸铵物质的量变化曲线
您最近一年使用:0次
名校
7 . 萘、四氢萘、十氢萘用途广泛,其转化关系为: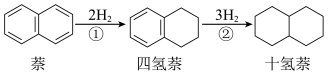 ,该过程中能量变化如图所示,下列说法不正确的是:
,该过程中能量变化如图所示,下列说法不正确的是:
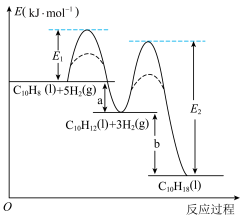
 ,该过程中能量变化如图所示,下列说法不正确的是:
,该过程中能量变化如图所示,下列说法不正确的是:
A.萘分子(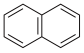 )的一氯代物有2种 )的一氯代物有2种 |
| B.实线表示无催化剂的反应过程,虚线表示有催化剂的反应过程 |
| C.E1、E2表示活化能,a的大小由E1决定,b的大小由E2决定 |
| D.物质的稳定性:十氢萘>四氢萘>萘 |
您最近一年使用:0次
2019-11-13更新
|
275次组卷
|
3卷引用:湖北省荆州中学、宜昌一中等“荆、荆、襄、宜四地七校2019-2020学年高二11月联考化学试题
8 . 请阅读下列材料,完成下面小题。
硫酸的工业用途非常广泛,可用于制造化肥、除铁锈、作电解液等。工业制硫酸的关键一步是将SO2氧化为SO3,该反应为2SO2+O2 2SO3。但该反应速率小,无法投入工业化生产。后来化学家们不断地改进反应条件,找到了理想的催化剂及反应的适宜温度,成功开发出了制造硫酸的生产工艺。
2SO3。但该反应速率小,无法投入工业化生产。后来化学家们不断地改进反应条件,找到了理想的催化剂及反应的适宜温度,成功开发出了制造硫酸的生产工艺。
1. SO2与O2在一定条件下反应生成SO3,该反应属于( )
A. 化合反应 B. 分解反应 C. 置换反应 D. 复分解反应
2. 上述材料中的反应是氧化还原反应,下列有关该反应的说法正确的是( )
A. O2是还原剂 B. SO2被氧化
C. O2失去电子 D. SO2发生还原反应
3. 上述材料中的反应在密闭容器中进行,下列关于该反应的说法正确的是( )
A. 升高温度能减慢反应速率
B. SO2与O2能100%转化为SO3
C. 减小O2的浓度能加快反应速率
D. 使用恰当的催化剂能加快反应速率
4. 上述材料中的反应为放热反应,下列说法正确的是( )
A. 断开化学键放出能量
B. 放热反应都不需要加热
C. 该反应的逆反应是吸热反应
D. 该反应的反应物总能量小于生成物的总能量
硫酸的工业用途非常广泛,可用于制造化肥、除铁锈、作电解液等。工业制硫酸的关键一步是将SO2氧化为SO3,该反应为2SO2+O2
 2SO3。但该反应速率小,无法投入工业化生产。后来化学家们不断地改进反应条件,找到了理想的催化剂及反应的适宜温度,成功开发出了制造硫酸的生产工艺。
2SO3。但该反应速率小,无法投入工业化生产。后来化学家们不断地改进反应条件,找到了理想的催化剂及反应的适宜温度,成功开发出了制造硫酸的生产工艺。1. SO2与O2在一定条件下反应生成SO3,该反应属于
A. 化合反应 B. 分解反应 C. 置换反应 D. 复分解反应
2. 上述材料中的反应是氧化还原反应,下列有关该反应的说法正确的是
A. O2是还原剂 B. SO2被氧化
C. O2失去电子 D. SO2发生还原反应
3. 上述材料中的反应在密闭容器中进行,下列关于该反应的说法正确的是
A. 升高温度能减慢反应速率
B. SO2与O2能100%转化为SO3
C. 减小O2的浓度能加快反应速率
D. 使用恰当的催化剂能加快反应速率
4. 上述材料中的反应为放热反应,下列说法正确的是
A. 断开化学键放出能量
B. 放热反应都不需要加热
C. 该反应的逆反应是吸热反应
D. 该反应的反应物总能量小于生成物的总能量
您最近一年使用:0次
9 . 萘、四氢萘、十氢萘用途广泛,其转化关系为: ,该过程中能量变化如图所示,下列说法不正确的是:
,该过程中能量变化如图所示,下列说法不正确的是:
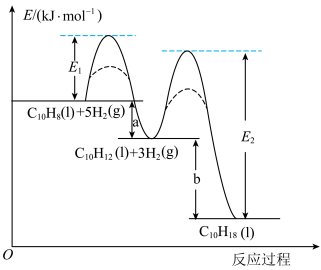
 ,该过程中能量变化如图所示,下列说法不正确的是:
,该过程中能量变化如图所示,下列说法不正确的是:
A.萘分子(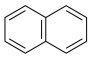 )的一氯代物有2种 )的一氯代物有2种 |
| B.E1、E2表示活化能,a的大小由E1决定,b的大小由E2决定 |
| C.实线表示无催化剂的反应过程,虚线表示有催化剂的反应过程 |
| D.物质的稳定性:十氢萘>四氢萘>萘 |
您最近一年使用:0次



