1 . 某实验小组探究 能否催化
能否催化 和
和 反应生成无毒物质。已知:①Ni、Fe的氢氧化物化学性质相似;②
反应生成无毒物质。已知:①Ni、Fe的氢氧化物化学性质相似;②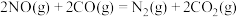
 。现采用如下两个装置完成探究实验(夹持装置略去)。下列有关说法正确的是
。现采用如下两个装置完成探究实验(夹持装置略去)。下列有关说法正确的是

 能否催化
能否催化 和
和 反应生成无毒物质。已知:①Ni、Fe的氢氧化物化学性质相似;②
反应生成无毒物质。已知:①Ni、Fe的氢氧化物化学性质相似;②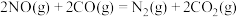
 。现采用如下两个装置完成探究实验(夹持装置略去)。下列有关说法正确的是
。现采用如下两个装置完成探究实验(夹持装置略去)。下列有关说法正确的是
| A.从理论上推断,高温有利于反应②自发进行 |
B.固体A成分可能为 、 、 |
| C.反应过程中装置1和2中气体均表现还原性 |
D.若实验证明 能够成功催化,则装置1中的方程式为: 能够成功催化,则装置1中的方程式为: |
您最近一年使用:0次
2 . 下列实验操作或做法正确且能达到目的的是
| 选项 | 实验操作或做法 | 目的 |
| A | 向2 mL0.1 mol/LNa2S溶液中滴加0.1 mol/LZnSO4溶液至不再有沉淀产生,再滴加几滴0.1 mol/LCuSO4溶液,出现黑色沉淀 | 验证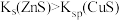 |
| B | 向各盛有5 mLH2O2溶液的两支试管中分别滴入2滴0.1 mol/L的FeCl3溶液和0.1 mol/L的CuSO4溶液 | 比较Fe3+与Cu2+对H2O2分解的催化效果 |
| C | 向盛有淀粉溶液的试管中加入少量稀硫酸,加热,再滴加几滴银氨溶液,水浴加热 | 证明淀粉已发生水解 |
| D | 先用稀硝酸酸化待测液,再滴加BaCl2溶液,生成白色沉淀 | 检验溶液中是否含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 下列实验设计及现象能达到实验目的的是
| 选项 | 实验目的 | 实验设计及现象 |
| A | 证明 气体中存在平衡 气体中存在平衡 | 压缩盛有 气体的注射器至原来体积的一半,红棕色变浅 气体的注射器至原来体积的一半,红棕色变浅 |
| B | 比较室温下 、 、 溶度积的大小 溶度积的大小 | 向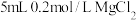 溶液中滴加少量NaOH溶液,充分振荡后,再滴加几滴 溶液中滴加少量NaOH溶液,充分振荡后,再滴加几滴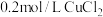 溶液,白色沉淀逐渐转化为蓝色 溶液,白色沉淀逐渐转化为蓝色 |
| C | 比较 和 和 的氧化性强弱 的氧化性强弱 | 常温下,向 溶液中加入 溶液中加入 溶液,将带火星的木条放在试管口,木条复燃 溶液,将带火星的木条放在试管口,木条复燃 |
| D | 证明反应生成乙烯 | 乙醇和浓硫酸共热至170℃,将产生的气体通入酸性高锰酸钾溶液中,溶液紫色褪去 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 用下列实验装置进行相应实验,能达到实验目的的是
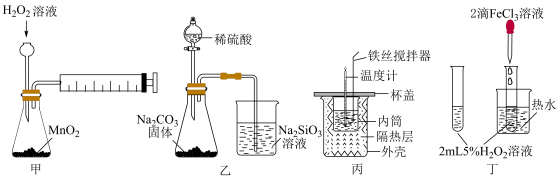

| A.用装置甲定量测定化学反应速率 |
| B.证明非金属性:S>C>Si |
| C.用装置丙准确测定中和反应的反应热 |
D.用装置丁验证 对 对 分解反应有催化作用 分解反应有催化作用 |
您最近一年使用:0次
名校
解题方法
5 . 某校化学小组探究 与
与 溶液的反应,进行了如下实验(以下实验过程中溶液体积变化忽略不计):
溶液的反应,进行了如下实验(以下实验过程中溶液体积变化忽略不计):
(1)对比实验i、ii、iii,说明反应速率与___________ 有关。
(2)为了探究淡黄色固体的成分,甲同学进行实验:取实验iv试管壁上的淡黄色固体,发现其微溶于乙醇,易溶于 ,淡黄色固体是
,淡黄色固体是___________ 。
(3)根据上述实验现象,甲同学猜测一定有单质碘生成,猜测的理论依据是___________ ,但实验中溶液始终没有变蓝。
(4)利用如图装置继续实验,证实了单质碘可以生成。实验现象是___________ 。
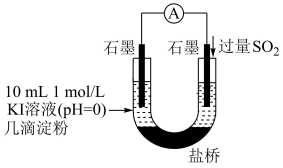
(5)对于实验i、ii、iii未能检测到单质碘,甲同学继续实验
根据(2)(4)(5)的实验现象,结合化学反应原理解释实验iv中始终未检测到单质碘的原因是___________ 。
(6)根据上述一系列实验,乙同学大胆猜测,整个反应中 起到了催化剂作用,为了证明乙同学的猜想正确,还需要的实验证据是
起到了催化剂作用,为了证明乙同学的猜想正确,还需要的实验证据是___________ 。
实验结果证实了猜想,则总反应的化学方程式是___________ 。
 与
与 溶液的反应,进行了如下实验(以下实验过程中溶液体积变化忽略不计):
溶液的反应,进行了如下实验(以下实验过程中溶液体积变化忽略不计):| 实验 | 实验操作 | 实验现象 |
| i | 取 淀粉 淀粉 溶液 溶液 ,通入 ,通入 至量 至量 | 溶液慢慢变为浅黄色 |
| ii | 取 淀粉 淀粉 溶液 溶液 ,通入 ,通入 至过量 至过量 | 溶液迅速变为黄色,略有浑浊 |
| iii | 取 淀粉 淀粉 溶液 溶液 (用盐酸酸化至 (用盐酸酸化至 ),通入 ),通入 至过量 至过量 | 溶液迅速变为黄色,有浑浊 |
| iv | 将实验iii中的黄色浊液进行离心分离 | 试管壁上附着淡黄色固体,溶液为黄色 |
(1)对比实验i、ii、iii,说明反应速率与
(2)为了探究淡黄色固体的成分,甲同学进行实验:取实验iv试管壁上的淡黄色固体,发现其微溶于乙醇,易溶于
 ,淡黄色固体是
,淡黄色固体是(3)根据上述实验现象,甲同学猜测一定有单质碘生成,猜测的理论依据是
(4)利用如图装置继续实验,证实了单质碘可以生成。实验现象是

(5)对于实验i、ii、iii未能检测到单质碘,甲同学继续实验
| 实验 | 实验操作 | 实验现象 |
| v | 将 通入蓝色的碘淀粉混合溶液中 通入蓝色的碘淀粉混合溶液中 | 溶液蓝色迅速褪去 |
| vi | 取实验iv离心后的黄色溶液少量,加入盐酸酸化的 溶液 溶液 | 生成白色沉淀 |
(6)根据上述一系列实验,乙同学大胆猜测,整个反应中
 起到了催化剂作用,为了证明乙同学的猜想正确,还需要的实验证据是
起到了催化剂作用,为了证明乙同学的猜想正确,还需要的实验证据是实验结果证实了猜想,则总反应的化学方程式是
您最近一年使用:0次
解题方法
6 . 近日,国际研究团队证明氮化钒纳米粒子这种高效选择性的催化剂,能够在温和的条件下实现电化学氮气还原反应,其反应历程如图所示:

下列叙述正确的是

下列叙述正确的是
| A.上述循环中,N原子形成化学键数目保持不变 |
| B.催化剂失活的原因之一是断裂了V—O |
| C.物质1是氮还原的催化剂,物质3是中间产物 |
| D.反应h中N元素被氧化,反应d断裂σ键 |
您最近一年使用:0次
解题方法
7 . 实验是探究物质性质的重要方法,下列实验中,操作及现象与得出的结论相一致的是
| 选项 | 实验目的 | 操作及现象 | 结论 |
| A | 探究不同催化剂的催化效率 | 两支试管中分别盛相同温度、相同浓度、相同体积的 溶液,分别滴加相同浓度、相同体积的 溶液,分别滴加相同浓度、相同体积的 溶液与 溶液与 溶液,滴加 溶液,滴加 溶液的试管中产生气体更快 溶液的试管中产生气体更快 |  对 对 分解的催化效率更高 分解的催化效率更高 |
| B | 验证反应 是可逆反应 是可逆反应 | 向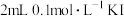 溶液中加入 溶液中加入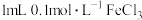 溶液,充分反应。取反应后试样,滴加 溶液,充分反应。取反应后试样,滴加 溶液,溶液变为红色;另取反应后试样,加入 溶液,溶液变为红色;另取反应后试样,加入 溶液,产生蓝色沉淀 溶液,产生蓝色沉淀 | 反应 是可逆反应 是可逆反应 |
| C | 检验 固体中是否含有单质Cu 固体中是否含有单质Cu | 取样,加入足量稀盐酸,观察现象 | 若有红色固体剩余,则说明样品中有单质Cu |
| D | 证明苯酚与溴水发生反应 | 向苯酚饱和溶液中滴加少量溴水,充分振荡 | 出现白色沉淀,说明苯酚与溴发生了反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . 某同学研究浓硝酸与KSCN溶液的反应,在通风橱中进行如下实验:

已知: 能被氧化为黄色的
能被氧化为黄色的 ,
, 可聚合为红色的
可聚合为红色的 。下列分析错误的是
。下列分析错误的是

已知:
 能被氧化为黄色的
能被氧化为黄色的 ,
, 可聚合为红色的
可聚合为红色的 。下列分析错误的是
。下列分析错误的是A. 被氧化为 被氧化为 的过程中,S的化合价升高 的过程中,S的化合价升高 |
B.分析①②③知, 聚合为 聚合为 的速率大于其被硝酸氧化的速率 的速率大于其被硝酸氧化的速率 |
C.取少量③中的溶液加入 溶液,产生白色沉淀,不能证明最终有 溶液,产生白色沉淀,不能证明最终有 生成,沉淀可能是碳酸钡 生成,沉淀可能是碳酸钡 |
D.①中改用溶有 的浓硝酸重复上述实验,溶液先变红后迅速褪色并产生大量红棕色气体,可能是 的浓硝酸重复上述实验,溶液先变红后迅速褪色并产生大量红棕色气体,可能是 气体对反应的进行起了催化作用 气体对反应的进行起了催化作用 |
您最近一年使用:0次
名校
9 . 煤和石油等化石燃料燃烧产生的NOx是大气中氮氧化物的主要来源。选择性催化还原脱硝技术被证明是控制尾部烟气中NOx排放的最成熟有效的技术之一,并得到了广泛应用。
回答下列问题:
Ⅰ.在相同时间内,三种催化剂下NO的转化率、NO2浓度随温度变化如图1所示。空速(空速是指规定的条件下,单位时间单位体积催化剂处理的气体量)的大小直接决定了烟气在催化剂表面的停留时间和装置的烟气处理能力。催化剂能够适应较大的空速,就可以在保证足够高的脱硝效率的前提下提高催化剂处理烟气的能力。相同时间内MnCeZr催化剂在不同空速下NO的转化率随温度变化如图2所示。

(1)①根据两图分析,选取工业脱硝的最佳反应条件为______ 。
②350~400℃产生较多NO2的原因为______ 。
(2)通过改善催化剂的结构特性可以使脱硝效率得到提升.较低温度下,MnCeZr催化剂的脱硝效率高于CeZr催化剂,说明主要是______ 的存在改善了催化剂的低温活性.在MnCe催化剂X点正反应速率______ (填“>”“<”或“=”)逆反应速率,说明理由:______ 。
Ⅱ.回答下列问题:
(3)氧气的添加可以使较低温度下催化剂的脱硝效率迅速提高,氧气会与未反应的氨气反应。
i.4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H1;
4NO(g)+6H2O(g) △H1;
ii.2NO(g)+O2(g) 2NO2(g) △H2;
2NO2(g) △H2;
iii.2NH3(g)+NO(g)+NO2(g) 2N2(g)+3H2O(g) △H3;
2N2(g)+3H2O(g) △H3;
iv.4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g) △H4=
4N2(g)+6H2O(g) △H4=_____ 。
(4)已知反应i和反应iv为竞争反应,若只考虑这两个反应,相同时间内,NH3出口/入口比值及出口NO、NO2浓度随温度变化如图3所示。体积为2L的恒容密闭容器中,NH3、O2均以4mol投料,250℃已达到平衡,则此时反应iv的平衡常数为______ mol/L(列出计算式即可)。

回答下列问题:
Ⅰ.在相同时间内,三种催化剂下NO的转化率、NO2浓度随温度变化如图1所示。空速(空速是指规定的条件下,单位时间单位体积催化剂处理的气体量)的大小直接决定了烟气在催化剂表面的停留时间和装置的烟气处理能力。催化剂能够适应较大的空速,就可以在保证足够高的脱硝效率的前提下提高催化剂处理烟气的能力。相同时间内MnCeZr催化剂在不同空速下NO的转化率随温度变化如图2所示。

(1)①根据两图分析,选取工业脱硝的最佳反应条件为
②350~400℃产生较多NO2的原因为
(2)通过改善催化剂的结构特性可以使脱硝效率得到提升.较低温度下,MnCeZr催化剂的脱硝效率高于CeZr催化剂,说明主要是
Ⅱ.回答下列问题:
(3)氧气的添加可以使较低温度下催化剂的脱硝效率迅速提高,氧气会与未反应的氨气反应。
i.4NH3(g)+5O2(g)
 4NO(g)+6H2O(g) △H1;
4NO(g)+6H2O(g) △H1;ii.2NO(g)+O2(g)
 2NO2(g) △H2;
2NO2(g) △H2;iii.2NH3(g)+NO(g)+NO2(g)
 2N2(g)+3H2O(g) △H3;
2N2(g)+3H2O(g) △H3;iv.4NH3(g)+4NO(g)+O2(g)
 4N2(g)+6H2O(g) △H4=
4N2(g)+6H2O(g) △H4=(4)已知反应i和反应iv为竞争反应,若只考虑这两个反应,相同时间内,NH3出口/入口比值及出口NO、NO2浓度随温度变化如图3所示。体积为2L的恒容密闭容器中,NH3、O2均以4mol投料,250℃已达到平衡,则此时反应iv的平衡常数为

您最近一年使用:0次
名校
解题方法
10 . 下列操作能达到实验目的的是
| 实验操作 | 实验目的 | |
| A | 相同温度下,向两支盛有相同体积不同浓度H2O2溶液的试管中分别滴入适量相同浓度的CuSO4溶液和FeCl3溶液 | 探究Cu2+、Fe3+对H2O2分解速率的影响 |
| B | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| C | 先在托盘上各放一张滤纸,然后在右盘上添加2g砝码,左盘上添加NaOH固体 | 称取2.0gNaOH固体 |
| D | 分别取甲苯和苯与酸性KMnO4溶液反应,观察酸性KMnO4溶液的褪色情况 | 证明甲苯中的甲基能够活化苯环 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-04-12更新
|
744次组卷
|
4卷引用:山东省济南市历城第二中学2021-2022学年高三下学期二轮复习测评联合考试(二模) 化学试题
山东省济南市历城第二中学2021-2022学年高三下学期二轮复习测评联合考试(二模) 化学试题(已下线)化学-2022年高考考前押题密卷(湖南卷)湖北省宜昌英杰学校2021-2022学年高三上学期9月月考化学试题巩固训练12



