23-24高三上·天津静海·阶段练习
名校
解题方法
1 . 用下列实验装置进行相应实验,能达到实验目的的是
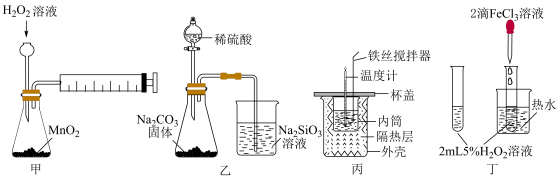

| A.用装置甲定量测定化学反应速率 |
| B.证明非金属性:S>C>Si |
| C.用装置丙准确测定中和反应的反应热 |
D.用装置丁验证 对 对 分解反应有催化作用 分解反应有催化作用 |
您最近一年使用:0次
2023·湖南娄底·模拟预测
解题方法
2 . 近日,国际研究团队证明氮化钒纳米粒子这种高效选择性的催化剂,能够在温和的条件下实现电化学氮气还原反应,其反应历程如图所示:

下列叙述正确的是

下列叙述正确的是
| A.上述循环中,N原子形成化学键数目保持不变 |
| B.催化剂失活的原因之一是断裂了V—O |
| C.物质1是氮还原的催化剂,物质3是中间产物 |
| D.反应h中N元素被氧化,反应d断裂σ键 |
您最近一年使用:0次
名校
解题方法
3 . 下列操作能达到实验目的的是
| 实验操作 | 实验目的 | |
| A | 相同温度下,向两支盛有相同体积不同浓度H2O2溶液的试管中分别滴入适量相同浓度的CuSO4溶液和FeCl3溶液 | 探究Cu2+、Fe3+对H2O2分解速率的影响 |
| B | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| C | 先在托盘上各放一张滤纸,然后在右盘上添加2g砝码,左盘上添加NaOH固体 | 称取2.0gNaOH固体 |
| D | 分别取甲苯和苯与酸性KMnO4溶液反应,观察酸性KMnO4溶液的褪色情况 | 证明甲苯中的甲基能够活化苯环 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-04-12更新
|
744次组卷
|
4卷引用:巩固训练12
巩固训练12山东省济南市历城第二中学2021-2022学年高三下学期二轮复习测评联合考试(二模) 化学试题(已下线)化学-2022年高考考前押题密卷(湖南卷)湖北省宜昌英杰学校2021-2022学年高三上学期9月月考化学试题
21-22高二下·浙江·阶段练习
解题方法
4 . 下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 检验某无色溶液中是否含有 | 取少量该溶液于试管中,加稀硝酸酸化,再加入硝酸钡溶液 | 若有白色沉淀生成,则该溶液中一定含有 |
| B | 探究X是否属于醛类物质 | 向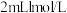 的 的 溶液,加入5滴 溶液,加入5滴 的 的 溶液,振荡后再加入 溶液,振荡后再加入 有机物X,加热 有机物X,加热 | 出现砖红色沉淀,则X可能是醛类物质 |
| C | 探究 和 和 的溶解度大小 的溶解度大小 | 向 溶液中加入一定量的 溶液中加入一定量的 溶液,充分反应后再加少量的 溶液,充分反应后再加少量的 溶液 溶液 | 若先生成白色沉淀,后产生蓝色沉淀,则证明 比 比 溶解度小 溶解度小 |
| D | 探究不同金属离于对 分解速率的影响 分解速率的影响 | 取2支试管,向2支试管中各加入 溶液,分别向试管中各加入 溶液,分别向试管中各加入 溶液和 溶液和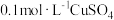 溶液 溶液 | 相同时间内产生气泡多的,则催化效果好 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021高三·全国·专题练习
解题方法
5 . 某兴趣小组在利用图所示装置做铜与稀硝酸反应的实验中,发现开始时气泡产生速率非常慢,一段时间后速率明显加快,烧瓶内溶液呈浅蓝色并不断加深,液面上方的气体颜色也在不断加深。该小组同学拟通过实验探究反应速率变化的原因。
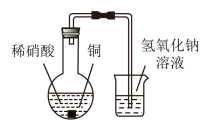
(1)图中铜与稀硝酸反应的离子方程式为___________ 。
(2)图中NaOH溶液能够吸收的有害气体是___________ 。
(3)小组同学提出了如下假设并设计实验探究:
I.甲同学认为反应速率变化的原因可能是反应放热导致溶液温度升高所致,故测定反应过程中溶液不同时间的温度,结果如下表:
结合实验目的和表中数据,你得出的结论是___________ 。
II.乙同学认为生成的Cu2+对反应有催化作用,为验证此假设,取A、B两支试管分别加入等量的铜片和稀硝酸,那么最好是在其中一支试管中加入少量的___________ (填序号)。
A.硝酸铜晶体 B.硝酸铜溶液 C.硫酸铜晶体 D.硫酸铜溶液
然后对比两支试管的反应,发现现象基本相同。故得出结论:Cu2+并不是反应的催化剂
III.丙同学根据现象推测反应过程中还有少量______ 生成,进而认为该物质对反应有催化作用,如图所示,丙同学从a处通入该物质后,发现左管中产生气泡速率明显快于右管。小组同学得出最后结论:这种物质对铜和稀硝酸的反应有催化作用。
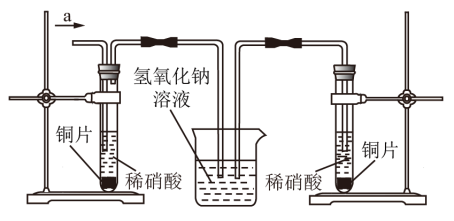
(4)实验结束后,发现试管中溶液呈绿色,而不显蓝色。部分同学认为是该溶液中Cu2+的浓度较高所致,另一部分同学认为是该溶液中溶解了通入的物质。丁同学设计了一个实验方案证明后者的推测更为合理。(在表格中写出该同学可能的实验操作和实验现象)

(1)图中铜与稀硝酸反应的离子方程式为
(2)图中NaOH溶液能够吸收的有害气体是
(3)小组同学提出了如下假设并设计实验探究:
I.甲同学认为反应速率变化的原因可能是反应放热导致溶液温度升高所致,故测定反应过程中溶液不同时间的温度,结果如下表:
| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 35 | 50 | 60 | 70 | 80 |
| 温度/℃ | 25 | 26 | 26 | 26 | 26 | 26 | 26.5 | 27 | 27 | 27 | 27 |
II.乙同学认为生成的Cu2+对反应有催化作用,为验证此假设,取A、B两支试管分别加入等量的铜片和稀硝酸,那么最好是在其中一支试管中加入少量的
A.硝酸铜晶体 B.硝酸铜溶液 C.硫酸铜晶体 D.硫酸铜溶液
然后对比两支试管的反应,发现现象基本相同。故得出结论:Cu2+并不是反应的催化剂
III.丙同学根据现象推测反应过程中还有少量

(4)实验结束后,发现试管中溶液呈绿色,而不显蓝色。部分同学认为是该溶液中Cu2+的浓度较高所致,另一部分同学认为是该溶液中溶解了通入的物质。丁同学设计了一个实验方案证明后者的推测更为合理。(在表格中写出该同学可能的实验操作和实验现象)
| 操作 | 现象 |
您最近一年使用:0次
2020·河北唐山·二模
名校
解题方法
6 . 下列实验目的能实现的是
| 实验目的 | 操作步骤及现象 | |
| A | 研究浓度对化学平衡的影响 | 2mL 0.001 mol·L-1FeCl3溶液与2mL 0.01 mol·L-1KSCN溶液混合后等分到两支试管,一支加入2mL 0.1 mol·L-1FeCl3溶液,另一支加入2mL H2O,第一支试管中溶液颜色较深 |
| B | 证明MnO2是双氧水分解的催化剂 | 准备两支各装有3%H2O2溶液5mL的试管,一支作对照,向另一支加入1.0g MnO2,发现加入MnO2的试管迅速产生大量气泡,证明MnO2是催化剂 |
| C | 比较AgCl和AgI溶度积的大小 | 向试管中加入2mL 0.1 mol·L-1AgNO3溶液,滴加0.1 mol·L-1NaCl溶液3mL,再滴加0.1 mol·L-1KI溶液,沉淀由白色变黄色 |
| D | 研究浓度对反应速率的影响 | 分别向盛有2 mL 0.1 mol·L-1和2mL 0.2 mol·L-1 KMnO4溶液的两支试管中加入5 mL 0.1 mol·L-1 H2C2O4,第一支试管中溶液先褪色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-06-29更新
|
218次组卷
|
3卷引用:押山东卷第11题 关于表格实验题的考查-备战2021年高考化学临考题号押题(山东卷)
(已下线)押山东卷第11题 关于表格实验题的考查-备战2021年高考化学临考题号押题(山东卷)河北省唐山市2020届高三第二次模拟考试理综化学试题黑龙江省佳木斯市第十二中学2022-2023学年高二上学期期中考试化学试题
解题方法
7 . 下列实验能达到相应目的的是
A. 将乙二醇转化为乙二酸 将乙二醇转化为乙二酸 |
B. 比较氯化铁和二氧化锰对H2O2分解反应的催化效果 比较氯化铁和二氧化锰对H2O2分解反应的催化效果 |
C. 证明稀硝酸与铜反应时表现出氧化性 证明稀硝酸与铜反应时表现出氧化性 |
D. 用SO2与Ba(NO3)2反应获得BaSO3沉淀 用SO2与Ba(NO3)2反应获得BaSO3沉淀 |
您最近一年使用:0次
解题方法
8 . 下列实验方案不能达到相应实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A. | 证明Fe3+的催化效果强于Cu2+ | 在两支试管中各加2ml5%H2O2溶液,再分别滴入0.1mol/LFeCl3和0.01mol/LCuSO4溶液各1ml |
| B. | 探究浓硫酸的吸水性 | 向表面皿中加入少量胆矾,再加入约3ml浓硫酸,搅拌,观察实验现象 |
| C. | 验证SO2的还原性 | 将SO2气体通入溴水中,观察溴水是否褪色 |
| D. | 检验新制氯水的氧化性和酸性 | 向少量紫色石蕊试液中逐滴加入新制氯水,边加边振荡,观察溶液颜色变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
13-14高一下·四川雅安·期中
名校
解题方法
9 . 影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究。
实验一:他们只利用Cu、Fe、Mg和不同浓度的硫酸(0.5 mol·L-1、2 mol·L-1、18.4 mol·L-1)设计实验方案来研究影响化学反应速率的因素。甲同学的实验报告如下表:
(1)甲同学表中实验步骤②为_________________________________________ 。
(2)甲同学的实验目的是_____________ ;要得出正确的实验结论,还需控制的实验条件是____________ 。乙同学为了更精确地研究浓度对反应速率的影响,利用如图所示装置进行定量实验。
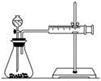
(3)乙同学在实验中应该测定的数据是___________________________________________________ 。
(4)乙同学完成该实验应选用的实验药品是________ ,该实验中不选用某浓度的硫酸,理由是___________ 。
实验二:已知 2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
(5)针对上述实验现象,丙同学认为KMnO4与H2C2O4反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你猜想还可能是______________ 的影响。
(6)若用实验证明你的猜想,除高锰酸钾酸性溶液、草酸溶液外,还需要选择的试剂最合理的是________ (填字母)。
A.硫酸钾 B.硫酸锰 C.二氯化锰 D.水
实验一:他们只利用Cu、Fe、Mg和不同浓度的硫酸(0.5 mol·L-1、2 mol·L-1、18.4 mol·L-1)设计实验方案来研究影响化学反应速率的因素。甲同学的实验报告如下表:
| 实验步骤 | 现象 | 结论 |
| ①分别取等体积的2 mol·L-1的硫酸于试管中 | 反应速率Mg>Fe,Cu不反应 | 金属的性质越活泼,反应速率越快 |
| ②____________ | 反应物浓度越大,反应速率越快 |
(1)甲同学表中实验步骤②为
(2)甲同学的实验目的是

(3)乙同学在实验中应该测定的数据是
(4)乙同学完成该实验应选用的实验药品是
实验二:已知 2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
(5)针对上述实验现象,丙同学认为KMnO4与H2C2O4反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你猜想还可能是
(6)若用实验证明你的猜想,除高锰酸钾酸性溶液、草酸溶液外,还需要选择的试剂最合理的是
A.硫酸钾 B.硫酸锰 C.二氯化锰 D.水
您最近一年使用:0次
2016-12-09更新
|
1625次组卷
|
8卷引用:第15讲 化学反应速率-2021年高考化学一轮复习名师精讲练
(已下线)第15讲 化学反应速率-2021年高考化学一轮复习名师精讲练(已下线)2013-2014四川省雅安中学下学期期中考试高一化学试卷(已下线)2013-2014重庆市重庆一中下学期期中考试高二化学试卷新疆阿勒泰地区2019-2020学年高一下学期期末考试化学(B)试题(已下线)第二章 化学反应速率和化学平衡(能力提升)-2020-2021学年高二化学单元测试定心卷(人教版选修4)内蒙古包头市第一中学2020-2021学年高二上学期第一次月考化学试题江苏省海安市2020-2021学年高二上学期期中考试化学试题江西省丰城市第九中学2021-2022学年高二上学期期中考试(日新班)化学试题
2024·浙江宁波·二模
解题方法
10 . 邻二醇在酸的作用下能转化为酮(或醛),反应的分步机理和协同机理如下:
①当碳原子上连有推电子基团时,有利于碳正离子(通常指的是价层只有6个电子的碳阳离子,是活性中间体)的稳定。
②2,3-二甲基-2,3-丁二醇与酸反应,对应的中间体和生成物相对能量(kJ/mol)如下:
③当碳正离子的相邻碳上有两个不同芳基时,迁移的相对速率与芳基的关系如下表:
下列说法不正确 的是

①当碳原子上连有推电子基团时,有利于碳正离子(通常指的是价层只有6个电子的碳阳离子,是活性中间体)的稳定。
②2,3-二甲基-2,3-丁二醇与酸反应,对应的中间体和生成物相对能量(kJ/mol)如下:
| 过渡态1 | 过渡态2 | 生成物 | |
| 分步机理 | 0.00 | 30.1 | 38.3 | -82.3 |
| 协同机理 | 0.00 | 44.0 | - | -82.3 |
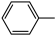
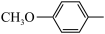
| 芳基 |
|
|
|
| 相对速率 | 0.7 | 1 | 500 |
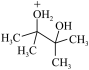
A.酸性条件下,2,3-二甲基-2,3-丁二醇转化为 主要以分步机理进行 主要以分步机理进行 |
| B.上述转化过程中酸可提高反应速率,但不影响平衡产率 |
| C.乙二醇在酸性条件下只能通过协同机理生成醛,原因是碳正离子中间体不稳定 |
D.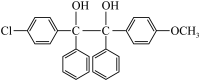 在酸的作用下,产物主要形式为 在酸的作用下,产物主要形式为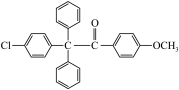 |
您最近一年使用:0次