下列实验目的能实现的是
| 实验目的 | 操作步骤及现象 | |
| A | 研究浓度对化学平衡的影响 | 2mL 0.001 mol·L-1FeCl3溶液与2mL 0.01 mol·L-1KSCN溶液混合后等分到两支试管,一支加入2mL 0.1 mol·L-1FeCl3溶液,另一支加入2mL H2O,第一支试管中溶液颜色较深 |
| B | 证明MnO2是双氧水分解的催化剂 | 准备两支各装有3%H2O2溶液5mL的试管,一支作对照,向另一支加入1.0g MnO2,发现加入MnO2的试管迅速产生大量气泡,证明MnO2是催化剂 |
| C | 比较AgCl和AgI溶度积的大小 | 向试管中加入2mL 0.1 mol·L-1AgNO3溶液,滴加0.1 mol·L-1NaCl溶液3mL,再滴加0.1 mol·L-1KI溶液,沉淀由白色变黄色 |
| D | 研究浓度对反应速率的影响 | 分别向盛有2 mL 0.1 mol·L-1和2mL 0.2 mol·L-1 KMnO4溶液的两支试管中加入5 mL 0.1 mol·L-1 H2C2O4,第一支试管中溶液先褪色 |
| A.A | B.B | C.C | D.D |
2020·河北唐山·二模 查看更多[3]
黑龙江省佳木斯市第十二中学2022-2023学年高二上学期期中考试化学试题(已下线)押山东卷第11题 关于表格实验题的考查-备战2021年高考化学临考题号押题(山东卷)河北省唐山市2020届高三第二次模拟考试理综化学试题
更新时间:2020-06-29 21:26:51
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】某密闭容器中的反应: 3H2(g) + N2(g)  2NH3(g) △H<0,正反应速率随时间变化的情况如图所示,判断下列有关t1 时刻条件变化的说法可能正确的是
2NH3(g) △H<0,正反应速率随时间变化的情况如图所示,判断下列有关t1 时刻条件变化的说法可能正确的是

 2NH3(g) △H<0,正反应速率随时间变化的情况如图所示,判断下列有关t1 时刻条件变化的说法可能正确的是
2NH3(g) △H<0,正反应速率随时间变化的情况如图所示,判断下列有关t1 时刻条件变化的说法可能正确的是
| A.其他条件不变,增大NH3浓度的同时减小N2浓度 |
| B.其他条件不变,再充入N2和H2 |
| C.其他条件不变,扩大容器的体积 |
| D.其他条件不变,降低反应温度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关化学反应速率和化学平衡的叙述错误的是
| A.增大反应物的浓度,活化分子的百分含量不变,反应速率增大 |
| B.锌与足量稀硫酸反应,加入少量硫酸铜粉末,反应速率增大,但产生氢气的量减少 |
| C.平衡正向移动时,反应物转化率可能减小 |
| D.锌与硫酸反应时,硫酸的浓度越大,产生 H2的速率越大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列实验的现象描述和结论都正确的是
| 实验操作 | 实验现象 | 实验结论 | |
| A | 将水滴入盛有Na2O2固体的试管中,立即把带火星的木条放在试管口 | 可观察到有气泡产生,木条复燃 | Na2O2固体遇水产生O2 |
| B | 向盛有10mL 0.1mol/L AgNO3溶液的试管中滴加几滴0.1mol/L KCl溶液,再向其中滴加几滴0.1mol/L KI溶液 | 先观察到白色沉淀,后沉淀颜色变为黄色 | Ksp(AgCl)> Ksp(AgI) |
| C | 向两支盛有少量溴的四氯化碳溶液的试管中分别加入适量苯和通入足量乙烯 | 溶液均褪色 | 溴与苯和乙烯都能发生反应 |
| D | 向两支盛有4mL0.01mol/L KMnO4溶液的试管中分别加入2mL 0.1mol/L和2mL 0.2mol/LH2C2O4溶液 | 前者比后者褪色快 | 其他条件不变,反应物浓度增加,反应速率增大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】利用可再生能源提供的能量可高温共电解H2O和CO2,并实现清洁燃料的制备。其工作流程和反应原理如图所示:不正确 的是。
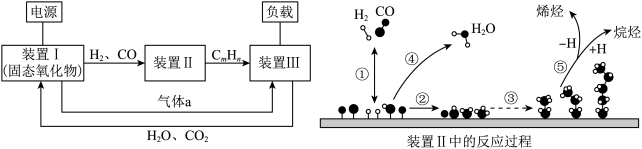
A.装置I中生成气体a的电极反应为 |
| B.装置Ⅱ中过程①~③均有极性键的断裂和生成 |
C.装置Ⅲ中消耗 理论上转移 理论上转移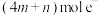 |
| D.该过程中CO2的循环利用率理论上可达100% |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关实验内容、实验装置和对应的实验目的均正确的是
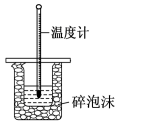 |  | 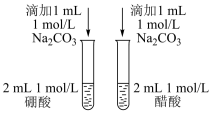 | 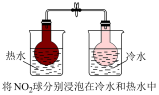 |
| A.可用于测定中和热 | B.验证CuCl2对双氧水分解的催化作用 | C.比较醋酸和硼酸的酸性强弱 | D.比较不同温度对化学反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】对于反应
 ,下列说法正确的是
,下列说法正确的是

 ,下列说法正确的是
,下列说法正确的是| A.该反应在任何温度下均能自发进行 |
B.反应的平衡常数可表示为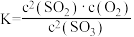 |
| C.使用高效催化剂能降低反应的活化能和焓变 |
D.升温、加压和使用催化剂能增大 的生成速率 的生成速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验操作和现象及实验结论均正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 向浓度均为0.1mol·L-1的KCl和KI的混合溶液中滴加少量AgNO3溶液,先出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| B | 向两支盛有2mL不同浓度Na2SO3溶液的试管中同时加入1mL2%双氧水,观察实验现象 | 探究浓度对化学反应速率的影响 |
| C | 将Na2S2O3溶液与硫酸两种溶液混合后再用水浴加热,观察出现浑浊所用的时间 | 探究温度对化学反应速率的影响 |
| D | 室温用pH试纸测同浓度的NaClO和CH3COONa溶液的pH,pH(NaClO)>pH(CH3COONa) | 酸性:HClO>CH3COOH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在一定温度下,10mL 1.0mol/L H2SO4与Zn粒发生反应。不同时刻测定生成H2的体积(已折算为标准状况)如下表。
下列叙述不正确的是(溶液体积变化忽略不计)
| t/min | 0 | 1 | 3 | 5 | 7 | 9 |
| V(H2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)
| A.0~5 min的平均反应速率:v(H2SO4)≈0.02mol/(L•min) |
| B.5~9 min的平均反应速率:v(H2SO4)< 0.02mol/(L•min) |
| C.反应到5 min时,c(H2SO4)=0.010mol/L |
| D.反应到5 min时,Zn溶解了65mg |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】25℃,将0.1 mol BaSO4粉末置于盛有500 mL蒸馏水的烧杯中,然后烧杯中加入Na2CO3固体(忽视溶液体积的变化)并充分搅拌,慢慢加入Na2CO3固体的过程中,溶液中几种离子的浓度变化曲线如图所示,下列说法中正确的是


| A.开始加入Na2CO3固体立即有Ba2CO3固体生成 |
B.向c( )=c( )=c( )的混合溶液中滴加BaCl2溶液时,先生成BaCO3沉淀 )的混合溶液中滴加BaCl2溶液时,先生成BaCO3沉淀 |
C.BaSO4(s)+ (aq) (aq) BaCO3(s)+ BaCO3(s)+ (aq)的 (aq)的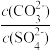 =0.04 =0.04 |
| D.若使0.05 mol BaSO4全部转化为BaCO3,至少要加入1.30 mol Na2CO3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】“灵感是在劳动时候产生的”。下列劳动项目与所写反应无关联的是
| 选项 | 劳动项目 | 反应 |
| A | 用硫酸铜给游泳池消毒 |  |
| B | 用稀盐酸洗涤铜铲的锈渍 |  |
| C | 用热的纯碱溶液除去炊具上的油污 |  |
| D | 用石膏改良盐碱地 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次


 +H2O
+H2O +2H2O
+2H2O

