下列有关化学反应速率和化学平衡的叙述错误的是
| A.增大反应物的浓度,活化分子的百分含量不变,反应速率增大 |
| B.锌与足量稀硫酸反应,加入少量硫酸铜粉末,反应速率增大,但产生氢气的量减少 |
| C.平衡正向移动时,反应物转化率可能减小 |
| D.锌与硫酸反应时,硫酸的浓度越大,产生 H2的速率越大 |
更新时间:2021-02-01 13:44:42
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列实验方案中不能达到相应实验目的的是:
| A | B | C | D | |
| 方案 | 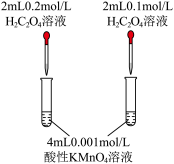 | 在2mL1mol/LNaOH溶液中,加入5滴1mol/L氯化镁溶液,有白色沉淀,再加入5滴氯化铁溶液,观察沉淀颜色 | 实验室制备氢气,用粗锌代替纯锌与稀硫酸反应,反应速率加快 | 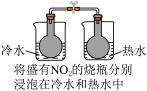 |
| 目的 | 探究浓度对化学反应速率的影响 | 探究沉淀溶解平衡的移动 | 探究形成原电池对反应速率的影响 | 探究温度对化学平衡的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】根据下列操作和现象,所得结论正确的是
| 实验操作及现象 | 实验结论 | |
| A | 向2mL5%的双氧水中分别滴加2滴0.1mol/L的Fe2(SO4)3和0.1mol/L的CuSO4溶液,前者产生气泡较快 | 对双氧水分解催化效率:Fe3+>Cu2+ |
| B | 向2mL0.1mol/L酸性KMnO4溶液中分别滴加3mL0.1mol/L和3mL0.2mol/L的H2C2O4溶液,后者首先褪色(提示:反应的部分关系为2MnO4-+5H2C2O4—2Mn2++10CO2) | 其他条件不变时,H2C2O4的浓度越大,化学反应速率越快 |
| C | 取两支试管a和b,各加入5ml0.1mol/LNa2S2O3溶液;另取两支试管c和d,各加入5ml0.1mol/LH2SO4溶液;将a、d放入热水浴中,b、c放入冷水浴中,一段时间后分别混合,热水浴中先出现浑浊。(S2O32-+2H+=SO2↑+S↓+H2O) | 温度越高,反应速率越快 |
| D | 用3mL稀H2SO4溶液与足量Zn反应,当气泡稀少时,加入1mL浓H2SO4,又迅速产生较多气泡 | H2SO4浓度增大,反应速率加快 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】已知硫代硫酸钠在酸性条件下会发生反应: ,下表中的两种溶液混合,出现浑浊的先后顺序是( )
,下表中的两种溶液混合,出现浑浊的先后顺序是( )
 ,下表中的两种溶液混合,出现浑浊的先后顺序是( )
,下表中的两种溶液混合,出现浑浊的先后顺序是( )| 组号 | 两种溶液的温度 |  溶液的体积、浓度 溶液的体积、浓度 | 稀硫酸的体积、浓度 |
| ① | 15℃ | 10mL0.1mol/L | 50mL0.05mol/L |
| ② | 15℃ | 10mL0.05mol/L | 10mL0.1mol/L |
| ③ | 25℃ | 10mL0.05mol/L | 10mL0.1mol/L |
| ④ | 25℃ | 10mL0.1mol/L | 30mL0.07mol/L |
| A.④①②③ | B.③④②① |
| C.④③②① | D.④③①② |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】向某密闭容器中加入足量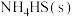 ,发生反应
,发生反应
 ,在某温度下达到平衡,下列说法正确的是
,在某温度下达到平衡,下列说法正确的是
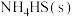 ,发生反应
,发生反应
 ,在某温度下达到平衡,下列说法正确的是
,在某温度下达到平衡,下列说法正确的是| A.升高温度,一段时间后气体平均相对分子质量增大 |
B.容器体积不变,移走一小部分 固体,随后气体分子数将减少 固体,随后气体分子数将减少 |
| C.温度不变,缩小容器体积,重新平衡后气体压强将增大 |
| D.保持温度和压强不变,充入氦气,随后固体质量将减少 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在水溶液中,重铬酸钾K2Cr2O7存在以下平衡:Cr2O72-+H2O 2CrO42-+2H+,下列说法正确的是( )
2CrO42-+2H+,下列说法正确的是( )
 2CrO42-+2H+,下列说法正确的是( )
2CrO42-+2H+,下列说法正确的是( )| A.向该溶液中加入过量浓NaOH溶液后,溶液呈橙红色 |
| B.该反应是氧化还原反应 |
| C.向该溶液中滴加适量的浓硫酸,平衡向逆反应方向移动,再次达到平衡后,氢离子浓度比原溶液大 |
| D.该反应的平衡常数表达式是K=c2(CrO42-)c2(H+)/c(Cr2O72-)c(H2O) |
您最近一年使用:0次

 ,一段时间后达到化学平衡状态,下列说法正确的是
,一段时间后达到化学平衡状态,下列说法正确的是
 ,反应速率加快
,反应速率加快 、
、 的浓度之和保持不变时,说明该反应达到了平衡状态
的浓度之和保持不变时,说明该反应达到了平衡状态 ,达新平衡后
,达新平衡后

