1 . 一定条件下, 可催化
可催化 在水中发生反应,过程分为两步
在水中发生反应,过程分为两步
i.
ⅱ.
某小组设计以下实验探究上述反应速率的影响因素(如图),
已知:(1)试管①中是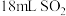 的稀溶液;②③④中是
的稀溶液;②③④中是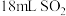 的饱和溶液
的饱和溶液
(2)四组实验中溶液出现混浊所用时间:①>②>③>④

下列说法错误的是
 可催化
可催化 在水中发生反应,过程分为两步
在水中发生反应,过程分为两步i.

ⅱ.

某小组设计以下实验探究上述反应速率的影响因素(如图),
已知:(1)试管①中是
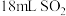 的稀溶液;②③④中是
的稀溶液;②③④中是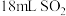 的饱和溶液
的饱和溶液(2)四组实验中溶液出现混浊所用时间:①>②>③>④

下列说法错误的是
A.通过实验①②可探究 的浓度对反应速率的影响 的浓度对反应速率的影响 |
B.实验①③可证明酸性条件下 的催化效果更好 的催化效果更好 |
C.实验④开始加入 ,发生反应ⅱ生成 ,发生反应ⅱ生成 和 和 ,加快了反应速率 ,加快了反应速率 |
D.总反应为: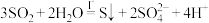 |
您最近一年使用:0次
2 . 中国科学院科研团队研究表明,在常温常压和可见光下,基于LDH(一种固体催化剂)合成NH3的原理如图所示。下列关于该过程的说法不正确的是
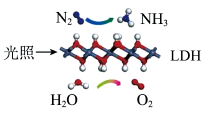

| A.该过程属于氮的固定 |
| B.LDH加快了反应的速率 |
| C.氧化剂和还原剂的物质的量之比为1∶3 |
| D.该过程证明,N2和H2合成NH3的反应是放热反应 |
您最近一年使用:0次
名校
解题方法
3 . 下列设计的实验方案能达到相应实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 探究化学反应的限度 | 取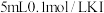 溶液,滴加 溶液,滴加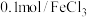 溶液 溶液 滴,充分反应,可根据溶液中既含 滴,充分反应,可根据溶液中既含 又含 又含 的实验事实判断该反应是可逆反应 的实验事实判断该反应是可逆反应 |
| B | 比较Mg与Al的金属活动性 | 常温下,将Mg、Al与NaOH溶液组成原电池 |
| C | 探究不同催化剂对同一反应速率的影响 | 相同条件下,向两支盛有等体积等浓度 溶液的试管中分别加入少量 溶液的试管中分别加入少量 粉末和5滴 粉末和5滴 的 的 溶液 溶液 |
| D | 证明在相同温度下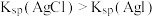 | 向盛有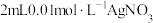 溶液的试管中滴加2滴 溶液的试管中滴加2滴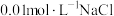 溶液,有白色沉淀生成,再向其中滴加2滴 溶液,有白色沉淀生成,再向其中滴加2滴 溶液,产生黄色沉淀 溶液,产生黄色沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 . 下列实验方案设计、现象和结论都正确的是
| 选项 | 目的 | 方案设计和现象 | 结论 |
| A | 证明 是弱电解质 是弱电解质 | 用pH计分别测量醋酸溶液和盐酸的pH,醋酸溶液的pH大 |  是弱电解质 是弱电解质 |
| B | 探究压强对化学平衡的影响 | 先将注射器充满 气体,然后将活塞往里推,注射器内气体颜色加深 气体,然后将活塞往里推,注射器内气体颜色加深 | 加压,平衡向生成 气体的方向移动 气体的方向移动 |
| C | 探究浓度对化学平衡的影响 | 向 (黄色)溶液中缓慢滴加硫酸,溶液由黄色变为橙色 (黄色)溶液中缓慢滴加硫酸,溶液由黄色变为橙色 | 增大 浓度,平衡向生成 浓度,平衡向生成 (橙色)方向移动 (橙色)方向移动 |
| D | 比较 、 、 催化分解 催化分解 的效率 的效率 | 向两份等浓度、等体积且等温的过氧化氢溶液中分别加入2滴等浓度的 溶液和 溶液和 溶液,前者产生气泡较快 溶液,前者产生气泡较快 | 催化效率: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 完成下列问题
(1)实验一:已知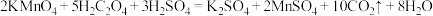 。在酸性高锰酸钾溶液与草酸(
。在酸性高锰酸钾溶液与草酸( )溶液反应时,发现开始一段时间,反应速度较快,溶液褪色不明显,但不久突然褪色,反应速度明显加快。
)溶液反应时,发现开始一段时间,反应速度较快,溶液褪色不明显,但不久突然褪色,反应速度明显加快。
①针对上述实验现象,小组同学认为 与
与 反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你认为还可能是
反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你认为还可能是___________ 的影响。
②若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,还需要的试剂最合理的是___________ (填字母)。
A.硫酸钾 B.硫酸锰 C.二氧化锰 D.水
(2)实验二:探究 和
和 混合时生成
混合时生成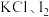 和
和 的反应存在一定的限度。
的反应存在一定的限度。
Ⅰ.向 溶液中滴加
溶液中滴加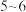 滴
滴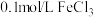 溶液,充分反应后,将所得溶液分成甲、乙两等份;
溶液,充分反应后,将所得溶液分成甲、乙两等份;
Ⅱ.向甲中滴加 ,充分振荡;
,充分振荡;
Ⅲ.向乙中滴加试剂X。
请回答下列问题:
①步骤Ⅲ中,试剂X是___________ ;
②步骤Ⅱ和Ⅲ中的实验现象说明 和
和 混合时生成
混合时生成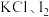 和
和 的反应存在一定的限度,该实验现象是
的反应存在一定的限度,该实验现象是___________ 。
(1)实验一:已知
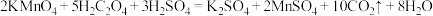 。在酸性高锰酸钾溶液与草酸(
。在酸性高锰酸钾溶液与草酸( )溶液反应时,发现开始一段时间,反应速度较快,溶液褪色不明显,但不久突然褪色,反应速度明显加快。
)溶液反应时,发现开始一段时间,反应速度较快,溶液褪色不明显,但不久突然褪色,反应速度明显加快。①针对上述实验现象,小组同学认为
 与
与 反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你认为还可能是
反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你认为还可能是②若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,还需要的试剂最合理的是
A.硫酸钾 B.硫酸锰 C.二氧化锰 D.水
(2)实验二:探究
 和
和 混合时生成
混合时生成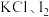 和
和 的反应存在一定的限度。
的反应存在一定的限度。Ⅰ.向
 溶液中滴加
溶液中滴加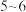 滴
滴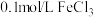 溶液,充分反应后,将所得溶液分成甲、乙两等份;
溶液,充分反应后,将所得溶液分成甲、乙两等份;Ⅱ.向甲中滴加
 ,充分振荡;
,充分振荡;Ⅲ.向乙中滴加试剂X。
请回答下列问题:
①步骤Ⅲ中,试剂X是
②步骤Ⅱ和Ⅲ中的实验现象说明
 和
和 混合时生成
混合时生成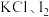 和
和 的反应存在一定的限度,该实验现象是
的反应存在一定的限度,该实验现象是
您最近一年使用:0次
名校
6 . 某研究性学习小组利用H2C2O4溶液和酸性KMnO4溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验如下,回答下列问题:
(1)通过实验A、B,可探究___________ 的改变对反应速率的影响,其中
___________ ,T1=___________ ;通过实验___________ (填序号)可探究出温度变化对化学反应速率的影响。
(2)利用实验B中数据计算,用KMnO4的浓度变化表示的反应速率v(KMnO4)=___________ 。(保留2位有效数字)
(3)写出该反应的离子方程式___________ 。
(4)在实验中发现高锰酸钾酸性溶液和草酸溶液反应时,开始一段时间反应较慢,溶液变色不明显;但不久突然褪色,反应明显加快。某同学认为是反应放热导致溶液温度升高所致,重做B组实验,测定反应过程中不同时间溶液的温度,结果如表:
①结合实验目的与表中数据,你得出的结论是___________ 。
②从影响化学反应速率的因素看,你认为还可能是___________ 的影响。若用实验证明你的猜想,除了酸性高锰酸钾溶液和草酸溶液外,还需要选择的试剂最合理的是___________ (填字母)。
A.硫酸钾 B.水 C.二氧化锰 D.硫酸锰
| 实验序号 | 实验温度/K | 参加反应的物质 | 溶液颜色褪至无色时所需时间/s | ||||
| KMnO4溶液(含硫酸) | H2C2O4溶液 | H2O | |||||
| V/mL | c/mol/L | V/mL | c/mol/L | V/mL | |||
| A | 293 | 20 | 0.2 | 40 | 1 | 0 | t1 |
| B | T1 | 20 | 0.2 | 30 | 1 | V1 | 8 |
| C | 313 | 20 | 0.2 | V2 | 1 | 0 | t2 |

(2)利用实验B中数据计算,用KMnO4的浓度变化表示的反应速率v(KMnO4)=
(3)写出该反应的离子方程式
(4)在实验中发现高锰酸钾酸性溶液和草酸溶液反应时,开始一段时间反应较慢,溶液变色不明显;但不久突然褪色,反应明显加快。某同学认为是反应放热导致溶液温度升高所致,重做B组实验,测定反应过程中不同时间溶液的温度,结果如表:
| 时间/s | 0 | 2 | 4 | 6 | 8 | 10 |
| 温度/℃ | 20 | 21 | 21 | 21.5 | 22 | 22 |
②从影响化学反应速率的因素看,你认为还可能是
A.硫酸钾 B.水 C.二氧化锰 D.硫酸锰
您最近一年使用:0次
2023-10-30更新
|
243次组卷
|
2卷引用:江西省吉安市井冈山市宁冈中学2023-2024学年高二上学期11月期中考试化学试题
名校
解题方法
7 . 实验一:已知 ,甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响。
,甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响。
设计如下(所取溶液体积均为10mL)。
(1)其他条件不变时,探究温度对化学反应速率的影响,应选择实验_____ (填实验编号);若同时选择实验①、实验②、实验③,测定混合液变浑浊的时间,可探究_____ 对化学反应速率的影响。
实验二:已知 ,乙同学通过室温下溶液颜色褪至无色所需时间,研究外界条件对化学反应速率的影响(实验内容及记录如下表)。
,乙同学通过室温下溶液颜色褪至无色所需时间,研究外界条件对化学反应速率的影响(实验内容及记录如下表)。
(2)表中
_____ ,
_____ 。
(3)利用实验1中数据计算,若用KMnO4溶液的浓度变化表示的反应速率为:
_____ 。
(4)在开始一段时间内,反应速率较小,溶液褪色不明显;但不久突然褪色,反应速率明显增大。针对上述现象,某同学认为该反应放热,导致溶液温度上升,反应速率增大。从影响化学反应速率的因素看,你猜想还可能是_____ 的影响。
(5)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,可以在反应一开始时加入_____(填字母)。
 ,甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响。
,甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响。设计如下(所取溶液体积均为10mL)。
| 实验编号 | 实验温度/℃ |  |  |
| ① | 25 | 0.1 | 0.1 |
| ② | 25 | 0.2 | 0.1 |
| ③ | 25 | 0.1 | 0.2 |
| ④ | 50 | 0.2 | 0.1 |
| ⑤ | 50 | 0.1 | 0.1 |
实验二:已知
 ,乙同学通过室温下溶液颜色褪至无色所需时间,研究外界条件对化学反应速率的影响(实验内容及记录如下表)。
,乙同学通过室温下溶液颜色褪至无色所需时间,研究外界条件对化学反应速率的影响(实验内容及记录如下表)。| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | |||
| 0.6mol/LH2C2O4溶液 | H2O | 3mol/L稀硫酸 | 0.05mol/LKMnO4溶液 | ||
| 1 | 3.0 | 2.0 | 2.0 | 3.0 | 1.5 |
| 2 | 2.0 | 3.0 | 2.0 |  | 2.7 |
| 3 | 1.0 |  | 2.0 | 3.0 | 3.9 |


(3)利用实验1中数据计算,若用KMnO4溶液的浓度变化表示的反应速率为:

(4)在开始一段时间内,反应速率较小,溶液褪色不明显;但不久突然褪色,反应速率明显增大。针对上述现象,某同学认为该反应放热,导致溶液温度上升,反应速率增大。从影响化学反应速率的因素看,你猜想还可能是
(5)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,可以在反应一开始时加入_____(填字母)。
| A.硫酸钾 | B.硫酸锰 | C.氯化锰 | D.水 |
您最近一年使用:0次
2023-10-27更新
|
55次组卷
|
3卷引用:广东省东莞市东华高级中学2023-2024学年高二上学期期中联考化学试卷
名校
8 . 下列实验操作、实验现象及实验目的均正确的是
| 选项 | 实验操作 | 实验现象 | 实验目的 |
| A | 向2 mL 0.1 mol·L−1AgNO3溶液中先后加入5滴0.1 mol·L−1NaCl溶液和5滴0.1 mol·L−1 KI溶液 | 先出现白色沉淀,后出现黄色沉淀 | 证明Ksp(AgCl) > Ksp(AgI) |
| B | 向两支装有2 mL 5% H2O2溶液的试管中分别滴入0.1 mol·L−1 FeCl3溶液和0.1 mol·L−1 CuCl2溶液各1 mL(Cl−不影响催化效果) | 滴入FeCl3溶液的试管中产生气泡速率更快 | 证明Fe3+对H2O2分解的催化效果好于Cu2+ |
| C | 向加了酚酞的Na2CO3溶液中加适量蒸馏水 | 溶液红色变深 | Na2CO3溶液的水解平衡正向移动 |
| D | 向铁粉与稀硝酸反应后的溶液中滴入铁氰化钾溶液 | 溶液中出现带有特征蓝色的沉淀 | 溶液中含Fe2+,不含Fe3+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . 用下列仪器或装置进行相应实验,能达到实验目的的是
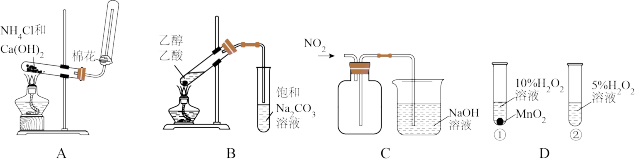

A.实验室制 | B.制备并收集乙酸乙酯 |
C.收集 气体 气体 | D.证明 是 是 分解的催化剂 分解的催化剂 |
您最近一年使用:0次
名校
解题方法
10 .  是一种绿色氧化还原试剂,在化学研究中应用广泛。
是一种绿色氧化还原试剂,在化学研究中应用广泛。
(一)A实验小组拟在同浓度 的催化下,探究
的催化下,探究 浓度对
浓度对 分解反应速率的影响。
分解反应速率的影响。
(1)写出本实验 分解反应方程式并标明电子转移的方向和数目:
分解反应方程式并标明电子转移的方向和数目:___________ 。
(2)设计实验方案:在不同 浓度下,测定
浓度下,测定___________ (要求所测得的数据能直接体现反应速率大小)。
(二)B实验小组在验证 氧化
氧化 时发现异常现象,并进行了深入探究。
时发现异常现象,并进行了深入探究。
实验Ⅰ:
(3)实验Ⅰ中溶液变红的原因是___________ 。(请用离子方程式表示其原理)
(4)探究实验Ⅰ中红色褪去的原因:取反应后溶液,___________ (填实验操作和现象),证明溶液中有 ,而几乎无
,而几乎无 。
。
(5)查阅资料发现,酸性溶液中 能氧化
能氧化 ,但反应很慢且无明显现象,
,但反应很慢且无明显现象, 对该反应没影响。实验Ⅰ中褪色相对较快,由此推测
对该反应没影响。实验Ⅰ中褪色相对较快,由此推测 在酸性溶液中能加快
在酸性溶液中能加快 与
与 的反应。通过实验Ⅱ和Ⅲ得到了证实。参照实验Ⅱ的图例,补全实验Ⅲ加入的试剂和现象。
的反应。通过实验Ⅱ和Ⅲ得到了证实。参照实验Ⅱ的图例,补全实验Ⅲ加入的试剂和现象。
实验Ⅱ:

实验Ⅲ:
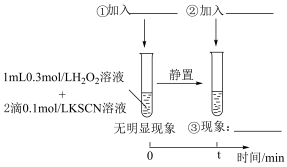
①___________ ;②___________ ;③___________ 。
(三)C实验小组猜测, 会否也能加快
会否也能加快 与
与 的反应。通过实验Ⅱ和Ⅳ得到了证实。
的反应。通过实验Ⅱ和Ⅳ得到了证实。
(6)实验Ⅳ:
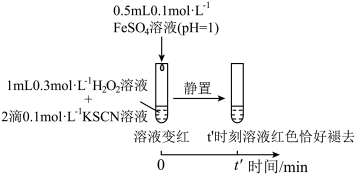
实验得知,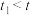 ,对比实验Ⅱ和Ⅳ得到结论:在本实验条件下,
,对比实验Ⅱ和Ⅳ得到结论:在本实验条件下,___________ 。
 是一种绿色氧化还原试剂,在化学研究中应用广泛。
是一种绿色氧化还原试剂,在化学研究中应用广泛。(一)A实验小组拟在同浓度
 的催化下,探究
的催化下,探究 浓度对
浓度对 分解反应速率的影响。
分解反应速率的影响。(1)写出本实验
 分解反应方程式并标明电子转移的方向和数目:
分解反应方程式并标明电子转移的方向和数目:(2)设计实验方案:在不同
 浓度下,测定
浓度下,测定(二)B实验小组在验证
 氧化
氧化 时发现异常现象,并进行了深入探究。
时发现异常现象,并进行了深入探究。实验Ⅰ:
| 装置与操作 | 现象 |
 | 溶液立即变红,继续滴加 溶液,红色变浅并逐渐褪去 溶液,红色变浅并逐渐褪去 |
(4)探究实验Ⅰ中红色褪去的原因:取反应后溶液,
 ,而几乎无
,而几乎无 。
。(5)查阅资料发现,酸性溶液中
 能氧化
能氧化 ,但反应很慢且无明显现象,
,但反应很慢且无明显现象, 对该反应没影响。实验Ⅰ中褪色相对较快,由此推测
对该反应没影响。实验Ⅰ中褪色相对较快,由此推测 在酸性溶液中能加快
在酸性溶液中能加快 与
与 的反应。通过实验Ⅱ和Ⅲ得到了证实。参照实验Ⅱ的图例,补全实验Ⅲ加入的试剂和现象。
的反应。通过实验Ⅱ和Ⅲ得到了证实。参照实验Ⅱ的图例,补全实验Ⅲ加入的试剂和现象。实验Ⅱ:

实验Ⅲ:

①
(三)C实验小组猜测,
 会否也能加快
会否也能加快 与
与 的反应。通过实验Ⅱ和Ⅳ得到了证实。
的反应。通过实验Ⅱ和Ⅳ得到了证实。(6)实验Ⅳ:

实验得知,
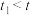 ,对比实验Ⅱ和Ⅳ得到结论:在本实验条件下,
,对比实验Ⅱ和Ⅳ得到结论:在本实验条件下,
您最近一年使用:0次
2023-10-19更新
|
162次组卷
|
2卷引用:广东省广州市执信中学2023-2024学年高二上学期11月期中考试化学试题



