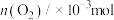解题方法
1 . 甲醇( )作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以
)作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以 为催化剂在水溶液中电催化二氧化碳还原为
为催化剂在水溶液中电催化二氧化碳还原为 和
和 的能量变化如图所示:
的能量变化如图所示:
 )作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以
)作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以 为催化剂在水溶液中电催化二氧化碳还原为
为催化剂在水溶液中电催化二氧化碳还原为 和
和 的能量变化如图所示:
的能量变化如图所示: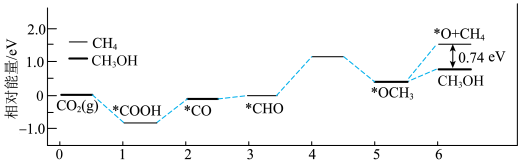
A.生成甲醇反应的决速步为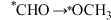 |
| B.两反应只涉及极性键的断裂和生成 |
| C.通过上图分析:甲烷比甲醇稳定 |
D.用 作催化剂可提高甲醇的选择性 作催化剂可提高甲醇的选择性 |
您最近一年使用:0次
2 . 劳动创造美好生活。下列与劳动项目相关的解释正确的是
选项 | 劳动项目 | 解释 |
A | 厨师用酵母菌发酵面粉 | 催化剂可以加快反应速率 |
B | 医护人员利用酒精消毒 | 乙醇具有强氧化性 |
C | 工人向食品包装袋内充 |
|
D | 保洁员用84消毒液清洗公共桌椅 | 84消毒液中的 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 从科技前沿到日常生活,化学无处不在。下列说法不正确的是
| A.今年诺贝尔化学奖授予量子点研究,2nm~20nm硅量子点属于纳米材料 |
| B.中科院研发出水煤气直接转化为烯烃的催化剂,催化剂能改变反应历程 |
C.我国在世界上首次将 合成淀粉,合成中发生了氧化还原反应 合成淀粉,合成中发生了氧化还原反应 |
D.自来水厂用系列水处理剂净化水,明矾与 都属于杀菌消毒剂 都属于杀菌消毒剂 |
您最近一年使用:0次
4 . 一定温度下,在2.0L密闭容器中加入纳米级 并通入
并通入 ,发生反应:
,发生反应: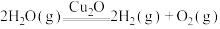
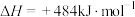 ,不同时间产生
,不同时间产生 的物质的量见下表,下列说法错误的是
的物质的量见下表,下列说法错误的是
 并通入
并通入 ,发生反应:
,发生反应: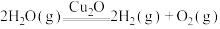
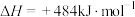 ,不同时间产生
,不同时间产生 的物质的量见下表,下列说法错误的是
的物质的量见下表,下列说法错误的是时间 | 20 | 40 | 60 | 80 |
| 1.0 | 1.6 | 2.0 | 2.0 |
A.使用纳米级 ,可以增大平衡时氧气的体积分数 ,可以增大平衡时氧气的体积分数 |
B.达到平衡时,至少需要从外界吸收能量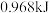 |
C.增大 ,可以改变反应的限度 ,可以改变反应的限度 |
D.前20min的平均反应速率 |
您最近一年使用:0次
名校
5 . 可逆反应aA(g)+bB(s)⇌cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(P)关系如图,其中正确的是
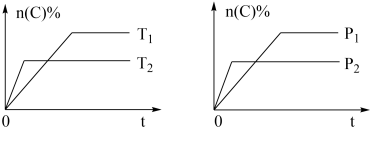

| A.升高温度,平衡向逆反应方向移动 |
| B.使用催化剂,C的物质的量分数增加 |
| C.化学方程式系数a>c+d |
| D.达到平衡后,P1条件V逆反应速率大于P2条件下V正反应速率 |
您最近一年使用:0次
名校
解题方法
6 .  催化还原 NO是重要的烟气脱硝技术,其反应过程与能量关系如图1所示。研究发现,在催化剂上可能发生的反应过程如图2所示。下列说法正确的是
催化还原 NO是重要的烟气脱硝技术,其反应过程与能量关系如图1所示。研究发现,在催化剂上可能发生的反应过程如图2所示。下列说法正确的是
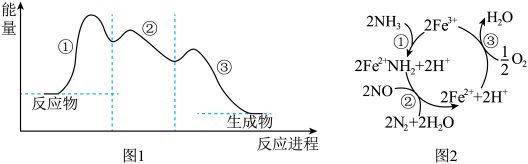
| A.图1三步反应中,第①步反应的活化能最大,为慢反应 |
B.图2中 催化剂 催化剂 |
| C.图2充入过量的O2有利于NO转化为 N2 |
D.图2脱硝的总反应为  |
您最近一年使用:0次
2024-01-22更新
|
69次组卷
|
2卷引用:四川省达州市2023-2024学年高二上学期期末监测化学试题
解题方法
7 . 一定条件下合成乙烯; 。已知温度对CO2的平衡转化率和催化剂催化效率的影响如图。下列说法正确的是
。已知温度对CO2的平衡转化率和催化剂催化效率的影响如图。下列说法正确的是

 。已知温度对CO2的平衡转化率和催化剂催化效率的影响如图。下列说法正确的是
。已知温度对CO2的平衡转化率和催化剂催化效率的影响如图。下列说法正确的是
| A.M点时平衡常数比N点时平衡常数小 |
B.若投料比 ,则图中M点乙烯的体积分数约为5.88% ,则图中M点乙烯的体积分数约为5.88% |
C.若该反应不使用催化剂,则M点的 大于N点的 大于N点的 |
| D.当温度高于250℃,由于升高温度导致催化剂的催化效率而使降低平衡逆向移动 |
您最近一年使用:0次
名校
8 .  与
与 在镍基催化剂催化作用下能发生如图所示的可逆反应,下列说法
在镍基催化剂催化作用下能发生如图所示的可逆反应,下列说法错误 的是

 与
与 在镍基催化剂催化作用下能发生如图所示的可逆反应,下列说法
在镍基催化剂催化作用下能发生如图所示的可逆反应,下列说法
| A.催化剂能降低反应的活化能,增大单位体积内的活化分子百分数 |
B.更换更高效的催化剂,能提高 的平衡转化率 的平衡转化率 |
C.图示反应过程中有 键的断裂与形成 键的断裂与形成 |
D.该过程的总反应为 |
您最近一年使用:0次
名校
9 . 甲酸常被用于橡胶、医药等工业。在一定条件下可分解生成 和
和 。在有、无催化剂条件下的能量与反应历程的关系如图所示。下列说法错误的是
。在有、无催化剂条件下的能量与反应历程的关系如图所示。下列说法错误的是

 和
和 。在有、无催化剂条件下的能量与反应历程的关系如图所示。下列说法错误的是
。在有、无催化剂条件下的能量与反应历程的关系如图所示。下列说法错误的是
| A.途径一与途径二甲酸平衡转化率相同 |
B.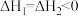 |
C.途径二 参与反应,通过改变反应途径,降低反应的活化能,加快反应速率 参与反应,通过改变反应途径,降低反应的活化能,加快反应速率 |
D.途径二反应的快慢由生成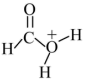 的速率决定 的速率决定 |
您最近一年使用:0次
名校
解题方法
10 . 已知反应S2O (aq)+2I-(aq)
(aq)+2I-(aq) 2SO
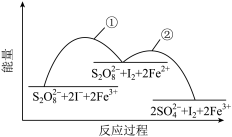
2SO (aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如图所示。下列有关说法正确的是
(aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如图所示。下列有关说法正确的是
 (aq)+2I-(aq)
(aq)+2I-(aq) 2SO
2SO (aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如图所示。下列有关说法正确的是
(aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如图所示。下列有关说法正确的是
| A.反应①②均为放热反应 |
| B.Fe2+是该反应的催化剂 |
| C.增大Fe3+浓度,能够加快反应速率 |
| D.若不加Fe3+,正反应的活化能比逆反应的活化能大 |
您最近一年使用:0次


 有强氧化性
有强氧化性