名校
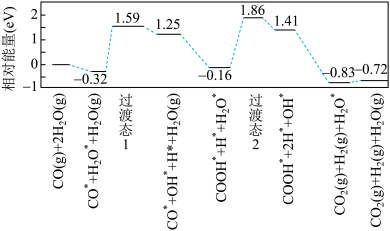
1 . 我国学者研究了在金催化剂表面上水煤气变换的反应,计算机模拟单个CO分子在金催化剂表面的反应历程如图所示(其中吸附在金催化剂表面上的物质用*标注) 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)| A.催化剂能够改变反应历程 |
B.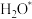 转化为 转化为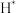 和 和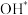 时需要吸收能量 时需要吸收能量 |
| C.反应过程中,过渡态1比过渡态2更难达到 |
D.总反应的热化学方程式为 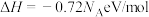 |
您最近一年使用:0次
2024-02-03更新
|
95次组卷
|
2卷引用:辽宁省本溪市第一中学2023-2024学年高二上学期1月期末化学试题
解题方法
2 . 研究 、CO、
、CO、 等大气污染气体的治理,对保护环境有重要的意义.
等大气污染气体的治理,对保护环境有重要的意义.
回答下列问题:
Ⅰ.在一定温度下,向2L的恒容密闭容器中充入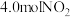 和4.0molCO,在催化剂作用下发生反应:
和4.0molCO,在催化剂作用下发生反应: ,相关数据如下:
,相关数据如下:
(1)已知升高温度,该反应的化学平衡常数K减小,则该反应在________ (填“高温”“低温”或“任何温度”)下能自发进行。
(2)0~5min内CO的化学反应速率v(CO)=________ mol/(L·s)。
(3)以下表述能说明该反应已达到平衡状态的是________ (填标号)。
A. 不再变化 B.混合气体的压强不再变化 C.混合气体的密度不再变化
不再变化 B.混合气体的压强不再变化 C.混合气体的密度不再变化
D. E.混合气体的颜色不再变化 F.化学平衡常数K不再变化
E.混合气体的颜色不再变化 F.化学平衡常数K不再变化
(4)该温度下反应的化学平衡常数K=________ (保留两位有效数字).
(5)在20min时,保持温度不变,向容器中再加入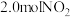 和
和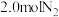 ,则v(正)
,则v(正)________ v(逆)(填“>”“<”或“=”).
Ⅱ.在高效催化剂的作用下用还原 ,也可消除氮氧化物的污染.
,也可消除氮氧化物的污染.
(6) 还原
还原 反应的化学方程式为
反应的化学方程式为________ 。
(7)在相同条件下,选用A、B、C三种不同催化剂进行反应,生成 的物质的量与时间的变化如图1所示,其中活化能最大的是
的物质的量与时间的变化如图1所示,其中活化能最大的是________ [填“Ea(A)”“Ea(B)”或“Ea(C)”,Ea代表活化能]。
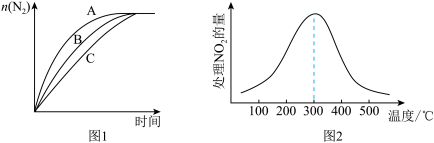
(8)在催化剂A作用下,测得相同时间内处理 的量与温度的关系如图2所示,曲线先增大后减小的原因可能是
的量与温度的关系如图2所示,曲线先增大后减小的原因可能是________ 。
 、CO、
、CO、 等大气污染气体的治理,对保护环境有重要的意义.
等大气污染气体的治理,对保护环境有重要的意义.回答下列问题:
Ⅰ.在一定温度下,向2L的恒容密闭容器中充入
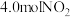 和4.0molCO,在催化剂作用下发生反应:
和4.0molCO,在催化剂作用下发生反应: ,相关数据如下:
,相关数据如下:| 0min | 5min | 10min | 15min | 20min | |
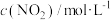 | 2.0 | 1.7 | 1.56 | 1.5 | 1.5 |
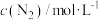 | 0 | 0.15 | 0.22 | 0.25 | 0.25 |
(1)已知升高温度,该反应的化学平衡常数K减小,则该反应在
(2)0~5min内CO的化学反应速率v(CO)=
(3)以下表述能说明该反应已达到平衡状态的是
A.
 不再变化 B.混合气体的压强不再变化 C.混合气体的密度不再变化
不再变化 B.混合气体的压强不再变化 C.混合气体的密度不再变化D.
 E.混合气体的颜色不再变化 F.化学平衡常数K不再变化
E.混合气体的颜色不再变化 F.化学平衡常数K不再变化(4)该温度下反应的化学平衡常数K=
(5)在20min时,保持温度不变,向容器中再加入
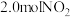 和
和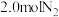 ,则v(正)
,则v(正)Ⅱ.在高效催化剂的作用下用还原
 ,也可消除氮氧化物的污染.
,也可消除氮氧化物的污染.(6)
 还原
还原 反应的化学方程式为
反应的化学方程式为(7)在相同条件下,选用A、B、C三种不同催化剂进行反应,生成
 的物质的量与时间的变化如图1所示,其中活化能最大的是
的物质的量与时间的变化如图1所示,其中活化能最大的是
(8)在催化剂A作用下,测得相同时间内处理
 的量与温度的关系如图2所示,曲线先增大后减小的原因可能是
的量与温度的关系如图2所示,曲线先增大后减小的原因可能是
您最近一年使用:0次
解题方法
3 . 铁的配合物离子(用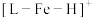 表示)参加某反应的一种反应机理和相对能量的变化情况如图所示:
表示)参加某反应的一种反应机理和相对能量的变化情况如图所示:
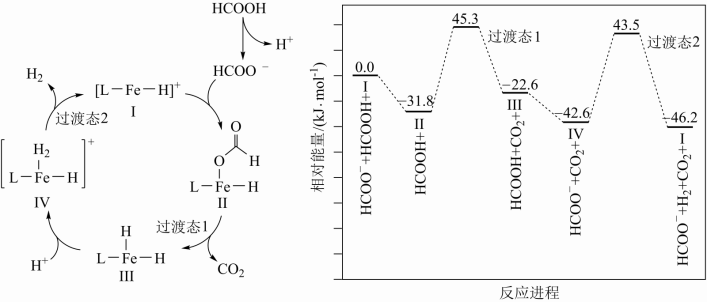
下列说法错误的是
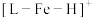 表示)参加某反应的一种反应机理和相对能量的变化情况如图所示:
表示)参加某反应的一种反应机理和相对能量的变化情况如图所示:
下列说法错误的是
A.该过程的总反应为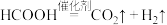 |
B. 浓度越大越有利于该转化过程进行 浓度越大越有利于该转化过程进行 |
| C.该过程的总反应速率由IV→I步骤决定 |
| D.I作为催化剂可以改变反应的活化能,不能改变反应的焓变 |
您最近一年使用:0次
2024-01-13更新
|
191次组卷
|
2卷引用:辽宁省部分学校2023-2024学年高二上学期1月期末化学试题
名校
解题方法
4 . 我国科研人员研究了不同含金催化剂催化乙烯加氢的反应历程如下图所示(已知反应:C2H4(g)+H2(g)=C2H6(g),△H=akJ·mol-1),下列说法错误的是
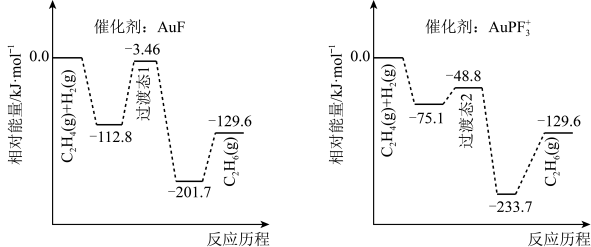

| A.1molC2H4(g)和1molH2(g)的键能之和比lmolC2H6(g)的键能大 |
| B.a=-129.6 |
| C.效果较好的催化剂是AuPF3+大 |
| D.稳定性:过渡态1<过渡态2 |
您最近一年使用:0次
2023-03-19更新
|
472次组卷
|
6卷引用:辽宁省大连市第四十八中学2023-2024学年高二上学期10月月考化学试题
名校
解题方法
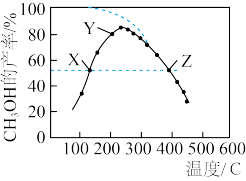
5 . 以CO2和H2为原料,在催化剂作用下合成CH3OH的反应为CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H,反应过程中的副反应为CO2(g)+H2(g)
CH3OH(g)+H2O(g) △H,反应过程中的副反应为CO2(g)+H2(g) CO(g)+H2O(g),反应相同时间,测得不同温度下CH3OH的产率如图中实线所示(图中虚线表示相同条件下CH3OH的平衡产率随温度的变化)。下列说法正确的是
CO(g)+H2O(g),反应相同时间,测得不同温度下CH3OH的产率如图中实线所示(图中虚线表示相同条件下CH3OH的平衡产率随温度的变化)。下列说法正确的是
 CH3OH(g)+H2O(g) △H,反应过程中的副反应为CO2(g)+H2(g)
CH3OH(g)+H2O(g) △H,反应过程中的副反应为CO2(g)+H2(g) CO(g)+H2O(g),反应相同时间,测得不同温度下CH3OH的产率如图中实线所示(图中虚线表示相同条件下CH3OH的平衡产率随温度的变化)。下列说法正确的是
CO(g)+H2O(g),反应相同时间,测得不同温度下CH3OH的产率如图中实线所示(图中虚线表示相同条件下CH3OH的平衡产率随温度的变化)。下列说法正确的是
A.CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H>0 CH3OH(g)+H2O(g) △H>0 |
| B.图中X点所示条件下,延长反应时间能提高CH3OH的产率 |
| C.图中X、Z点的正反应速率与其逆反应速率均相等 |
| D.选用合适的催化剂不可以减弱副反应的发生 |
您最近一年使用:0次
2022-12-06更新
|
224次组卷
|
2卷引用:辽宁省朝阳市建平县2023-2024学年高二上学期1月期末化学试题
名校
6 . N2O是一种温室气体,易形成颗粒性污染物,研究N2O的分解对环境保护有重要意义。在N2O中加入少量碘蒸气反应机理为:
①I2(g)=2I(g)(快反应)
②I(g)+N2O(g)=N2(g)+IO(g)(慢反应)
③2IO(g)+N2O(g)=N2(g)+ O2(g)+I2(g)(快反应)
O2(g)+I2(g)(快反应)
下列叙述错误的是
①I2(g)=2I(g)(快反应)
②I(g)+N2O(g)=N2(g)+IO(g)(慢反应)
③2IO(g)+N2O(g)=N2(g)+
 O2(g)+I2(g)(快反应)
O2(g)+I2(g)(快反应)下列叙述错误的是
| A.升高温度,反应①正向进行程度大 | B.反应②的活化能比反应③大 |
| C.碘蒸气可以提高N2O的分解率 | D.N2O的分解速率由反应②决定 |
您最近一年使用:0次
2022-12-06更新
|
134次组卷
|
3卷引用:辽宁省朝阳市建平县2023-2024学年高二上学期1月期末化学试题
名校
7 . 下图为工业合成氨的流程图。下列说法正确的是
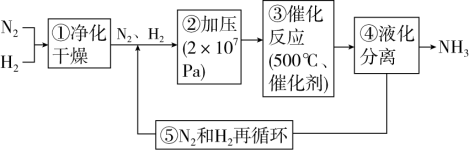

| A.步骤②中“加压”既可以提高原料的转化率,又可以加快反应速率 |
B.步骤③中反应温度提高至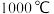 ,反应速率加快且催化剂的活性更高 ,反应速率加快且催化剂的活性更高 |
| C.步骤③、④、⑤均有利于提高原料平衡的转化率 |
| D.步骤⑤采用循环操作,主要是为了提高平衡混合物中氨的含量 |
您最近一年使用:0次
2022-01-27更新
|
233次组卷
|
2卷引用:辽宁省大连市第四十八中学2023-2024学年高二上学期10月月考化学试题



