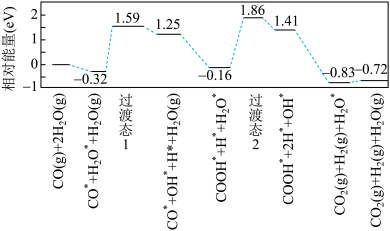
我国学者研究了在金催化剂表面上水煤气变换的反应,计算机模拟单个CO分子在金催化剂表面的反应历程如图所示(其中吸附在金催化剂表面上的物质用*标注) 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)| A.催化剂能够改变反应历程 |
B.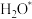 转化为 转化为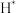 和 和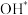 时需要吸收能量 时需要吸收能量 |
| C.反应过程中,过渡态1比过渡态2更难达到 |
D.总反应的热化学方程式为 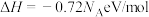 |
更新时间:2024-02-03 10:34:19
|
相似题推荐
【推荐1】下列依据热化学方程式得出的结论正确的是
| 选项 | 热化学方程式 | 结论 |
| A | 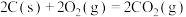    |  |
| B |  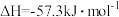 | 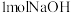 的稀溶液与稀醋酸完全中和,放出热量等于 的稀溶液与稀醋酸完全中和,放出热量等于 |
| C | 500℃、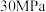 下, 下,   | 将 和过量的 和过量的 在此条件下充分反应,放出热量 在此条件下充分反应,放出热量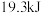 |
| D |   |  的燃烧热 的燃烧热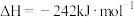 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列热化学方程式或叙述正确的是
A.1 mol 液态肼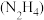 在足量氧气中完全燃烧生成水蒸气,放出642 kJ热量: 在足量氧气中完全燃烧生成水蒸气,放出642 kJ热量: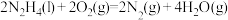  |
B.12g石墨转化为CO时,放出110.5 kJ热量: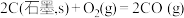 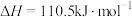 |
C.已知: 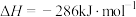 ,则 ,则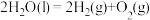 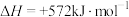 |
D.已知: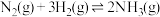 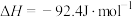 ,则在一定条件下向密闭容器中充入0.5mol ,则在一定条件下向密闭容器中充入0.5mol  和1.5mol 和1.5mol  充分反应放出46.2 kJ的热量 充分反应放出46.2 kJ的热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】2SO2(g)+O2(g) 2SO2(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能),下列有关叙述正确的是
2SO2(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能),下列有关叙述正确的是
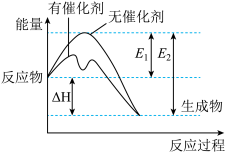
 2SO2(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能),下列有关叙述正确的是
2SO2(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能),下列有关叙述正确的是
| A.E1-E2=△H |
| B.该反应为吸热反应 |
| C.增大氧气的浓度,能使活化分子百分数增大 |
| D.使用催化剂可以提高SO2的转化率 |
您最近一年使用:0次
【推荐2】 是一种强温室气体,且易形成颗粒性污染物,研究
是一种强温室气体,且易形成颗粒性污染物,研究 的分解对环境保护有重要意义。碘蒸气的存在能大幅度提高
的分解对环境保护有重要意义。碘蒸气的存在能大幅度提高 的分解速率,反应历程如下:
的分解速率,反应历程如下:
第一步 (快反应)
(快反应)
第二步 (慢反应)
(慢反应)
第三步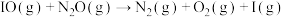 (快反应)
(快反应)
实验表明,含碘时 的分解速率方程
的分解速率方程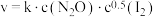 (k为速率常数)。下列表述正确的是
(k为速率常数)。下列表述正确的是
 是一种强温室气体,且易形成颗粒性污染物,研究
是一种强温室气体,且易形成颗粒性污染物,研究 的分解对环境保护有重要意义。碘蒸气的存在能大幅度提高
的分解对环境保护有重要意义。碘蒸气的存在能大幅度提高 的分解速率,反应历程如下:
的分解速率,反应历程如下:第一步
 (快反应)
(快反应)第二步
 (慢反应)
(慢反应)第三步
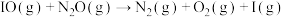 (快反应)
(快反应)实验表明,含碘时
 的分解速率方程
的分解速率方程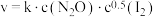 (k为速率常数)。下列表述正确的是
(k为速率常数)。下列表述正确的是| A.IO为反应的中间产物 | B.第一步对总反应速率起决定作用 |
C. 浓度与 浓度与 分解速率无关 分解速率无关 | D.第二步活化能比第三步小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】可逆反应 的v-t图像如图甲所示。若其他条件都不变,只是在反应前加入合适的催化剂,则其v-t图像如图乙所示。下列判断
的v-t图像如图甲所示。若其他条件都不变,只是在反应前加入合适的催化剂,则其v-t图像如图乙所示。下列判断不正确 的是
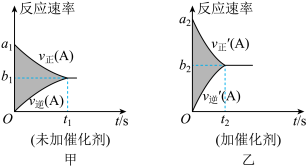
 的v-t图像如图甲所示。若其他条件都不变,只是在反应前加入合适的催化剂,则其v-t图像如图乙所示。下列判断
的v-t图像如图甲所示。若其他条件都不变,只是在反应前加入合适的催化剂,则其v-t图像如图乙所示。下列判断
| A.a1<a2 | B.平衡时图甲和图乙中反应速率相等 |
| C.t1>t2 | D.平衡时图甲和图乙中反应限度相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一步合成甲基丙烯酸甲酯的反应如下(其他产物已省略)。科学家为了研究甲醇的脱氢过程对反应速率的影响,进行了下表所示动力学同位素效应实验(其他条件均相同)。
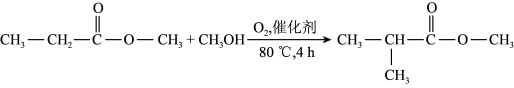
下列说法正确的是

| 实验编号 | 反应物 | 反应速率常数 | 数据分析 | |
| Ⅰ | 丙酸甲酯 | 甲醇( ) ) | 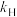 | |
| Ⅱ | 丙酸甲酯 | 氘代甲醇D1(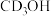 ) ) | 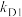 | 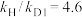 |
| Ⅲ | 丙酸甲酯 | 氘代甲醇D2( ) ) | 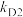 | 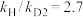 |
A. 、 、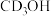 和 和 互为同素异形体 互为同素异形体 |
| B.相比于甲醇,氘代甲醇参与的反应活化能较小 |
| C.相比于C—H键,C—D键断裂的速率较慢 |
| D.相比于O—H键,C—H的断裂对反应速率的影响较小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】根据下列实验事实,不能得到相应结论的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向醋酸溶液中滴加少量Na2SiO3溶液,观察到白色沉淀 | 醋酸的酸性强于H2SiO3 |
| B | 向均盛有2mL5% H2O2溶液的两支试管中分别滴入0.2mol/LFeCl3和0.3mol/LCuCl2溶液各1mL,前者生成气泡的速率更快 | 催化效果: Fe3+> Cu2+ |
| C | 向一定浓度的醋酸溶液中加入镁条,产生气泡的速率会先加快再减慢 | 反应产生气泡速度变化,是因为醋酸电离平衡先正向移动,再逆向移动 |
| D | 常温下分别测等浓度的醋酸和氨水pH,二者的pH 分别为2和12 | 常温下,醋酸和氨水的电离平衡常数相等 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次