名校
解题方法
1 . 已知在2L的密闭容器中进行如下可逆反应,各物质的有关数据如下:
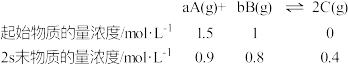
请回答下列问题。
(1)该可逆反应的化学方程式可表示为_______ 。
(2)用物质B来表示0~2s的平均反应速率为_______ 。
(3)从反应开始到2s末,A的转化率为_______ 。
(4)下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是_______ (填序号)。
A.vB(消耗)=vC(生成)
B.容器内气体的总压强保持不变
C.容器内气体的密度不变
D.vA:vB:vC=3:1:2
E.容器内气体C的物质的量分数保持不变
(5)若平衡后改变温度,使得容器中气体的平均摩尔质量变大,则反应向_______ (填“反应物”或“生成物”)的方向移动。
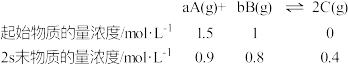
请回答下列问题。
(1)该可逆反应的化学方程式可表示为
(2)用物质B来表示0~2s的平均反应速率为
(3)从反应开始到2s末,A的转化率为
(4)下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是
A.vB(消耗)=vC(生成)
B.容器内气体的总压强保持不变
C.容器内气体的密度不变
D.vA:vB:vC=3:1:2
E.容器内气体C的物质的量分数保持不变
(5)若平衡后改变温度,使得容器中气体的平均摩尔质量变大,则反应向
您最近一年使用:0次
解题方法
2 . 利用太阳能等可再生能源,通过光催化、光电催化或电解水制氢来进行二氧化碳加氢制甲醇,发生的主要反应是:CO2(g)+3H2(g)  CH3OH(g) + H2O(g),若上述反应在恒温、恒容条件下,下列示意图正确且能说明该反应进行到 t1时刻达到平衡状态的是
CH3OH(g) + H2O(g),若上述反应在恒温、恒容条件下,下列示意图正确且能说明该反应进行到 t1时刻达到平衡状态的是
 CH3OH(g) + H2O(g),若上述反应在恒温、恒容条件下,下列示意图正确且能说明该反应进行到 t1时刻达到平衡状态的是
CH3OH(g) + H2O(g),若上述反应在恒温、恒容条件下,下列示意图正确且能说明该反应进行到 t1时刻达到平衡状态的是A. | B.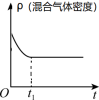 |
C. | D. |
您最近一年使用:0次
名校
3 . 化学与人类生活、生产息息相关。下列说法正确的是
| A.碳酸钠去除油污时,适当加热效果更好 |
B.施肥时,草木灰(有效成分为 )与铵态氨肥混合使用可增强肥效 )与铵态氨肥混合使用可增强肥效 |
| C.泡沫灭火器利用了硫酸铝溶液与碳酸钠溶液的反应 |
| D.高炉炼铁时可通过增加高炉的高度来降低排出气体中CO的百分含量 |
您最近一年使用:0次
名校
解题方法
4 . 直接以 为原料生产
为原料生产 是目前的研究热点,我国科学家用
是目前的研究热点,我国科学家用 人工合成淀粉时,第一步就需要将
人工合成淀粉时,第一步就需要将 转化为
转化为 。回答下列问题:
。回答下列问题:
(1)已知:Ⅰ.

Ⅱ.
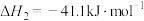 :
:
Ⅲ.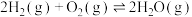
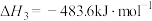 :
:
Ⅳ.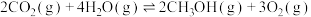
 。
。
①反应①的自发条件是___________ (填“高温自发”“低温自发”或“任何温度下都自发”)。
②反应Ⅳ的 =
=___________ 。
(2)以 、
、 为原料合成
为原料合成 涉及的主要反应如下:
涉及的主要反应如下:
Ⅰ.
Ⅱ. 。
。
①研究表明,在 催化剂存在下,
催化剂存在下, 和
和 只发生反应Ⅰ和Ⅱ,密闭容器保持恒温恒容,下列条件能表明该反应达到平衡状态的是
只发生反应Ⅰ和Ⅱ,密闭容器保持恒温恒容,下列条件能表明该反应达到平衡状态的是___________ (填字母)。
A.当2个 键断裂,同时断裂一个
键断裂,同时断裂一个 键
键
B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.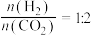
E. 体积分数保持不变
体积分数保持不变
②一定条件下,向体积为VL的恒容密闭容器中通入1mol 和3mol
和3mol  ,发生上述反应,达到平衡时,容器中
,发生上述反应,达到平衡时,容器中 为amol,
为amol, 为bmol,此时
为bmol,此时 的浓度为
的浓度为___________  (用含a、b、V的代数式表示,下同),反应Ⅱ的平衡常数为
(用含a、b、V的代数式表示,下同),反应Ⅱ的平衡常数为___________ 。
(3)甲醇燃料电池以甲醇为燃料,其工作原理如图所示:
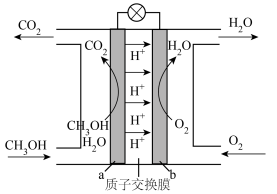
b电极是___________ (填“正极”或“负极”),写出a极的电极反应式:___________ 。
 为原料生产
为原料生产 是目前的研究热点,我国科学家用
是目前的研究热点,我国科学家用 人工合成淀粉时,第一步就需要将
人工合成淀粉时,第一步就需要将 转化为
转化为 。回答下列问题:
。回答下列问题:(1)已知:Ⅰ.


Ⅱ.

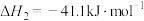 :
:Ⅲ.
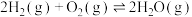
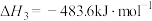 :
:Ⅳ.
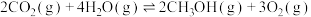
 。
。①反应①的自发条件是
②反应Ⅳ的
 =
=(2)以
 、
、 为原料合成
为原料合成 涉及的主要反应如下:
涉及的主要反应如下:Ⅰ.

Ⅱ.
 。
。①研究表明,在
 催化剂存在下,
催化剂存在下, 和
和 只发生反应Ⅰ和Ⅱ,密闭容器保持恒温恒容,下列条件能表明该反应达到平衡状态的是
只发生反应Ⅰ和Ⅱ,密闭容器保持恒温恒容,下列条件能表明该反应达到平衡状态的是A.当2个
 键断裂,同时断裂一个
键断裂,同时断裂一个 键
键B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.
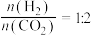
E.
 体积分数保持不变
体积分数保持不变②一定条件下,向体积为VL的恒容密闭容器中通入1mol
 和3mol
和3mol  ,发生上述反应,达到平衡时,容器中
,发生上述反应,达到平衡时,容器中 为amol,
为amol, 为bmol,此时
为bmol,此时 的浓度为
的浓度为 (用含a、b、V的代数式表示,下同),反应Ⅱ的平衡常数为
(用含a、b、V的代数式表示,下同),反应Ⅱ的平衡常数为(3)甲醇燃料电池以甲醇为燃料,其工作原理如图所示:

b电极是
您最近一年使用:0次
2023-12-26更新
|
327次组卷
|
2卷引用:山西省吕梁市孝义市2023-2024学年高二上学期12月月考化学试题
名校
解题方法
5 . 在一定条件下,将 和
和 通入恒容密闭容器中进行反应,容器中发生两个反应
通入恒容密闭容器中进行反应,容器中发生两个反应 和
和 。在不同温度下,测得平衡时体系中
。在不同温度下,测得平衡时体系中 、
、 、
、 的物质的量与温度的关系如图所示。下列说法正确的是
的物质的量与温度的关系如图所示。下列说法正确的是

 和
和 通入恒容密闭容器中进行反应,容器中发生两个反应
通入恒容密闭容器中进行反应,容器中发生两个反应 和
和 。在不同温度下,测得平衡时体系中
。在不同温度下,测得平衡时体系中 、
、 、
、 的物质的量与温度的关系如图所示。下列说法正确的是
的物质的量与温度的关系如图所示。下列说法正确的是
A.曲线 代表 代表 的物质的量与温度的关系 的物质的量与温度的关系 |
B. 的平衡常数: 的平衡常数: 点 点 点 点 |
C. 点时 点时 的反应速率: 的反应速率: |
D. 时,随着温度升高, 时,随着温度升高, 的体积分数不断增大 的体积分数不断增大 |
您最近一年使用:0次
名校
解题方法
6 . 在一定温度的恒容密闭容器中发生: ,下列不能说明反应一定达到平衡状态的是
,下列不能说明反应一定达到平衡状态的是
 ,下列不能说明反应一定达到平衡状态的是
,下列不能说明反应一定达到平衡状态的是A. 的质量保持不变 的质量保持不变 |
B. 、 、 、 、 、 、 的物质的量之比为1:3:1:1 的物质的量之比为1:3:1:1 |
C. |
| D.容器内气体压强不再变化 |
您最近一年使用:0次
2023-11-10更新
|
139次组卷
|
2卷引用:山西省阳泉市第一中学校2023-2024学年高二上学期11月期中考试化学试题
名校
7 . 恒温、恒容密闭容器中发生反应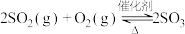 ,能说明该反应已达到平衡状态的是
,能说明该反应已达到平衡状态的是
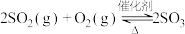 ,能说明该反应已达到平衡状态的是
,能说明该反应已达到平衡状态的是A. | B. |
| C.气体的密度不再随时间而变化 | D.气体总压强不再随时间而变化 |
您最近一年使用:0次
2023-09-06更新
|
123次组卷
|
2卷引用: 山西省孝义中学校2023-2024学年高二上学期开学考试化学试题
名校
8 . 下列有关化学反应速率或限度的说法中正确的是
| A.常温下,Al片分别与浓硝酸和稀硝酸接触2min,与浓硝酸接触收集的气体更多 |
B.铝片与过量的稀硫酸反应,加入 溶液可减缓速率且不影响 溶液可减缓速率且不影响 的产量 的产量 |
C.用双氧水制氧气时,加入少量 粉末可显著加快反应速率 粉末可显著加快反应速率 |
D.工业合成氨时,使用过量的氮气、有可能使 的转化率达到100% 的转化率达到100% |
您最近一年使用:0次
2023-07-16更新
|
283次组卷
|
8卷引用:山西省怀仁市第一中学校、大地学校高中部2023-2024学年高二上学期第一次月考化学试题
山西省怀仁市第一中学校、大地学校高中部2023-2024学年高二上学期第一次月考化学试题河南省开封市五校2022-2023学年高一下学期期末联考化学试题江西省井冈山大学附属中学2022-2023学年高一下学期期中考试化学试题(已下线)第05讲 化学反应的速率与限度-【寒假自学课】2024年高一化学寒假提升学与练(人教版2019)(已下线)热点06化学反应的速率和限度(已下线)6.2.2化学反应的限度课后作业巩固篇(已下线)专题06 化学反应的速率与限度(考点清单)(讲+练)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)(已下线)期中测试卷二【测试范围:第五、六章】-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)
名校
解题方法
9 . 碳单质可用于脱硝。向容积为2L的密闭容器中加入炭(足量)和NO,模拟脱硝反应:C(s)+2NO(g) N2(g)+CO2(g),下列条件能说明反应已经达到平衡状态的是
N2(g)+CO2(g),下列条件能说明反应已经达到平衡状态的是
 N2(g)+CO2(g),下列条件能说明反应已经达到平衡状态的是
N2(g)+CO2(g),下列条件能说明反应已经达到平衡状态的是| A.2v正(NO)=v逆(N2) |
| B.气体的密度不再发生变化 |
| C.容器内气体的压强不再发生变化 |
| D.N2和CO2的物质的量之比不再发生变化 |
您最近一年使用:0次
10 . 甲烷和甲醇(CH3OH)既是重要的化工原料,又是未来重要的能源物质。
(1)通过CO(g)和H2(g)化合可制得甲醇。反应为 ,反应过程中能量变化如图所示。则1molCO(g)和2molH2(g)的总能量
,反应过程中能量变化如图所示。则1molCO(g)和2molH2(g)的总能量_____ (填“>”、“<”或“=”)1molCH3OH(g)的能量。

(2)将2.0molCH4(g)和3.0molH2O(g)通入容积为V的恒容密闭容器中,恒温条件下发生反应: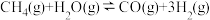 。测得在10min时反应达到平衡,此时CH4的物质的量为1.6mol,CO的物质的量浓度为0.2mol·L-1.则0~10min内,用CO表示该反应的平均反应速率υ(CO)=
。测得在10min时反应达到平衡,此时CH4的物质的量为1.6mol,CO的物质的量浓度为0.2mol·L-1.则0~10min内,用CO表示该反应的平均反应速率υ(CO)=_____ mol·L-1·min-1,V=_____ L;
下列描述中能说明该反应已达平衡状态的是_____ (填标号)。
A.断裂3mol H−H键时,生成2mol H−O键
B.容器内混合气体的平均摩尔质量保持不变
C.容器内混合气体的压强保持不变
D.容器内CO与H2的体积之比保持不变
(3)在容积为1L的恒容密闭容器中投入等物质的量的CO2(g)和H2(g),进行反应: 。CO2(g)、CH3OH(g)的物质的量随时间变化关系如图所示:
。CO2(g)、CH3OH(g)的物质的量随时间变化关系如图所示:

根据图示可知,表示正反应速率与逆反应速率相等的点是_____ (填“a”、“b”、“c”或“d”);用同一物质表示反应速率时,a、c两点的正反应速率:υa_____ υc (填“>”、“<”或“=”,下同),该反应达到平衡时,CO2的转化率_____ 50%。
(4)中国科学院应用化学研究所在甲醇燃料电池(以甲醇燃烧反应为原理)技术方面获得新突破。该反应每消耗1.6g甲醇,外电路中通过导线的电子的数目为_____ 。
(1)通过CO(g)和H2(g)化合可制得甲醇。反应为
 ,反应过程中能量变化如图所示。则1molCO(g)和2molH2(g)的总能量
,反应过程中能量变化如图所示。则1molCO(g)和2molH2(g)的总能量
(2)将2.0molCH4(g)和3.0molH2O(g)通入容积为V的恒容密闭容器中,恒温条件下发生反应:
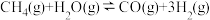 。测得在10min时反应达到平衡,此时CH4的物质的量为1.6mol,CO的物质的量浓度为0.2mol·L-1.则0~10min内,用CO表示该反应的平均反应速率υ(CO)=
。测得在10min时反应达到平衡,此时CH4的物质的量为1.6mol,CO的物质的量浓度为0.2mol·L-1.则0~10min内,用CO表示该反应的平均反应速率υ(CO)=下列描述中能说明该反应已达平衡状态的是
A.断裂3mol H−H键时,生成2mol H−O键
B.容器内混合气体的平均摩尔质量保持不变
C.容器内混合气体的压强保持不变
D.容器内CO与H2的体积之比保持不变
(3)在容积为1L的恒容密闭容器中投入等物质的量的CO2(g)和H2(g),进行反应:
 。CO2(g)、CH3OH(g)的物质的量随时间变化关系如图所示:
。CO2(g)、CH3OH(g)的物质的量随时间变化关系如图所示:
根据图示可知,表示正反应速率与逆反应速率相等的点是
(4)中国科学院应用化学研究所在甲醇燃料电池(以甲醇燃烧反应为原理)技术方面获得新突破。该反应每消耗1.6g甲醇,外电路中通过导线的电子的数目为
您最近一年使用:0次
2023-07-05更新
|
325次组卷
|
4卷引用:山西省忻州市2022-2023学年高一下学期7月期末考试化学试题



