名校
解题方法
1 . “中国芯”的发展离不开单晶硅,工业上制高纯硅,先制得粗硅,再制高纯硅。
Ⅰ.请回答:
(1)工业制粗硅反应的化学方程式为___________ 。
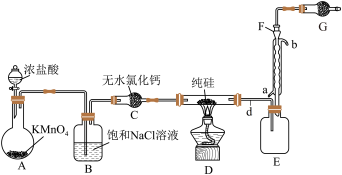
Ⅱ.某小组拟在实验室用如图所示装置模拟探究四氯化硅的制备和应用(夹持装置已省略)。
① ,
, ;
;
② 遇水剧烈水解,
遇水剧烈水解, 的熔点、沸点分别为
的熔点、沸点分别为 、
、 。
。
请回答下列问题:
(2)装无水氯化钙的仪器名称是___________ 。
(3)若拆去B装置,可能的后果是___________ (写出一个即可)。
(4)有同学最初将E、F、G装置设计成图甲所示装置,图甲装置的主要缺点是___________ (写出一个即可)。 在高温条件下易分解生成
在高温条件下易分解生成 和
和 。利用
。利用 和
和 制备新型无机非金属材料(
制备新型无机非金属材料( )的装置如图乙,写出该反应的化学方程式:
)的装置如图乙,写出该反应的化学方程式:___________ 。利用尾气制备盐酸,宜选择下列装置中的___________ (填序号)。
(6) 也是制取高纯硅的重要原料,它在浓的
也是制取高纯硅的重要原料,它在浓的 溶液中的反应方程式为
溶液中的反应方程式为___________ 。
Ⅰ.请回答:
(1)工业制粗硅反应的化学方程式为
Ⅱ.某小组拟在实验室用如图所示装置模拟探究四氯化硅的制备和应用(夹持装置已省略)。
①
 ,
, ;
;②
 遇水剧烈水解,
遇水剧烈水解, 的熔点、沸点分别为
的熔点、沸点分别为 、
、 。
。请回答下列问题:
(2)装无水氯化钙的仪器名称是
(3)若拆去B装置,可能的后果是
(4)有同学最初将E、F、G装置设计成图甲所示装置,图甲装置的主要缺点是
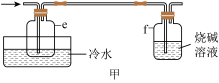
 在高温条件下易分解生成
在高温条件下易分解生成 和
和 。利用
。利用 和
和 制备新型无机非金属材料(
制备新型无机非金属材料( )的装置如图乙,写出该反应的化学方程式:
)的装置如图乙,写出该反应的化学方程式: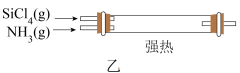

(6)
 也是制取高纯硅的重要原料,它在浓的
也是制取高纯硅的重要原料,它在浓的 溶液中的反应方程式为
溶液中的反应方程式为
您最近一年使用:0次
2024-01-06更新
|
1086次组卷
|
4卷引用:河北省廊坊市2023-2024学年高一下学期3月月考化学试题
河北省廊坊市2023-2024学年高一下学期3月月考化学试题贵州省贵阳市第一中学2023-2024学年高三上学期11月高考适应性月考化学试卷(三)(已下线)题型17 化学实验综合-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)专题09 化学实验综合题-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)
2 . NH3与O2作用分别生成N2、NO、N2O的反应均为放热反应。工业尾气中的NH3可通过催化氧化为N2除去。将一定比例的NH3、O2和N2的混合气体以一定流速通过装有催化剂的反应管,NH3的转化率、生成N2的选择性[
 100%]与温度的关系如图所示。
100%]与温度的关系如图所示。

 100%]与温度的关系如图所示。
100%]与温度的关系如图所示。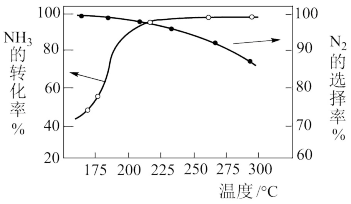
| A.其他条件不变,升高温度,NH3的平衡转化率增大 |
| B.其他条件不变,在175~300 ℃范围,随温度的升高,出口处N2和氮氧化物的量均不断增大 |
| C.催化氧化除去尾气中的NH3应选择反应温度高于250 ℃ |
| D.高效除去尾气中的NH3,需研发低温下NH3转化率高和N2选择性高的催化剂 |
您最近一年使用:0次
2021-11-18更新
|
8382次组卷
|
21卷引用:2024新东方高一上期末考化学01
2024新东方高一上期末考化学01江苏省镇江市2021-2022学年高三上学期期中考试化学试题2021年新高考江苏化学高考真题(已下线)秘籍07 化学反应速率及平衡图象剖析-备战2022年高考化学抢分秘籍(全国通用)(已下线)押江苏卷第14题 反应机理、化学反应速率与平衡 -备战2022年高考化学临考题号押题(江苏卷)湖南省郴州市第一中学2022届高三下学期期中考试化学试题北京市西城区第一六一中学2022届高三考前热身测试化学试题北京市和平街第一中学2021-2022学年高三下学期保温化学试题江苏省平潮高级中学等五校联盟2022届高三高考临门一脚化学试题(已下线)微专题30 非金属及其化合物制备流程与实验探究(S、Se、Te、Cl、Br、I)-备战2023年高考化学一轮复习考点微专题江苏省江阴长泾中学2021-2022学年高二下学期3月份阶段性检测学试题(已下线)专题讲座(七) 常考速率、平衡图像题解题策略(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)微专题38 新情景下的综合图象与突破-备战2023年高考化学一轮复习考点微专题(已下线)易错点11 氮元素及其化合物-备战2023年高考化学考试易错题(已下线)易错点22 化学反应平衡和移动-备战2023年高考化学考试易错题广东省深圳市红岭中学2022-2023学年高二上学期期中考试化学试题湖南省株洲市第四中学2022-2023学年高二上学期期中考试化学试题(已下线)专题15 化学反应速率和化学平衡(已下线)专题15 化学反应速率和化学平衡(已下线)第28讲化化学平衡的移动及反应进行的方向(已下线)题型12 化学平衡图表分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
10-11高一下·山西临汾·期中
名校
解题方法
3 . 下列有关反应2SO2+O2 2SO3的说法中不正确的是
2SO3的说法中不正确的是
 2SO3的说法中不正确的是
2SO3的说法中不正确的是| A.该反应为可逆反应,故在一定条件下二氧化硫与氧气不可能全部转化为三氧化硫 |
| B.达到平衡后,反应就停止了,故此时正、逆反应速率相等且均为零 |
| C.一定条件下,向某密闭容器中加入2molSO2和1molO2,则从反应开始到达到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等 |
| D.在利用上述反应生产三氧化硫时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题 |
您最近一年使用:0次
2021-04-28更新
|
159次组卷
|
11卷引用:2011-2012学年河北省邢台一中高一下学期期末考试化学试卷
(已下线)2011-2012学年河北省邢台一中高一下学期期末考试化学试卷(已下线)2010-2011学年山西省临汾一中高一下学期期中考试化学试卷(已下线)2011-2012学年云南省开远四中高一下学期期中考试化学试卷《课时同步君》2017-2018学年高一化学人教必修2-2.3.2 化学反应的限度黑龙江省哈尔滨市第六中学校2019-2020学年高一下学期返校适应训练化学试题安徽省滁州市定远县育才学校2020-2021学年高一下学期期中考试化学试题河北省张家口市第一中学2021-2022学年高二上学期10月月考化学试题(已下线)6.2.2 化学平衡(第2课时 化学平衡移动)-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)2015-2016学年贵州遵义航天中学高二上第三次月考化学卷(已下线)2018年12月27日 《每日一题》人教选修4-可逆反应天津市两校联考2021-2022学年高二上学期第二次质量检测化学试题
20-21高一下·浙江·阶段练习
名校
4 . 下图所示为工业合成氨的流程图。下列有关生产条件的调控作用分析正确的是
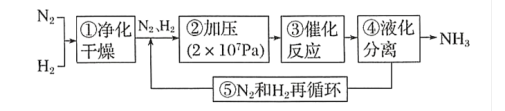

| A.①中“净化”可以防止催化剂中毒,③选择高效催化剂可以使原料完全转化成氨 |
| B.②中“加压”可以加快反应速率,因为在该压强下催化剂的活性最大 |
| C.③一般选择控制反应温度为700℃左右 |
| D.④⑤有利于提高原料的利用率,能节约生产成本 |
您最近一年使用:0次
2021-04-21更新
|
292次组卷
|
3卷引用:河北省辛集中学2020-2021学年高一下学期期中考试化学试题
名校
5 . 某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
(实验原理)2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
(实验内容及记录)
(1)请完成此实验设计,其中:V1=______ ,V2=______ 。
(2)根据上表中实验①、②的数据,可以得到的结论是______ 。
(3)探究温度对化学反应速率的影响,应选择______ (填实验编号)。
(实验原理)2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
(实验内容及记录)
| 实验编号 | 实验温度 | 试管中所加试剂及其用量/mL | 溶液褪至无色所需时间/min | |||
| 0.6mol/LH2C2O4溶液 | H2O | 3mol/L稀H2SO4溶液 | 0.05mol/LKMnO4溶液 | |||
| ① | 25 | 3.0 | V1 | 2.0 | 3.0 | 1.5 |
| ② | 25 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
| ③ | 50 | 2.0 | V2 | 2.0 | 3.0 | 1.0 |
(2)根据上表中实验①、②的数据,可以得到的结论是
(3)探究温度对化学反应速率的影响,应选择
您最近一年使用:0次
2020-12-27更新
|
215次组卷
|
2卷引用:河北省邯郸市大名县第一中学2020-2021学年高一下学期3月月考化学试题
名校
6 . 在不同条件下,用 氧化一定浓度
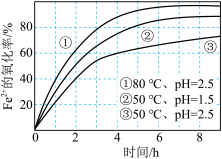
氧化一定浓度 溶液的过程中所测得的实验数据如图所示。下列分析或推测不合理的是( )
溶液的过程中所测得的实验数据如图所示。下列分析或推测不合理的是( )
 氧化一定浓度
氧化一定浓度 溶液的过程中所测得的实验数据如图所示。下列分析或推测不合理的是( )
溶液的过程中所测得的实验数据如图所示。下列分析或推测不合理的是( )
A.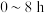 内, 内, 的氧化率随时间延长而逐渐增大 的氧化率随时间延长而逐渐增大 |
B.由曲线②和③可知,pH越大, 的氧化速率越快 的氧化速率越快 |
C.由曲线①和③可知,温度越高, 的氧化速率越快 的氧化速率越快 |
D.氧化过程的离子方程式为 |
您最近一年使用:0次
2020-09-24更新
|
3381次组卷
|
27卷引用:河北省南宫中学2019-2020学年高一下学期6月月考(开学考试)化学试题
河北省南宫中学2019-2020学年高一下学期6月月考(开学考试)化学试题河北省承德市隆化存瑞中学2019-2020学年高一下学期期末测试化学试题北京市朝阳区2018-2019学年高一第二学期期末质量检测化学试题江苏省南通市海安高级中学2019-2020学年高一下学期5月月考化学试题荆、荆、襄、宜四地七校考试联盟2019-2020学年高一下学期期中联考化学试题北京市海淀区北京理工大学附中2019-2020学年高一下学期期末练习化学试题北京市延庆区2019-2020学年高一下学期期末考试化学试题北京市大兴区2019-2020学年高一下学期期末考试化学试题北京市海淀区19中2019-2020学年高一下学期期末考试化学试题鲁科版(2019)高一必修第二册 第2章 化学键 反应规律 第三节 化学反应的快慢和限度 作业帮高中化学苏教2019版必修第二册-专题6 第一单元 第1课时 化学反应速率人教版2019必修第二册 全书综合测评江西省南昌市八一中学2021-2022学年高一下学期复学摸底考试化学试题北京市东直门中学2021—2022学年高一下学期6月月考化学试题广东省江门市广东实验中学江门分校2022-2023学年高一下学期第二次月考化学试题(已下线)第06练化学反应的速率与限度-2020年【衔接教材·暑假作业】新高二化学(人教版)(已下线)易错11 影响化学反应速率的因素-备战2021年高考化学一轮复习易错题(已下线)第二章 化学反应速率和化学平衡(能力提升)-2020-2021学年高二化学单元测试定心卷(人教版选修4)内蒙古通辽市开鲁县第一中学2021届高三上学期第二次阶段性考试化学试题北京市海淀人大附中西山学校2020-2021学年高二上学期期中考试化学试题(已下线)小题必刷27 化学反应速率、图像及其影响因素——2021年高考化学一轮复习小题必刷(通用版本)山东省淄博市高青县第一中学2021-2022学年高二上学期期中考试化学试题安徽省舒城中学2022-2023学年高二上学期第二次月考化学试题吉林省长春市新解放学校2022-2023学年高二上学期11月月考化学试题重庆市璧山来凤中学2023-2024学年高二上学期9月月考化学试题四川省成都市第八中学校2022-2023学年高二上学期11月期中考试化学试题云南省保山市腾冲市2022-2023学年高二上学期期中教育教学质量监测化学试卷
名校
解题方法
7 . 常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g) Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×10−5。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。下列判断正确的是( )
Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×10−5。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。下列判断正确的是( )
 Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×10−5。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。下列判断正确的是( )
Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×10−5。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。下列判断正确的是( )| A.230℃时增加镍的量,平衡向正向移动,反应的平衡常数不变 |
| B.第一阶段,在30℃和50℃两者之间选择反应温度,选30℃ |
| C.第二阶段,Ni(CO)4分解率较高 |
| D.该反应达到平衡时,4υ消耗[Ni(CO)4]=υ生成(CO) |
您最近一年使用:0次
名校
解题方法
8 . 反应Ⅰ、Ⅱ、Ⅲ均会在工业生产硝酸过程中发生,其中反应Ⅰ、Ⅱ发生在氧化炉中,反应Ⅲ发生在氧化塔中,不同温度下各反应的化学平衡常数如下表所示。下列说法正确的是
温度 (K) | 化学平衡常数 | ||
反应Ⅰ: 4NH3 + 5O2 → 4NO + 6H2O | 反应Ⅱ: 4NH3 + 3O2 → 2N2 + 6H2O | 反应Ⅲ: 2NO + O2 → 2NO2 | |
500 | 1.1×1026 | 7.1×1034 | 1.3×102 |
700 | 2.1×1019 | 2.6×1025 | 1.0 |
| A.使用选择性催化反应Ⅰ的催化剂可增大氧化炉中NO的含量 |
| B.通过改变氧化炉的温度可促进反应Ⅰ而抑制反应Ⅱ |
| C.通过改变氧化炉的压强可促进反应Ⅰ而抑制反应Ⅱ |
| D.氧化炉出气在进入氧化塔前应进一步提高温度 |
您最近一年使用:0次
2020-05-13更新
|
495次组卷
|
6卷引用:河北省石家庄市第二中学本部2019-2020学年高一下学期期末结业考试化学试题
河北省石家庄市第二中学本部2019-2020学年高一下学期期末结业考试化学试题山东省2020届夏季普通高中学业水平等级考试模拟考试化学试题浙江省杭州市学军中学2020届高三下学期最后一次模拟考化学试题山东省枣庄市2021届高三上学期第三次质量检测化学试题陕西省西安市第一中学2020-2021学年高二上学期期中考试化学试题(已下线)2.4.1 合成氨生产适宜条件的选择-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)
名校
9 . 某温度下,将2mol A和3mol B充入一密闭容器中,发生反应:aA(g)+ B(g) C(g)+ D(g),5min后达到平衡。已知该温度下其平衡常数为1,在t0时刻,若保持温度不变将容器体积扩大为原来的10倍,A的转化率不发生变化,则下列说法正确的是
C(g)+ D(g),5min后达到平衡。已知该温度下其平衡常数为1,在t0时刻,若保持温度不变将容器体积扩大为原来的10倍,A的转化率不发生变化,则下列说法正确的是
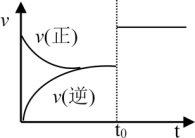
 C(g)+ D(g),5min后达到平衡。已知该温度下其平衡常数为1,在t0时刻,若保持温度不变将容器体积扩大为原来的10倍,A的转化率不发生变化,则下列说法正确的是
C(g)+ D(g),5min后达到平衡。已知该温度下其平衡常数为1,在t0时刻,若保持温度不变将容器体积扩大为原来的10倍,A的转化率不发生变化,则下列说法正确的是
| A.a=2 |
| B.达到平衡时A的转化率为60% |
| C.速率随时间变化关系如图所示 |
| D.为提高A的转化率,可采取升高温度的措施 |
您最近一年使用:0次
2018-12-24更新
|
279次组卷
|
7卷引用:河北省石家庄市第二中学2019-2020学年高一下学期期末考试化学试题
名校
10 . 为了研究外界条件对H2O2分解速率的影响,有同学利用实验室提供的仪器和试剂设计了如下实验。注意:设计实验时,必须控制只有一个变量!
试剂:4% H2O2溶液,12% H2O2溶液,lmol/LFeCl3溶液
仪器:试管、带刻度的胶头滴管、酒精灯
(1)实验l:实验目的:温度对化学反应速率的影响
实验步骤:分别向甲、乙两支试管中加入5mL4% H202溶液,再分别加入3滴1mol/LFeCl3溶液,待两支试管中均有适量气泡出现时,将试管甲放入5℃水浴中,将试管乙放入40℃水浴中。实验现象:试管___________ 。(填甲或乙)中产生气泡的速率快,说明____________ 。
(2)实验2:实验目的:浓度对化学反应速率的影响
实验步骤:向试管甲中加入5mL4% H2O2溶液,向试管乙中加入5mL12%H2O2溶液。
实验现象:试管甲、乙中均有少量气体缓慢产生。
该实验现象不明显,你如何改进实验方案,使实验现象支持“浓度改变会影响化学反应速率”
这一理论预测____________ 。
(3)实验3:实验目的:________ 。
实验步骤:在试管甲中加入5mL4% H2O2溶液,在试管乙中加入5mL4% H2O2溶液再加入lmL lmoFLFeC13溶液。
你认为方案3的设计是否严谨?_______ (填是或否),说明理由_______ 。
试剂:4% H2O2溶液,12% H2O2溶液,lmol/LFeCl3溶液
仪器:试管、带刻度的胶头滴管、酒精灯
(1)实验l:实验目的:温度对化学反应速率的影响
实验步骤:分别向甲、乙两支试管中加入5mL4% H202溶液,再分别加入3滴1mol/LFeCl3溶液,待两支试管中均有适量气泡出现时,将试管甲放入5℃水浴中,将试管乙放入40℃水浴中。实验现象:试管
(2)实验2:实验目的:浓度对化学反应速率的影响
实验步骤:向试管甲中加入5mL4% H2O2溶液,向试管乙中加入5mL12%H2O2溶液。
实验现象:试管甲、乙中均有少量气体缓慢产生。
该实验现象不明显,你如何改进实验方案,使实验现象支持“浓度改变会影响化学反应速率”
这一理论预测
(3)实验3:实验目的:
实验步骤:在试管甲中加入5mL4% H2O2溶液,在试管乙中加入5mL4% H2O2溶液再加入lmL lmoFLFeC13溶液。
你认为方案3的设计是否严谨?
您最近一年使用:0次
2017-04-03更新
|
526次组卷
|
6卷引用:河北省张家口市宣化区宣化第一中学2019-2020学年高一下学期期中考试化学试题



