名校
解题方法
1 . 下列有关反应2SO2+O2 2SO3的说法中不正确的是
2SO3的说法中不正确的是
 2SO3的说法中不正确的是
2SO3的说法中不正确的是| A.该反应为可逆反应,故在一定条件下二氧化硫与氧气不可能全部转化为三氧化硫 |
| B.达到平衡后,反应就停止了,故此时正、逆反应速率相等且均为零 |
| C.一定条件下,向某密闭容器中加入2molSO2和1molO2,则从反应开始到达到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等 |
| D.在利用上述反应生产三氧化硫时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题 |
您最近一年使用:0次
2021-04-28更新
|
158次组卷
|
11卷引用:安徽省滁州市定远县育才学校2020-2021学年高一下学期期中考试化学试题
安徽省滁州市定远县育才学校2020-2021学年高一下学期期中考试化学试题(已下线)2010-2011学年山西省临汾一中高一下学期期中考试化学试卷(已下线)2011-2012学年云南省开远四中高一下学期期中考试化学试卷(已下线)2011-2012学年河北省邢台一中高一下学期期末考试化学试卷《课时同步君》2017-2018学年高一化学人教必修2-2.3.2 化学反应的限度黑龙江省哈尔滨市第六中学校2019-2020学年高一下学期返校适应训练化学试题(已下线)6.2.2 化学平衡(第2课时 化学平衡移动)-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)2015-2016学年贵州遵义航天中学高二上第三次月考化学卷(已下线)2018年12月27日 《每日一题》人教选修4-可逆反应天津市两校联考2021-2022学年高二上学期第二次质量检测化学试题河北省张家口市第一中学2021-2022学年高二上学期10月月考化学试题
2 . 关于水煤气变换反应CO(g)+H2O(g)⇌CO2(g)+H2(g)ΔH(简称WGS反应),目前普遍接受的表面氧化还原机理的可能基元反应(一步完成的反应)步骤如下:
①H2O+*⇌H2O*②H2O*+*⇌OH*+H*③OH*+*⇌O*+H*④2H*+*⇌H2+2*⑤CO+*⇌CO*⑥CO*+O*⇌CO2*+*⑦CO2*⇌CO2+*
其中*表示催化剂表面活性位,X*表示金属表面吸附物种。
WGS反应中可能基元反应步骤的活化能数值(单位:kJ·mol−1)如下表:
注:表中X(111)表示不同金属的同一晶面,110与111表示不同晶面。
下列说法正确的是
①H2O+*⇌H2O*②H2O*+*⇌OH*+H*③OH*+*⇌O*+H*④2H*+*⇌H2+2*⑤CO+*⇌CO*⑥CO*+O*⇌CO2*+*⑦CO2*⇌CO2+*
其中*表示催化剂表面活性位,X*表示金属表面吸附物种。
WGS反应中可能基元反应步骤的活化能数值(单位:kJ·mol−1)如下表:
| 基元反应 | 正反应(Ef) | 逆反应(Et) | ||||
| Cu(110) | Cu(111) | Pd(111) | Cu(110) | Cu(111) | Pd(111) | |
| ① | 0 | 0 | 0 | 58 | 58 | 42 |
| ② | 96 | 109 | 108 | 24 | 8 | 0 |
| ③ | 58 | 67 | 63 | 96 | 88 | 92 |
| ④ | 80 | 63 | 92 | 21 | 29 | 8 |
| ⑤ | 0 | 0 | 0 | 50 | 50 | 142 |
| ⑥ | 45 | 46 | 100 | 95 | 117 | 140 |
| ⑦ | 21 | 21 | 17 | 0 | 0 | 0 |
下列说法正确的是
| A.由表中数据可以得出催化剂通过改变反应的焓变影响反应速率 |
| B.由表中数据可计算Cu(111)催化WGS反应的焓变ΔH=+44kJ·mol−1 |
| C.由表格数据可以看出Cu(111)的催化效果优于Cu(110) |
| D.该机理中WGS反应的速率控制步骤是② |
您最近一年使用:0次
3 . 某工厂利用黄铁矿(主要成分为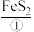 )制取硫酸的工艺流程如下:
)制取硫酸的工艺流程如下:
第一步:将黄铁矿粉碎后在沸腾炉中高温处理造气,可获得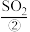 和炉渣(主要成分为
和炉渣(主要成分为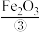 )。
)。
第二步:将获得的气体净化后与空气按一定比例通入催化反应室中,在催化剂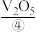 的作用下转化为
的作用下转化为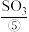 。
。
第三步:用吸收塔吸收后,再加适量水稀释至质量分数为98%的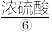 (密度约为1.84g·cm-3)。
(密度约为1.84g·cm-3)。
工业生产中产生的尾气用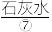 吸收,使其转化为
吸收,使其转化为 后,再用
后,再用 处理,生成SO2和
处理,生成SO2和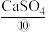 ,这样得到的SO2含量较高,可循环用作原料。
,这样得到的SO2含量较高,可循环用作原料。
根据上述短文,回答下列问题:
(1)上述10种物质中属于氧化物的是___________ (填序号,下同)。
(2)常温下,⑦⑧⑨⑩四种物质中能导电的是___________ 。
(3)写出③与⑨反应的离子方程式:___________ 。
(4)第三步中对应⑥的物质的量浓度为___________ mol·L-1。
(5)标准状况下,1.12L②完全转化为⑤时,反应中转移的电子的物质的量为___________ mol。
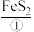 )制取硫酸的工艺流程如下:
)制取硫酸的工艺流程如下:第一步:将黄铁矿粉碎后在沸腾炉中高温处理造气,可获得
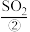 和炉渣(主要成分为
和炉渣(主要成分为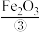 )。
)。第二步:将获得的气体净化后与空气按一定比例通入催化反应室中,在催化剂
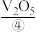 的作用下转化为
的作用下转化为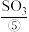 。
。第三步:用吸收塔吸收后,再加适量水稀释至质量分数为98%的
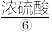 (密度约为1.84g·cm-3)。
(密度约为1.84g·cm-3)。工业生产中产生的尾气用
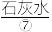 吸收,使其转化为
吸收,使其转化为 后,再用
后,再用 处理,生成SO2和
处理,生成SO2和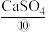 ,这样得到的SO2含量较高,可循环用作原料。
,这样得到的SO2含量较高,可循环用作原料。根据上述短文,回答下列问题:
(1)上述10种物质中属于氧化物的是
(2)常温下,⑦⑧⑨⑩四种物质中能导电的是
(3)写出③与⑨反应的离子方程式:
(4)第三步中对应⑥的物质的量浓度为
(5)标准状况下,1.12L②完全转化为⑤时,反应中转移的电子的物质的量为
您最近一年使用:0次
名校
解题方法
4 . 干燥剂的干燥性能可用干燥效率(1m3 空气中实际余留水蒸气的质量)来衡量,某些干燥剂的干燥效率数据如表所示,根据表中数据做出的推测不合理的是( )
| 物质 | CaCl2 | CaBr2 | CaO | CaSO4 | MgO | Al2O3 | ZnCl2 | ZnBr2 | CuSO4 |
| 干燥效率 | 0.14 | 0.14 | 0.2 | 0.04 | 0.008 | 0.003 | 0.8 | 1.1 | 1.4 |
| A.干燥剂中非金属元素对干燥效率无影响 |
| B.MgO 的干燥性能比 CaO 好 |
| C.MgSO4 的干燥效率可能小于 0.04 |
| D.干燥剂中金属元素对于干燥效率影响可能比较大 |
您最近一年使用:0次
2020-10-25更新
|
138次组卷
|
4卷引用:安徽省舒城中学2020-2021学年高一上学期开学考试化学试题
名校
5 . 用尿素[(NH2)2CO]水溶液吸收氮氧化物也是一种可行的方法。NO 和 NO2不同配比混合气通入尿素溶液中,总氮还原率与配比关系如下图。

(1)用尿素[(NH2)2CO]水溶液吸收体积比为 1∶1 的 NO 和 NO2混合气,可将 N 元素转变为对环境无害的气体。写出该反应的化学方程式___________________ 。
(2)随着 NO 和 NO2配比的提高,总氮还原率降低的主要原因是__________________ 。

(1)用尿素[(NH2)2CO]水溶液吸收体积比为 1∶1 的 NO 和 NO2混合气,可将 N 元素转变为对环境无害的气体。写出该反应的化学方程式
(2)随着 NO 和 NO2配比的提高,总氮还原率降低的主要原因是
您最近一年使用:0次
名校
6 . 工业合成氨缓解了有限耕地与不断增长的人口对粮食大量需求之间的矛盾。
(1)N2分子通常条件下非常稳定,其本质原因是_____ ,工业上选择500℃主要出于两方面考虑,一是反应速率快;二是_____ 。
(2)将1mol气态分子断裂成气态原子所吸收的能量叫键能。相关键能数据如下表:
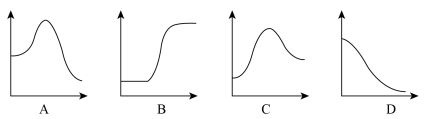
结合表中所给信息,下图中能正确表示合成氨反应过程中能量变化关系的是_____ 。
(3)一定条件下,氨与水的反应存在限度,氨水成弱碱性,用一个化学用语,表示氨与水反应及溶液显碱性的原因_____ 。
(4)硫酸铵是一种固态氮肥,俗称“肥田粉”。硫酸铵可由氨与硫酸反应生成,硫酸铵中含有的化学键类型有_____ 。
(5)氨氧化法可以用来生产硝酸,写出第一步和第三步的化学反应方程式_________________ 、_________________ 。
(1)N2分子通常条件下非常稳定,其本质原因是
(2)将1mol气态分子断裂成气态原子所吸收的能量叫键能。相关键能数据如下表:
| 共价键 | H-H | N≡N | N-H |
| 键能(kJ/mol) | 436 | 946 | 391 |
结合表中所给信息,下图中能正确表示合成氨反应过程中能量变化关系的是

(3)一定条件下,氨与水的反应存在限度,氨水成弱碱性,用一个化学用语,表示氨与水反应及溶液显碱性的原因
(4)硫酸铵是一种固态氮肥,俗称“肥田粉”。硫酸铵可由氨与硫酸反应生成,硫酸铵中含有的化学键类型有
(5)氨氧化法可以用来生产硝酸,写出第一步和第三步的化学反应方程式
您最近一年使用:0次
名校
解题方法
7 . 含碘化合物在有关反应原理的实验中有着广泛应用。为研究温度对反应速率的影响,某小组利用还原性物质R与KIO3溶液在不同温度下反应,当R消耗完时,体系中即有单质碘析出,通过测量析出单质碘所需要的时间可以研究温度对该反应反应速率的影响。具体实验与相关结论如下:将0.020 mol·L-1的R溶液(含少量淀粉)10.0 mL与0.020mol·L-1的KIO3酸性溶液40.00 mL(过量)混合,每隔5℃进行实验,记录10~60℃间溶液变蓝时间,实验所得数据如表所示。
下列判断不正确的是
| 温度/℃ | 10 | 15 | 20 | 25 | 30 | 35 | 40 | 45 | 50 | 55 | 60 |
| 溶液变蓝时间/s | 80 | 74 | 69 | 63 | 61 | 58 | 56 | 63 | 68 | 未变色 | 未变色 |
下列判断不正确的是
| A.40℃之后通过测量溶液变蓝的时间无法正确判断温度对反应速率的影响 |
| B.温度为25℃、45 ℃时,R的反应速率相等 |
| C.10℃时R的反应速率为5.0×10-5mol·L-1·s-1 |
| D.如果要得到温度变化对该反应反应速率影响的完整结论,需要在40℃之后更换指示剂 |
您最近一年使用:0次
2020-04-16更新
|
74次组卷
|
4卷引用:安徽省黄山市2023-2024学年屯溪一中高一上学期10月化学月考
安徽省黄山市2023-2024学年屯溪一中高一上学期10月化学月考(已下线)【南昌新东方】2019 南昌一中 高一下第二次月考内蒙古通辽市开鲁县第一中学2020-2021学年高二上学期第一次月考化学试题(已下线)【浙江新东方】59
8 . 天然气是一种重要的化工原料和燃料,常含有少量H2S。一种在酸性介质中进行天然气脱硫的原理示意图如图所示。下列说法正确的是


| A.脱硫过程中Fe2(SO4)3溶液的pH逐渐减小 |
| B.CH4是天然气脱硫过程的催化剂 |
| C.脱硫过程需不断补充FeSO4 |
| D.整个脱硫过程中参加反应的n(H2S):n(O2)=2:1 |
您最近一年使用:0次
2020-04-01更新
|
947次组卷
|
6卷引用:安徽省淮北市实验高级中学2022-2023学年高一上学期阶段性考试化学试题
9 . 在好氧菌和厌氧菌作用下,废液中 能转化为
能转化为 和
和 ,示意图如下:
,示意图如下:
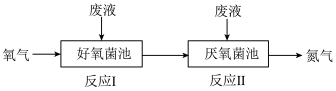
反应Ⅰ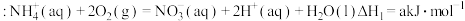
反应Ⅱ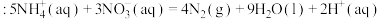

下列说法正确的是( )
 能转化为
能转化为 和
和 ,示意图如下:
,示意图如下: 
反应Ⅰ
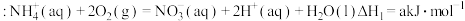
反应Ⅱ
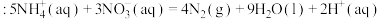

下列说法正确的是( )
| A.两池发生的反应中,氮元素只被氧化 |
B.两池中投放的废液体积相等时, 能完全转化为 能完全转化为 |
C.常温常压下,反应Ⅱ中生成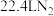 转移的电子数为 转移的电子数为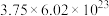 |
D.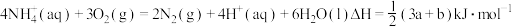 |
您最近一年使用:0次
2020-01-25更新
|
389次组卷
|
11卷引用:安徽省安庆市怀宁县怀宁中学2019-2020学年高一下学期期中考试化学试题
安徽省安庆市怀宁县怀宁中学2019-2020学年高一下学期期中考试化学试题安徽省淮南市第一中学2019-2020学年高一下学期期末考试化学试题江苏省南通、徐州、扬州、泰州、淮安、宿迁六市2018届高三第二次调研(二模)化学试题2020届高三化学二轮冲刺新题专练——盖斯定律的应用2(已下线)【新东方】 2020-11沪科版化学拓展性课程4《离子互换反应和氧化还原反应》测试题江苏省启东中学2020-2021学年高二上学期第一次月考化学试题福建省福州市格致中学2022-2023学年高三上学期期中模拟测试化学试题重庆市松树桥中学校2023-2024学年高二上学期半期考试(期中)化学试题新疆乌鲁木齐市高级中学2023-2024学年高三上学期12月月考化学试题新疆乌鲁木齐市高级中学2024届高三上学期12月月考化学
名校
解题方法
10 . 汽车尾气和燃煤尾气是造成空气污染的重要原因之一,治理汽车尾气和燃煤尾气是环境保护的重要课题。回答下列问题:
(1)煤燃烧产生的烟气中含有氮的氧化物,用CH4催化还原NO2可消除氮氧化物的污染。已知:①CH4(g)+ 2NO2(g)= N2(g)+CO2(g)+2H2O(g) △H=-867.0kJ/mol;②N2(g)+2O2(g)= 2NO2(g) △H=+67.8 kJ/mol;③N2(g)+O2(g)=2NO(g) △H=+89.0 kJ/mol则CH4催化还原NO的热化学方程式为___________________ 。
(2)在汽车排气系统中安装三元催化转化器,可发生反应:2NO(g)+2CO(g)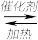 2CO2(g)+N2(g)。在某密闭刚性容器中通入等量的CO和NO,发生上述反应时,c(CO)随温度(T)和时间(t)的变化曲线如图所示。
2CO2(g)+N2(g)。在某密闭刚性容器中通入等量的CO和NO,发生上述反应时,c(CO)随温度(T)和时间(t)的变化曲线如图所示。
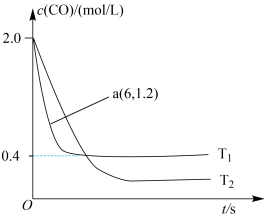
①据此判断该反应的正反应为__________ (填“放热”或“吸热”)反应。
②温度T1时,该反应的平衡常数K=___________ ;反应速率v=v正-v逆=k正c2(NO)c2(CO)-k逆c2(CO2)c(N2),k正、k逆分别为正、逆反应速率常数,计算a处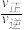 =
=______________ 。
(3)SNCR-SCR脱硝技术是一种新型的除去烟气中氮氧化物的脱硝技术,一般采用氨气或尿素作还原剂,其基本流程如图:

①SNCR-SCR脱硝技术中用NH3作还原剂还原NO的主要反应为4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g),△H<0,则用尿素[CO(NH2)2]作还原剂还原NO2的化学方程式为_________________ 。
②体系温度直接影响SNCR技术的脱硝效率,如图所示:
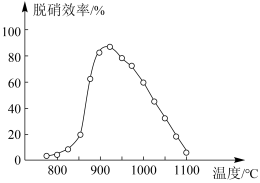
SNCR与SCR技术相比,SCR技术的反应温度不能太高,其原因是_________________ ;当体系温度约为925℃时,SNCR脱硝效率最高,其可能的原因是_____________________ 。
(1)煤燃烧产生的烟气中含有氮的氧化物,用CH4催化还原NO2可消除氮氧化物的污染。已知:①CH4(g)+ 2NO2(g)= N2(g)+CO2(g)+2H2O(g) △H=-867.0kJ/mol;②N2(g)+2O2(g)= 2NO2(g) △H=+67.8 kJ/mol;③N2(g)+O2(g)=2NO(g) △H=+89.0 kJ/mol则CH4催化还原NO的热化学方程式为
(2)在汽车排气系统中安装三元催化转化器,可发生反应:2NO(g)+2CO(g)
 2CO2(g)+N2(g)。在某密闭刚性容器中通入等量的CO和NO,发生上述反应时,c(CO)随温度(T)和时间(t)的变化曲线如图所示。
2CO2(g)+N2(g)。在某密闭刚性容器中通入等量的CO和NO,发生上述反应时,c(CO)随温度(T)和时间(t)的变化曲线如图所示。
①据此判断该反应的正反应为
②温度T1时,该反应的平衡常数K=
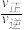 =
=(3)SNCR-SCR脱硝技术是一种新型的除去烟气中氮氧化物的脱硝技术,一般采用氨气或尿素作还原剂,其基本流程如图:

①SNCR-SCR脱硝技术中用NH3作还原剂还原NO的主要反应为4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g),△H<0,则用尿素[CO(NH2)2]作还原剂还原NO2的化学方程式为
②体系温度直接影响SNCR技术的脱硝效率,如图所示:

SNCR与SCR技术相比,SCR技术的反应温度不能太高,其原因是
您最近一年使用:0次
2019-03-16更新
|
761次组卷
|
3卷引用:安徽省阜阳市第三中学2018-2019学年高一下学期第二次调研考试化学试题



