解题方法
1 . 丙烯是一种重要的化工原料,工业上丙烷制丙烯的相关反应如下:
ⅰ.
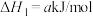
ⅱ.

ⅲ.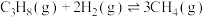
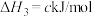
回答下列问题:
Ⅰ.单独投料(副反应抑制法)。
(1)反应: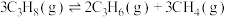

_________  。
。
(2) 时,单独加入
时,单独加入 至
至 后达到平衡,体系中部分组分(仅考虑表内转化)的体积分数
后达到平衡,体系中部分组分(仅考虑表内转化)的体积分数 见下表。
见下表。
①若只考虑体系中反应ⅱ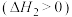 ,以下操作有利于减小
,以下操作有利于减小 平衡转化率的是
平衡转化率的是___________ (填字母)。
A.通入少量 B.使用高选择性催化剂 C.降温 D.减压
B.使用高选择性催化剂 C.降温 D.减压
② 内
内 消耗的平均速率:反应ⅰ
消耗的平均速率:反应ⅰ_________ 反应ⅱ(填“<”、“>”或“=”)。
(3)一定温度下,向 恒容密闭容器中通入
恒容密闭容器中通入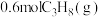 ,压强为
,压强为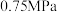 ,若只考虑反应ⅰ、ⅱ,反应后测得各组分的平衡压强(即组分的物质的量分数
,若只考虑反应ⅰ、ⅱ,反应后测得各组分的平衡压强(即组分的物质的量分数 总压)为
总压)为 、
、 ,则该温度下,用物质的量浓度表示反应Ⅰ的平衡常数
,则该温度下,用物质的量浓度表示反应Ⅰ的平衡常数
___________ 。
Ⅱ.共进料投料(耦合反应法)。
工业上也常采用 与
与 共进料投料,通过发生耦合反应制丙烯,反应如下:
共进料投料,通过发生耦合反应制丙烯,反应如下:
(4) 为用压强表示的反应平衡常数,一定温度下:
为用压强表示的反应平衡常数,一定温度下:
ⅰ.

ⅳ.
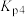
则体系中反应

___________ (用含 、
、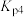 的式子表示)。
的式子表示)。
(5)实际工艺生产中按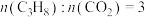 进料,平衡体系中部分组分的体积分数与温度的关系如图所示,综合反应分析:
进料,平衡体系中部分组分的体积分数与温度的关系如图所示,综合反应分析:________ (填“吸热”或“放热”)反应,在________ (填“高温”或“低温”)下进行自发反应。
②生产中温度须不低于 ,原因是
,原因是___________ 。
ⅰ.

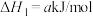
ⅱ.


ⅲ.
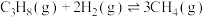
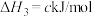
回答下列问题:
Ⅰ.单独投料(副反应抑制法)。
(1)反应:
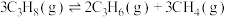

 。
。(2)
 时,单独加入
时,单独加入 至
至 后达到平衡,体系中部分组分(仅考虑表内转化)的体积分数
后达到平衡,体系中部分组分(仅考虑表内转化)的体积分数 见下表。
见下表。| 物质 |  |  |  |  |
体积分数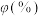 | 18 | 20 | 47 | 0 |
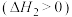 ,以下操作有利于减小
,以下操作有利于减小 平衡转化率的是
平衡转化率的是A.通入少量
 B.使用高选择性催化剂 C.降温 D.减压
B.使用高选择性催化剂 C.降温 D.减压②
 内
内 消耗的平均速率:反应ⅰ
消耗的平均速率:反应ⅰ(3)一定温度下,向
 恒容密闭容器中通入
恒容密闭容器中通入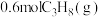 ,压强为
,压强为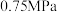 ,若只考虑反应ⅰ、ⅱ,反应后测得各组分的平衡压强(即组分的物质的量分数
,若只考虑反应ⅰ、ⅱ,反应后测得各组分的平衡压强(即组分的物质的量分数 总压)为
总压)为 、
、 ,则该温度下,用物质的量浓度表示反应Ⅰ的平衡常数
,则该温度下,用物质的量浓度表示反应Ⅰ的平衡常数
Ⅱ.共进料投料(耦合反应法)。
工业上也常采用
 与
与 共进料投料,通过发生耦合反应制丙烯,反应如下:
共进料投料,通过发生耦合反应制丙烯,反应如下:
(4)
 为用压强表示的反应平衡常数,一定温度下:
为用压强表示的反应平衡常数,一定温度下:ⅰ.


ⅳ.

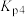
则体系中反应


 、
、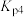 的式子表示)。
的式子表示)。(5)实际工艺生产中按
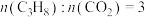 进料,平衡体系中部分组分的体积分数与温度的关系如图所示,综合反应分析:
进料,平衡体系中部分组分的体积分数与温度的关系如图所示,综合反应分析: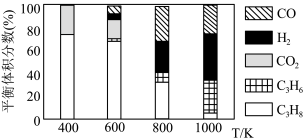
②生产中温度须不低于
 ,原因是
,原因是
您最近一年使用:0次
2 . 下列不能用勒夏特列原理解释的是
A.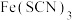 溶液中加入固体KSCN后颜色变深 溶液中加入固体KSCN后颜色变深 |
| B.用热的纯碱溶液洗油污时,去污效果好 |
C.用饱和食盐水除去 中的HCl,可以减少 中的HCl,可以减少 的损失 的损失 |
D.在密闭容器中进行反应 ,增大压强,混合气体颜色加深 ,增大压强,混合气体颜色加深 |
您最近一年使用:0次
2023-02-12更新
|
73次组卷
|
2卷引用:陕西省榆林市2022-2023学年高二上学期教学质量过程性评价化学试题
名校
3 . 能源问题是现代社会发展的三大基本问题之一。
(1)焦炭可用于制取水煤气。实验测得1.2 g 碳与水蒸气完全反应生成水煤气时,吸收了13.16 kJ热量。该反应的热化学方程式为______________ ;该反应在________ 条件下能自发进行(选“高温”、“低温”或“任意温度”)。
(2)甲醇(CH3OH)广泛用作燃料电池的燃料,工业上可由CO和H2来合成,化学方程式为CO(g)+2H2(g) CH3OH(g)。如图是在不同温度下CO的转化率随时间变化的曲线。
CH3OH(g)。如图是在不同温度下CO的转化率随时间变化的曲线。

①T1和T2温度下的平衡常数大小关系是K1________ (填“>”、“<”或“=”)K2。
②若容器容积不变,下列措施不能增加CO转化率的是________ (填字母)。
a.降低温度
b.将CH3OH(g)从体系中分离
c.使用合适的催化剂
③生成甲醇的化学反应速率(v)与时间(t)的关系如图所示。则图中t2时采取的措施可能是_____ ;

④若在T1℃时,往一密闭容器通入等物质的量CO和H2测得容器内总压强1MPa,40min达平衡时测得容器内总压强为0.6MPa,计算生成甲醇的压强平衡常数KP=________ (MPa)-2(小数点后保留2位小数,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)甲醇(CH3OH)燃料电池是以铂为电极,以KOH溶液为电解质溶液,在两极区分别加入CH3OH和O2即可产生电流。请写出负极的电极反应为_______________ 。
(1)焦炭可用于制取水煤气。实验测得1.2 g 碳与水蒸气完全反应生成水煤气时,吸收了13.16 kJ热量。该反应的热化学方程式为
(2)甲醇(CH3OH)广泛用作燃料电池的燃料,工业上可由CO和H2来合成,化学方程式为CO(g)+2H2(g)
 CH3OH(g)。如图是在不同温度下CO的转化率随时间变化的曲线。
CH3OH(g)。如图是在不同温度下CO的转化率随时间变化的曲线。
①T1和T2温度下的平衡常数大小关系是K1
②若容器容积不变,下列措施不能增加CO转化率的是
a.降低温度
b.将CH3OH(g)从体系中分离
c.使用合适的催化剂
③生成甲醇的化学反应速率(v)与时间(t)的关系如图所示。则图中t2时采取的措施可能是

④若在T1℃时,往一密闭容器通入等物质的量CO和H2测得容器内总压强1MPa,40min达平衡时测得容器内总压强为0.6MPa,计算生成甲醇的压强平衡常数KP=
(3)甲醇(CH3OH)燃料电池是以铂为电极,以KOH溶液为电解质溶液,在两极区分别加入CH3OH和O2即可产生电流。请写出负极的电极反应为
您最近一年使用:0次
2020-05-03更新
|
96次组卷
|
2卷引用:陕西省榆林市绥德县绥德中学2019-2020高二下学期第一次阶段性测试化学试题
名校
解题方法
4 . 下列事实不能用勒夏特列原理解释的是
A.对于2HI(g) H2(g)+ I2(g),达平衡后,缩小容器体积可使体系颜色变深 H2(g)+ I2(g),达平衡后,缩小容器体积可使体系颜色变深 |
| B.合成氨反应中为提高氨的产率,理论上应采取降低温度的措施 |
| C.实验室配制FeCl3溶液时,将FeCl3固体加入到少量的浓盐酸中再加水稀释 |
| D.用饱和食盐水可以去除Cl2中的HCl |
您最近一年使用:0次
2020-03-03更新
|
131次组卷
|
3卷引用:陕西省榆林市绥德县绥德中学2019-2020高二下学期第一次阶段性测试化学试题
名校
5 . 某可逆反应正向反应过程中能量变化如图所示,下列说法正确的是
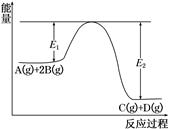

| A.该反应为吸热反应 |
| B.当反应达到平衡时,降低温度,A的转化率减小 |
| C.升高温度平衡常数K增大;压强增大,平衡向正反应方向移动 |
| D.加入催化剂,反应速率增大,E1减小,E2减小,反应热不变 |
您最近一年使用:0次
2016-12-09更新
|
316次组卷
|
7卷引用:陕西省榆林市第十二中学2020-2021学年高二上学期第二次月考化学试题



