1 . 盐酸羟胺(化学式为 )是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。
)是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。
实验室以环己酮肟、盐酸为原料制备盐酸羟胺的反应原理如下:
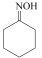 (环己酮肟)
(环己酮肟)
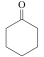 (环己酮)
(环己酮)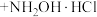
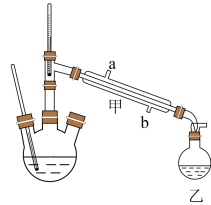
制备盐酸羟胺的实验装置如图所示(加热、搅拌和夹持装置已省略)。
盐酸羟胺在不同温度下的溶解度如下表:
(1)仪器甲中进水口应为___________ 。
A.a处 B.b处 C.a处或b处均可
(2)反应过程中,将环已酮不断蒸出的主要原因是___________ 。
(3)容器乙中收集到环己酮的水溶液,环已酮和水之间存在的相互作用有___________。
(4)反应后,从三口烧瓶的溶液中获取盐酸羟胺的实验方法为___________。
称取0.500g由上述方法制得的盐酸羟胺产品,加水配制成100mL溶液。量取20.00mL于锥形瓶中,加入适量稀硫酸酸化,再加入过量硫酸铁铵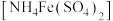 溶液充分反应,接着加入足量磷酸溶液(与
溶液充分反应,接着加入足量磷酸溶液(与 形成无色配合物),最后用
形成无色配合物),最后用 的酸性溶液滴定,达到滴定终点时消耗
的酸性溶液滴定,达到滴定终点时消耗 的酸性溶液的体积为11.35mL。
的酸性溶液的体积为11.35mL。
反应原理为:①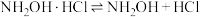
②
③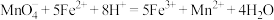
(5)将反应②补充完整,并标出电子转移的方向和数目___________ 。
(6)配制上述盐酸羟胺溶液所需要的定量仪器有___________ 。
A.电子天平 B.100mL容量瓶 C.滴定管 D.量筒
判断滴定终点的现象为___________ 。
(7)通过计算判断该产品的纯度级别___________ 。(写出计算过程)
已知:
 )是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。
)是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。实验室以环己酮肟、盐酸为原料制备盐酸羟胺的反应原理如下:
 (环己酮肟)
(环己酮肟)
 (环己酮)
(环己酮)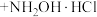
制备盐酸羟胺的实验装置如图所示(加热、搅拌和夹持装置已省略)。

盐酸羟胺在不同温度下的溶解度如下表:
| 温度(℃) | 溶解度(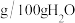 ) ) |
| 20 | 46.7 |
| 40 | 54.9 |
| 60 | 63.2 |
| 80 | 71.1 |
A.a处 B.b处 C.a处或b处均可
(2)反应过程中,将环已酮不断蒸出的主要原因是
(3)容器乙中收集到环己酮的水溶液,环已酮和水之间存在的相互作用有___________。
| A.共价键 | B.离子键 | C.氢键 | D.范德华力 |
| A.冷却结晶 | B.渗析 | C.蒸馏 | D.萃取、分液 |
称取0.500g由上述方法制得的盐酸羟胺产品,加水配制成100mL溶液。量取20.00mL于锥形瓶中,加入适量稀硫酸酸化,再加入过量硫酸铁铵
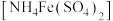 溶液充分反应,接着加入足量磷酸溶液(与
溶液充分反应,接着加入足量磷酸溶液(与 形成无色配合物),最后用
形成无色配合物),最后用 的酸性溶液滴定,达到滴定终点时消耗
的酸性溶液滴定,达到滴定终点时消耗 的酸性溶液的体积为11.35mL。
的酸性溶液的体积为11.35mL。反应原理为:①
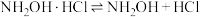
②

③
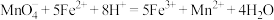
(5)将反应②补充完整,并标出电子转移的方向和数目
(6)配制上述盐酸羟胺溶液所需要的定量仪器有
A.电子天平 B.100mL容量瓶 C.滴定管 D.量筒
判断滴定终点的现象为
(7)通过计算判断该产品的纯度级别
| 纯度级别 | 优级纯 | 分析纯 | 化学纯 |
质量分数 | 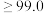 |  |  |

您最近一年使用:0次
2024-01-13更新
|
364次组卷
|
3卷引用:上海市四区联考2023-2024学年高三上学期化学一模试卷
上海市四区联考2023-2024学年高三上学期化学一模试卷上海市嘉定区第二中学2023-2024学年高三上学期第一次质量调研 化学试卷 (已下线)专题09 化学实验综合题-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)
名校
2 . I2O5是白色粉末状固体,在合成氨工业中常用I2O5来定量测量CO的含量。
已知:(I)2I2(s)+5O2(g)=2I2O5(s)
(Π)I2O5(s)+5CO(g) 5CO2(g)+I2(s)
5CO2(g)+I2(s)
(1)结合反应I和反应II分析,I2在CO转化为CO2的反应中所起的作用是______ 。20℃时向装有足量I2O5的2L恒容密闭容器中充入2molCO,发生反应II,反应达到平衡后固体质量减小8g,该温度下反应的平衡常数K=______ (写出计算过程,结果用分数表示)。
(2)若在恒温恒容的密闭体系中进行上述反应II,下列不能说明反应II达到平衡状态的是______ 。
(3)10℃时,某恒容密闭容器中充有足量的I2O5,向该容器中充入CO,发生反应II,平衡时CO2与充入CO的物质的量关系如图所示。
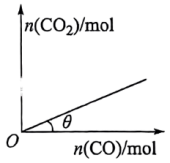
若压缩容器体积;θ值______ (填“增大”“减小”或“不变”),理由是______ 。
已知:(I)2I2(s)+5O2(g)=2I2O5(s)
(Π)I2O5(s)+5CO(g)
 5CO2(g)+I2(s)
5CO2(g)+I2(s)(1)结合反应I和反应II分析,I2在CO转化为CO2的反应中所起的作用是
(2)若在恒温恒容的密闭体系中进行上述反应II,下列不能说明反应II达到平衡状态的是
| A.混合气体的密度保持不变 | B.CO和CO2的物质的量相等 |
| C.v(CO)=v(CO2) | D.混合气体的平均分子量不变 |
(3)10℃时,某恒容密闭容器中充有足量的I2O5,向该容器中充入CO,发生反应II,平衡时CO2与充入CO的物质的量关系如图所示。

若压缩容器体积;θ值
您最近一年使用:0次
22-23高一下·上海·期末
3 . 工业合成氨
(1)合成氨的适宜条件探究:N2(g)+3H2(g) 2NH3(g) + Q(Q>0)
2NH3(g) + Q(Q>0)
∴合成氨的合理生产条件:① 使用___________ 为催化剂 ②一定程度的加压 ③温度控制在催化剂的活性温度(500℃) ④及时分离___________
(1)合成氨的适宜条件探究:N2(g)+3H2(g)
 2NH3(g) + Q(Q>0)
2NH3(g) + Q(Q>0)| 反应条件 | 对化学反应速率的影响 | 对平衡混合物中NH3含量的影响 | 化学反应速率与化学平衡综合考虑 |
| 增大压强 | 影响一致,应 | ||
| 升高温度 | 影响 | ||
| 使用催化剂 | 用合适催化剂有利于加快反应速率 | ||
| 增加反应物浓度 | 平衡向 | 影响一致应 |
您最近一年使用:0次
21-22高三下·上海浦东新·阶段练习
名校
解题方法
4 . 在恒温恒容的容器中发生反应X(g)+nY(g)⇌2M(g)+N(?),下列说法正确的是
| A.若n≠1,X,Y的转化率一定不相等 |
| B.转移走部分N,X的转化率一定增大 |
| C.增大压强,X的转化率减小,N一定为气体 |
| D.增加M的量,M的百分含量一定增大 |
您最近一年使用:0次
2022-04-01更新
|
302次组卷
|
3卷引用:上海市华东师范大学第二附属中学2021-2022年高三下学期3月等级考化学试题
(已下线)上海市华东师范大学第二附属中学2021-2022年高三下学期3月等级考化学试题上海市七宝中学2022-2023学年高二下学期期末考试化学试题四川省遂宁市射洪中学校2021-2022学年高二下学期期中考试化学试题



