1 . 某温度下,反应CH2=CH2(g)+H2O(g) CH3CH2OH(g)在密闭容器中达到平衡。下列说法
CH3CH2OH(g)在密闭容器中达到平衡。下列说法错误 的是
 CH3CH2OH(g)在密闭容器中达到平衡。下列说法
CH3CH2OH(g)在密闭容器中达到平衡。下列说法| A.升高温度,v正减小 |
| B.达到平衡时,CH2=CH2的体积分数不再发生变化 |
| C.恒容下,充入一定量的H2O(g),速率增大 |
| D.加入催化剂,可缩短到达平衡的时间 |
您最近一年使用:0次
2024-02-25更新
|
440次组卷
|
2卷引用:海南中学白沙学校2022-2023学年高一下学期期末考试化学试题
名校
解题方法
2 . 海洋是生命的摇篮,蕴藏着丰富的化学资源。回答下列问题:
(1)粗盐中可溶性杂质离子包含Mg2+、Ca2+、 。要除去这些杂质离子得到精盐水,加入试剂的顺序可为
。要除去这些杂质离子得到精盐水,加入试剂的顺序可为___________
A.BaCl2溶液、NaOH溶液、Na2CO3溶液、盐酸
B.NaOH溶液、Na2CO3溶液、BaCl2溶液、盐酸
C.BaCl2溶液、Na2CO3溶液、NaOH溶液、盐酸
制取 晶体的“结晶”操作为
晶体的“结晶”操作为___________
(2)从海带中提取碘的实验过程如下图所示:
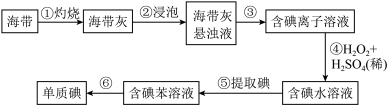
①灼烧海带时,应将海带放入___________ 中灼烧
A.烧杯 B.容量瓶 C.坩埚 D.锥形瓶
②请写出步骤④反应的离子方程式__________ 。
(3)海水显碱性,海水提溴过程中,先调其pH<3.5后,再通入氯气,调节海水pH可提高C12的利用率,用平衡原理解释其原因是___________ 。
(1)粗盐中可溶性杂质离子包含Mg2+、Ca2+、
 。要除去这些杂质离子得到精盐水,加入试剂的顺序可为
。要除去这些杂质离子得到精盐水,加入试剂的顺序可为A.BaCl2溶液、NaOH溶液、Na2CO3溶液、盐酸
B.NaOH溶液、Na2CO3溶液、BaCl2溶液、盐酸
C.BaCl2溶液、Na2CO3溶液、NaOH溶液、盐酸
制取
 晶体的“结晶”操作为
晶体的“结晶”操作为(2)从海带中提取碘的实验过程如下图所示:

①灼烧海带时,应将海带放入
A.烧杯 B.容量瓶 C.坩埚 D.锥形瓶
②请写出步骤④反应的离子方程式
(3)海水显碱性,海水提溴过程中,先调其pH<3.5后,再通入氯气,调节海水pH可提高C12的利用率,用平衡原理解释其原因是
您最近一年使用:0次
名校
3 . 把7 molA气体和5 molB气体混合放入2 L密闭容器中,在一定条件下发生反应:3A(g)+B(g) 2C(s)+2D(g) △H<0,该温度下此反应的平衡常数K=
2C(s)+2D(g) △H<0,该温度下此反应的平衡常数K= ,经5min达到平衡,此时生成2 mol C,求:
,经5min达到平衡,此时生成2 mol C,求:
(1)此反应的平衡常数的表达式___________ ,增大A的浓度,K值___________ (填“增大”“减小”或不变,下同),A的转化率______
(2)压缩容器的容积增大压强,平衡___________ 移动(填“向左”“向右”或“不”)。B的浓度___________ (填“增大”“减小”或不变)
(3)若在相同温度下,测得某个时刻2 L密闭容器中有2molA、4molB、4molC和4molD,则此时该反应
___________  (填“>”“=”或“<”)
(填“>”“=”或“<”)
(4)平衡时D的浓度为___________ ,平衡时压强与初始时压强之比___________
 2C(s)+2D(g) △H<0,该温度下此反应的平衡常数K=
2C(s)+2D(g) △H<0,该温度下此反应的平衡常数K= ,经5min达到平衡,此时生成2 mol C,求:
,经5min达到平衡,此时生成2 mol C,求:(1)此反应的平衡常数的表达式
(2)压缩容器的容积增大压强,平衡
(3)若在相同温度下,测得某个时刻2 L密闭容器中有2molA、4molB、4molC和4molD,则此时该反应

 (填“>”“=”或“<”)
(填“>”“=”或“<”)(4)平衡时D的浓度为
您最近一年使用:0次
名校
4 . 某温度下,在恒容密闭容器中加入一定量X,发生反应 ,一段时间后达到平衡。下列说法正确的是
,一段时间后达到平衡。下列说法正确的是
 ,一段时间后达到平衡。下列说法正确的是
,一段时间后达到平衡。下列说法正确的是| A.升高温度,若c(Z)增大,则△H>0 |
| B.加入一定量氩气,平衡向逆反应方向移动 |
| C.增加X的量,平衡向正反应方向移动,Z的浓度增大 |
| D.将体积增大为原来的2倍,再次达到平衡时,Z的浓度保持不变 |
您最近一年使用:0次
名校
5 . 化学反应通过改变条件可以调控反应速率及反应限度,工业合成氨反应
 ,在400-500℃、10MPa-30MPa、铁触媒为催化剂条件下,实现了氨的高效生产。以合成氨为情境,完成下列填空:
,在400-500℃、10MPa-30MPa、铁触媒为催化剂条件下,实现了氨的高效生产。以合成氨为情境,完成下列填空:
(1)其他条件不变的情况下,缩小容器体积以增大反应体系的压强,逆反应速率v逆___________ (选填“增大”、“减小”、“不变”),平衡___________ 移动(选填“向正反应方向”、“向逆反应方向”、“不影响”)。
(2)其他条件不变的情况下,高温条件下___________ (选填“有利”、“不利”)平衡向正反应方向移动。
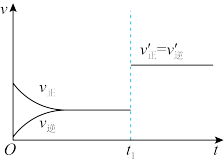
(3)如图为反应速率(v)与时间(t)关系的示意图,由图判断,在 时刻曲线发生变化后,平衡混合物中
时刻曲线发生变化后,平衡混合物中 的百分含量
的百分含量___________ (选填“增大”、“减小”、“不变”)。
(4)若达到平衡时, 、
、 、
、 的物质的量分别为2mol、2mol、1mol。保持温度不变,再充入
的物质的量分别为2mol、2mol、1mol。保持温度不变,再充入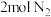 、
、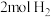 、
、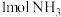 ,则平衡
,则平衡___________ 移动(选填“向正反应方向”、“向逆反应方向”、“不影响”)

 ,在400-500℃、10MPa-30MPa、铁触媒为催化剂条件下,实现了氨的高效生产。以合成氨为情境,完成下列填空:
,在400-500℃、10MPa-30MPa、铁触媒为催化剂条件下,实现了氨的高效生产。以合成氨为情境,完成下列填空:(1)其他条件不变的情况下,缩小容器体积以增大反应体系的压强,逆反应速率v逆
(2)其他条件不变的情况下,高温条件下
(3)如图为反应速率(v)与时间(t)关系的示意图,由图判断,在
 时刻曲线发生变化后,平衡混合物中
时刻曲线发生变化后,平衡混合物中 的百分含量
的百分含量
(4)若达到平衡时,
 、
、 、
、 的物质的量分别为2mol、2mol、1mol。保持温度不变,再充入
的物质的量分别为2mol、2mol、1mol。保持温度不变,再充入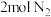 、
、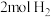 、
、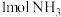 ,则平衡
,则平衡
您最近一年使用:0次



