1 . CuSO4溶液呈蓝色,CuCl2溶液却为黄绿色,因为存在如下的平衡:[Cu(H2O)4 ]2+(蓝色)+ 4Cl- [CuCl4]2-(黄色)+ 4H2O,欲使黄绿色向蓝色转化的操作是
[CuCl4]2-(黄色)+ 4H2O,欲使黄绿色向蓝色转化的操作是
 [CuCl4]2-(黄色)+ 4H2O,欲使黄绿色向蓝色转化的操作是
[CuCl4]2-(黄色)+ 4H2O,欲使黄绿色向蓝色转化的操作是| A.通入H2S气体 | B.加水稀释 | C.加入AgNO3溶液 | D.加入NaBr固体 |
您最近一年使用:0次
2 . 反应 C2H6(g) =C2H4(g) +H2(g) ∆H>0 在一定条件下于密闭容器中达到平衡,下列各项措施中,不能提高乙烷(C2H6)的平衡转化率的是
| A.增大压强 | B.升高反应温度 | C.分离出部分氢气 | D.等容下通入惰性气体 |
您最近一年使用:0次
解题方法
3 . 关于反应A(g)+B(g) C(g) ΔH<0,下列说法中,正确的是
C(g) ΔH<0,下列说法中,正确的是
 C(g) ΔH<0,下列说法中,正确的是
C(g) ΔH<0,下列说法中,正确的是| A.一定是自发反应 |
| B.温度升高,化学反应速率加快 |
| C.反应物浓度增大,平衡向正反应方向移动 |
| D.催化剂不参与化学反应 |
您最近一年使用:0次
名校
4 . 可逆反应2SO2+O2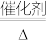 2SO3 △H<0,开始把2molSO2和1molO2充入容积为2L的恒容密闭容器中,在500℃条件下达化学平衡,下列说法中正确的是
2SO3 △H<0,开始把2molSO2和1molO2充入容积为2L的恒容密闭容器中,在500℃条件下达化学平衡,下列说法中正确的是
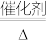 2SO3 △H<0,开始把2molSO2和1molO2充入容积为2L的恒容密闭容器中,在500℃条件下达化学平衡,下列说法中正确的是
2SO3 △H<0,开始把2molSO2和1molO2充入容积为2L的恒容密闭容器中,在500℃条件下达化学平衡,下列说法中正确的是| A.升高温度平衡向正反应方向移动 |
| B.增大压强SO2的转化率增大 |
| C.加入催化剂平衡不发生移动,但反应速率加快 |
| D.只增大SO2浓度平衡不移动 |
您最近一年使用:0次
5 . 对于平衡体系mA(g)+nB(g) pC(g)+qD(g) △H<0。下列结论正确的是
pC(g)+qD(g) △H<0。下列结论正确的是
 pC(g)+qD(g) △H<0。下列结论正确的是
pC(g)+qD(g) △H<0。下列结论正确的是| A.若温度不变,将容器的体积缩小到原来的一半,达到新平衡时A的浓度为原来的2.2倍,则m+n>p+q |
| B.若m+n=p+q,则向含有amol气体的平衡体系中再加入amol的B,达到新平衡时气体的总物质的量等于2amol |
| C.若平衡时,A.B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n |
| D.温度升高时,K值增大 |
您最近一年使用:0次
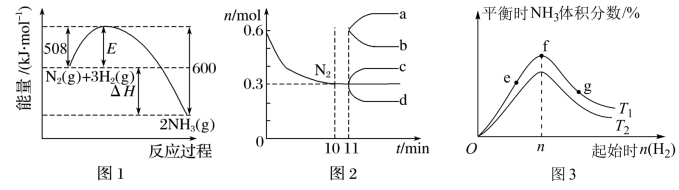
6 . 一定条件下,合成氨反应: 。图1表示在该反应过程中的能量的变化,图2表示在2L的密闭容器中反应时
。图1表示在该反应过程中的能量的变化,图2表示在2L的密闭容器中反应时 的物质的量随时间的变化曲线,图3表示在其他条件不变的情况下,改变起始物
的物质的量随时间的变化曲线,图3表示在其他条件不变的情况下,改变起始物 的物质的量对该反应平衡的影响。下列说法正确的是
的物质的量对该反应平衡的影响。下列说法正确的是
 。图1表示在该反应过程中的能量的变化,图2表示在2L的密闭容器中反应时
。图1表示在该反应过程中的能量的变化,图2表示在2L的密闭容器中反应时 的物质的量随时间的变化曲线,图3表示在其他条件不变的情况下,改变起始物
的物质的量随时间的变化曲线,图3表示在其他条件不变的情况下,改变起始物 的物质的量对该反应平衡的影响。下列说法正确的是
的物质的量对该反应平衡的影响。下列说法正确的是
A.升高温度,正、逆反应速率均加快, 的转化率增大 的转化率增大 |
B.由图2信息,从11min起其他条件不变,增加 的量,则 的量,则 的变化曲线为b 的变化曲线为b |
C.由图2信息,10min末该反应以 表示的反应速率为 表示的反应速率为 |
D.图3中温度 ,e、f、g三点所处的平衡状态中,反应物 ,e、f、g三点所处的平衡状态中,反应物 的转化率最高的是g点 的转化率最高的是g点 |
您最近一年使用:0次
2021高三·全国·专题练习
7 . “减少碳排放,实现碳中和”是当今世界的热门话题。某课题组利用CO2和H2在催化剂的作用下合成甲醇,主要发生如下三个反应:
I. CO2(g)+3H2(g)→CH3OH(g)+H2O(g) ΔH1=-49.5kJ·mol-1
II.CO2(g)+H2(g)→CO(g)+H2O(g) ΔH2=+40.9kJ·mol-1
III.……
下列措施中,能提高CO2转化率的是___________。
I. CO2(g)+3H2(g)→CH3OH(g)+H2O(g) ΔH1=-49.5kJ·mol-1
II.CO2(g)+H2(g)→CO(g)+H2O(g) ΔH2=+40.9kJ·mol-1
III.……
下列措施中,能提高CO2转化率的是___________。
| A.在原料气中加入适量H2O(g) |
| B.从体系中不断分离出甲醇 |
| C.循环利用原料气 |
| D.使用高效催化剂 |
您最近一年使用:0次
8 . 下列有关化学与生活、工业的叙述中错误的是
| A.实验室制取H2时,用浓硫酸代替稀硫酸可加快反应速率 |
| B.制取乙酸乙酯时,加入浓硫酸,可加快酯化反应的速率,增大乙酸乙酯的产率 |
| C.硫酸工业中,使用催化剂可加快SO2转化为SO3的速率,有利于提高SO2的平衡转化率 |
| D.CO会与血红蛋白结合使人中毒,中毒反应为CO+HbO=O2+HbCO,可将中毒病人放入高压氧舱中解毒 |
您最近一年使用:0次
解题方法
9 . 根据下列实验操作及现象所得出的结论或解释正确的是
| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A | FeCl3+3KSCN⇌Fe(SCN)3+3KCl在平衡体系中加入KCl晶体 | 溶液颜色不变 | 加入少量KCl晶体,不会影响该化学平衡 |
| B | 取相同大小、形状和质量的Cu粒分别投入稀硝酸和浓硝酸中 | Cu粒与浓硝酸反应更剧烈 | 实验目的是探究浓度对化学反应速率的影响 |
| C | 将20℃0.5mol·Lˉ1Na2CO3溶液加热到60℃,用传感器测定溶液pH | 溶液的pH逐渐减小 | Kw改变与水解平衡移动共同作用的结果 |
| D | 用pH试纸测得相同浓度的CH3COONa溶液、NaNO2溶液的pH | CH3COONa溶液pH约为9,NaNO2溶液的pH约为8 | CH3COOH的酸性比HNO2强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
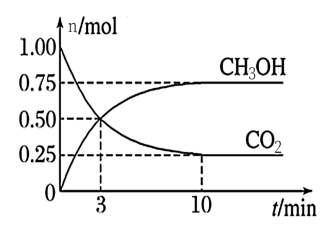
10 . 工业上可以用CO2来生产甲醇燃料。在体积为2 L的密闭容器中,充入l mol CO2和3 mol H2,一定条件下发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g)。测得CH3OH和CO2的物质的量随时间变化如图所示。下列描述正确的是
CH3OH(g)+H2O(g)。测得CH3OH和CO2的物质的量随时间变化如图所示。下列描述正确的是
 CH3OH(g)+H2O(g)。测得CH3OH和CO2的物质的量随时间变化如图所示。下列描述正确的是
CH3OH(g)+H2O(g)。测得CH3OH和CO2的物质的量随时间变化如图所示。下列描述正确的是
| A.达到平衡时,H2的转化率为75% |
| B.3 min 时,CH3OH和CO2的浓度相等,达到了化学平衡状态 |
| C.反应进行到10 min后,向容器中再充入CO2,则CO2的转化率会增大 |
| D.反应开始到10 min,用CO2表示的反应速率为0.0375 mol·L-1·min-1 |
您最近一年使用:0次



