1 . 某实验将 和
和 充入一定体积的密闭容器中,在不同温度下发生反应:
充入一定体积的密闭容器中,在不同温度下发生反应:
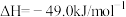 ,测得
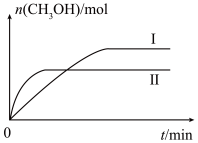
,测得 的物质的量随时间变化如下图所示,回答问题:
的物质的量随时间变化如下图所示,回答问题:
(1)该反应的平衡常数表达式为
_______ 。
(2)曲线I、Ⅱ对应的温度
_______  (填“>”或“<”)。
(填“>”或“<”)。
平衡常数关系为
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(3)其他条件不变时,下列措施能提高 转化率的是_______(填字母代号)。
转化率的是_______(填字母代号)。
(4)其他条件不变时,将容器体积扩大一倍,平衡向_______ 移动(填“正向”、“逆向”或“不”)
 和
和 充入一定体积的密闭容器中,在不同温度下发生反应:
充入一定体积的密闭容器中,在不同温度下发生反应:
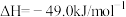 ,测得
,测得 的物质的量随时间变化如下图所示,回答问题:
的物质的量随时间变化如下图所示,回答问题:
(1)该反应的平衡常数表达式为

(2)曲线I、Ⅱ对应的温度

 (填“>”或“<”)。
(填“>”或“<”)。平衡常数关系为

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(3)其他条件不变时,下列措施能提高
 转化率的是_______(填字母代号)。
转化率的是_______(填字母代号)。A.减小 的浓度 的浓度 | B.降低温度 |
C.增加 的浓度 的浓度 | D.增大压强 |
您最近一年使用:0次
解题方法
2 . 25℃时,根据下列实验及现象不能推出相应结论的是
| 序号 | 实验及现象 | 结论 |
| A | 缓慢加热 溶液至60℃,用 溶液至60℃,用 传感器测得溶液 传感器测得溶液 逐渐减小 逐渐减小 | 溶液中 逐渐增大, 逐渐增大, 逐渐减小 逐渐减小 |
| B | 乙酸乙酯在碱性条件下水解,用电导仪测得溶液电导率逐渐减小 |  的电导率大于 的电导率大于 的电导率 的电导率 |
| C | 将等量的柠檬酸钠分别加入等体积的水和盐酸中,用温度传感器测得后者溶液温度更低 | 柠檬酸钠和盐酸的反应为吸热反应 |
| D | 压缩 和 和 混合气体,用色度传感器测得气体颜色先变深后缓慢变浅 混合气体,用色度传感器测得气体颜色先变深后缓慢变浅 |  平衡正向移动 平衡正向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 利用 催化氮气合成氨气,并生成CO、
催化氮气合成氨气,并生成CO、 等燃料气的方程式如下所示:
等燃料气的方程式如下所示:
反应①:
反应②:
(1)氮原子核外电子排布式为:_______ 。
(2)比较C、N、O原子的半径大小:_______ 。
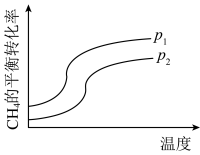
(3)反应①的进程如图所示,则 和
和 的大小为:
的大小为:_______ 。
(4)某一2L恒温恒容装置,反应前充入3mol甲烷,10min后,甲烷为1.2mol,求前10min氮气的反应速率为:_______ 。
(5)写出反应①和反应②的总反应方程式:_______ 。
(6)这个制取氨气的方法和工业制取氨气相比,优点是:_______ 、_______ 。
 催化氮气合成氨气,并生成CO、
催化氮气合成氨气,并生成CO、 等燃料气的方程式如下所示:
等燃料气的方程式如下所示:反应①:

反应②:

(1)氮原子核外电子排布式为:
(2)比较C、N、O原子的半径大小:
(3)反应①的进程如图所示,则
 和
和 的大小为:
的大小为:
(4)某一2L恒温恒容装置,反应前充入3mol甲烷,10min后,甲烷为1.2mol,求前10min氮气的反应速率为:
(5)写出反应①和反应②的总反应方程式:
(6)这个制取氨气的方法和工业制取氨气相比,优点是:
您最近一年使用:0次



