利用 催化氮气合成氨气,并生成CO、
催化氮气合成氨气,并生成CO、 等燃料气的方程式如下所示:
等燃料气的方程式如下所示:
反应①:
反应②:
(1)氮原子核外电子排布式为:_______ 。
(2)比较C、N、O原子的半径大小:_______ 。
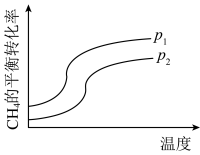
(3)反应①的进程如图所示,则 和
和 的大小为:
的大小为:_______ 。
(4)某一2L恒温恒容装置,反应前充入3mol甲烷,10min后,甲烷为1.2mol,求前10min氮气的反应速率为:_______ 。
(5)写出反应①和反应②的总反应方程式:_______ 。
(6)这个制取氨气的方法和工业制取氨气相比,优点是:_______ 、_______ 。
 催化氮气合成氨气,并生成CO、
催化氮气合成氨气,并生成CO、 等燃料气的方程式如下所示:
等燃料气的方程式如下所示:反应①:

反应②:

(1)氮原子核外电子排布式为:
(2)比较C、N、O原子的半径大小:
(3)反应①的进程如图所示,则
 和
和 的大小为:
的大小为:
(4)某一2L恒温恒容装置,反应前充入3mol甲烷,10min后,甲烷为1.2mol,求前10min氮气的反应速率为:
(5)写出反应①和反应②的总反应方程式:
(6)这个制取氨气的方法和工业制取氨气相比,优点是:
更新时间:2023-03-17 10:26:15
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】铁、钴(Co)、镍(Ni)是同族元素,它们的化合物在工业上有重要的应用。
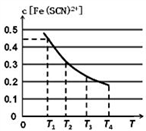
(1)现将含0.5mol FeCl3的溶液和含0.5mol KSCN的溶液混合,混合后溶液体积为1L,已知溶液存在平衡:Fe3+(aq)+SCN-(aq) Fe(SCN)2+(aq)(忽略其它过程)。平衡浓度c[Fe(SCN)2+]与温度T的关系如图所示:温度为T1时,反应在5秒钟时达到平衡,平衡时c[Fe(SCN)2+]=0.45 mol·L-1,求达到平衡时的平均反应速率v(SCN-)=
Fe(SCN)2+(aq)(忽略其它过程)。平衡浓度c[Fe(SCN)2+]与温度T的关系如图所示:温度为T1时,反应在5秒钟时达到平衡,平衡时c[Fe(SCN)2+]=0.45 mol·L-1,求达到平衡时的平均反应速率v(SCN-)=____________ ,该温度下的Fe3+的平衡转化率为_____________ ,该温度下反应的平衡常数为__________ 。
(2)羰基法提纯镍涉及的一个反应为:Ni(s)+4CO(g) Ni(CO)4(g)
Ni(CO)4(g)
①当温度升高时,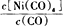 减小,则该反应的⊿H
减小,则该反应的⊿H_____ 0(填“>”或“<”)。
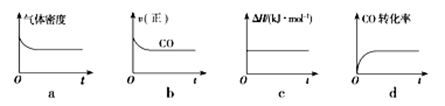
②一定温度下,将一定量的粗镍和CO加入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是________ (填代号)。
(3)CoxNi(1-x)Fe2O4 (其中Co、Ni均为+2价)可用作H2O2分解的催化剂,具有较高的活性。两种不同方法制得的催化剂在10℃时催化、分解6%的H2O2溶液的相对初始速率随x变化的曲线如右图所示。
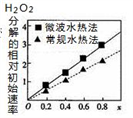
由图中信息可知__________ 法制取得到的催化剂活性更高;Co2+、Ni2+ 两种离子中催化效果较好的是_____ 。
(1)现将含0.5mol FeCl3的溶液和含0.5mol KSCN的溶液混合,混合后溶液体积为1L,已知溶液存在平衡:Fe3+(aq)+SCN-(aq)
 Fe(SCN)2+(aq)(忽略其它过程)。平衡浓度c[Fe(SCN)2+]与温度T的关系如图所示:温度为T1时,反应在5秒钟时达到平衡,平衡时c[Fe(SCN)2+]=0.45 mol·L-1,求达到平衡时的平均反应速率v(SCN-)=
Fe(SCN)2+(aq)(忽略其它过程)。平衡浓度c[Fe(SCN)2+]与温度T的关系如图所示:温度为T1时,反应在5秒钟时达到平衡,平衡时c[Fe(SCN)2+]=0.45 mol·L-1,求达到平衡时的平均反应速率v(SCN-)=
(2)羰基法提纯镍涉及的一个反应为:Ni(s)+4CO(g)
 Ni(CO)4(g)
Ni(CO)4(g)①当温度升高时,
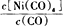 减小,则该反应的⊿H
减小,则该反应的⊿H②一定温度下,将一定量的粗镍和CO加入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是

(3)CoxNi(1-x)Fe2O4 (其中Co、Ni均为+2价)可用作H2O2分解的催化剂,具有较高的活性。两种不同方法制得的催化剂在10℃时催化、分解6%的H2O2溶液的相对初始速率随x变化的曲线如右图所示。

由图中信息可知
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】650℃时,在2L的密闭容器内发生 的反应,其中n(A)随时间的变化如下表:
的反应,其中n(A)随时间的变化如下表:
(1)求从0~2min内该反应的平均速率:v(A)=___________ ;4min时C的物质的量n(C)=___________ 。
(2)在第5min时,A的转化率为___________ 。
(3)如图所示,表示C变化曲线的是___________ 。
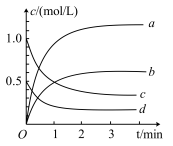
(4)能说明该反应已达到平衡状态的是___________ 。
a.v(A)=2v(B) b.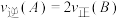
c.容器内密度保持不变 d.混合气体中A的体积分数保持不变
 的反应,其中n(A)随时间的变化如下表:
的反应,其中n(A)随时间的变化如下表:| t/(min) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(A)/mol | 2.0 | 1.0 | 0.8 | 0.7 | 0.7 | 0.7 |
(2)在第5min时,A的转化率为
(3)如图所示,表示C变化曲线的是

(4)能说明该反应已达到平衡状态的是
a.v(A)=2v(B) b.
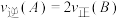
c.容器内密度保持不变 d.混合气体中A的体积分数保持不变
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】我国含煤量和煤使用量均为全球第一,所以如何提高煤的使用效率,同时减少对环境的危害一直是我国科学家研究的重要课题。其中重要的汽化反应为:CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
(1)已知:2CO(g)+O2(g)=2CO2(g) △H=-566 kJ/mol;2H2(g)+O2(g)=2H2O(g) △H=-484 kJ/mol,则反应CO和水蒸气反应生成CO2和H2的热化学方程式:_______ 。
(2)为提高该汽化反应的CO转化率,可采用的方法有_______(填编号)。
(3)在3L密闭容器中,将4.0 mol CO与8.0 mol H2O混合迅速加热到600℃,在600℃时跟踪测定CO的物质的量变化如图所示:
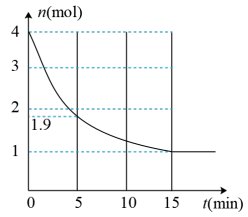
①该体系在第_______ min时达到化学平衡,从反应开始到5 min时,用CO2表示的反应速率为_______ ,600℃的平衡常数为_______ 。
②保持温度不变,15 min后向该密闭容器中再次充入3 mol CO、1 mol H2O(g)、1 mol CO2(g)、1 mol H2(g),此时平衡_______ (填“正移”、“不移”或“逆移”),其原因是_______ 。
 CO2(g)+H2(g)
CO2(g)+H2(g)(1)已知:2CO(g)+O2(g)=2CO2(g) △H=-566 kJ/mol;2H2(g)+O2(g)=2H2O(g) △H=-484 kJ/mol,则反应CO和水蒸气反应生成CO2和H2的热化学方程式:
(2)为提高该汽化反应的CO转化率,可采用的方法有_______(填编号)。
| A.选择适当的催化剂 | B.增大压强 |
| C.升高温度 | D.及时分离出CO2 |
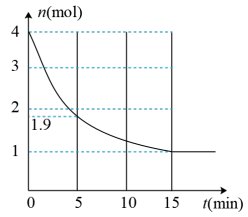
①该体系在第
②保持温度不变,15 min后向该密闭容器中再次充入3 mol CO、1 mol H2O(g)、1 mol CO2(g)、1 mol H2(g),此时平衡
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】氢能是一种极具发展潜力的清洁能源,以下反应是目前大规模制取氢气的重要方法之一:
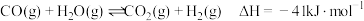
(1)为提高该反应中 的平衡转化率,理论上可以采取的措施为
的平衡转化率,理论上可以采取的措施为___________ 。
a.增大压强 b.升高温度 c.通入过量水蒸气
(2) 时,该反应的平衡常数
时,该反应的平衡常数 。该温度下,在容积为
。该温度下,在容积为 的密闭容器中进行反应,测得某一时刻反应混合物中
的密闭容器中进行反应,测得某一时刻反应混合物中 、
、 、
、 、
、 的物质的量分别为
的物质的量分别为 、
、 、
、 、
、 。
。
①该时刻反应的浓度商
___________ (填计算结果)。
②该时刻反应___________ (填“正向进行”或“逆向进行”或“已达平衡”)。
(3) 时,该反应的平衡常数
时,该反应的平衡常数 ,该温度下,在容积为
,该温度下,在容积为 的密闭容器中投入
的密闭容器中投入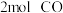 与
与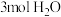 。反应达平衡时
。反应达平衡时 的转化率为
的转化率为___________ 。
(4)下图表示不同温度下, 平衡转化率随
平衡转化率随 的变化趋势。
的变化趋势。 、
、 和
和 的三个温度中最大的是
的三个温度中最大的是___________ (填“ ”或“
”或“ ”或“
”或“ ”),原因是
”),原因是___________ 。
已知: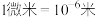 ,
,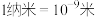
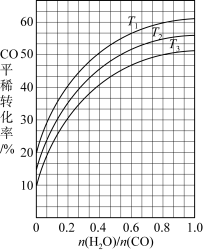
(5)实验发现,其它条件不变,一定反应时间内,向反应体系中投入一定量的 可以增大
可以增大 的物质的量分数,实验结果如图所示。相比使用微米
的物质的量分数,实验结果如图所示。相比使用微米 ,使用纳米
,使用纳米 时
时 的物质的量分数更大的可能原因是
的物质的量分数更大的可能原因是___________ 。

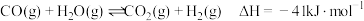
(1)为提高该反应中
 的平衡转化率,理论上可以采取的措施为
的平衡转化率,理论上可以采取的措施为a.增大压强 b.升高温度 c.通入过量水蒸气
(2)
 时,该反应的平衡常数
时,该反应的平衡常数 。该温度下,在容积为
。该温度下,在容积为 的密闭容器中进行反应,测得某一时刻反应混合物中
的密闭容器中进行反应,测得某一时刻反应混合物中 、
、 、
、 、
、 的物质的量分别为
的物质的量分别为 、
、 、
、 、
、 。
。①该时刻反应的浓度商

②该时刻反应
(3)
 时,该反应的平衡常数
时,该反应的平衡常数 ,该温度下,在容积为
,该温度下,在容积为 的密闭容器中投入
的密闭容器中投入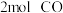 与
与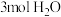 。反应达平衡时
。反应达平衡时 的转化率为
的转化率为(4)下图表示不同温度下,
 平衡转化率随
平衡转化率随 的变化趋势。
的变化趋势。 、
、 和
和 的三个温度中最大的是
的三个温度中最大的是 ”或“
”或“ ”或“
”或“ ”),原因是
”),原因是
已知:
 ,
,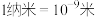
(5)实验发现,其它条件不变,一定反应时间内,向反应体系中投入一定量的
 可以增大
可以增大 的物质的量分数,实验结果如图所示。相比使用微米
的物质的量分数,实验结果如图所示。相比使用微米 ,使用纳米
,使用纳米 时
时 的物质的量分数更大的可能原因是
的物质的量分数更大的可能原因是
您最近半年使用:0次
【推荐2】CO2是最强温室气体,研究CO2的有效利用、制造更高价值化学品具有重大意义。以CO2为主要原料可合成清洁能源二甲醚。已知:
I.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H1=-49.1kJ/mol;
II.2CH3OH(g)⇌CH3OCH3(g)+H2O(g) △H2=-24.5kJ/mol;
II.CO2(g)+H2(g)⇌CO(g)+H2O(g) △H3=+41.2kJ/mol
(1)CO2(g)与H2(g)转化为CH3OCH3(g)和H2O(g)的热化学方程式为____________ 。
(2)为实现上述反应I在常温常压下进行,科学家设计了如图所示装置(其中质子交换膜允许H+通过)。该装置为______ (填“原电池”或“电解池”),甲槽中电极上发生的反应式为_________ 。
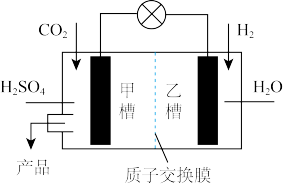
(3)在10.0L的密闭容器中投入1molCO2和2.75molH2,在不同条件下发生反应I,实验测得平衡时甲醇的物质的量随温度、压强变化如图:

①图中压强p1______ (填">”或“<")p2。
②在图中M点,平衡常数K=__________ (计算结果保留2位小数)。
I.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H1=-49.1kJ/mol;
II.2CH3OH(g)⇌CH3OCH3(g)+H2O(g) △H2=-24.5kJ/mol;
II.CO2(g)+H2(g)⇌CO(g)+H2O(g) △H3=+41.2kJ/mol
(1)CO2(g)与H2(g)转化为CH3OCH3(g)和H2O(g)的热化学方程式为
(2)为实现上述反应I在常温常压下进行,科学家设计了如图所示装置(其中质子交换膜允许H+通过)。该装置为

(3)在10.0L的密闭容器中投入1molCO2和2.75molH2,在不同条件下发生反应I,实验测得平衡时甲醇的物质的量随温度、压强变化如图:

①图中压强p1
②在图中M点,平衡常数K=
您最近半年使用:0次
【推荐3】俄乌两国都是产粮大国,2022年2月至今两国冲突导致世界粮食供应紧张。羰基硫(COS)是一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在容积不变的密闭容器中,将CO和H2S混合后在催化剂和加热并达到下列平衡:CO(g)+H2S(g) COS(g)+H2(g)。
COS(g)+H2(g)。
(1)已知COS结构与CO2相似,COS的电子式为_______ 。若反应前CO的物质的量为10mol,达到平衡时CO的物质的量为8mol,且化学平衡常数为0.1。下列说法正确的是_______ (填字母)。
a.增大压强,化学平衡正向移动
b.增大CO浓度,正反应速率增大,逆反应速率减小
c.反应前H2S的物质的量为7mol
d.达到平衡时CO的转化率为20%
(2)①在不同温度下达到化学平衡时,H2S的转化率如图所示,则该反应是_______ (填“吸热”或“放热”)。
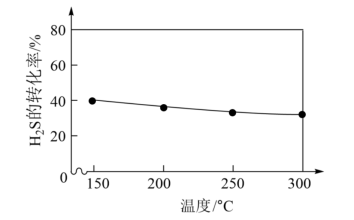
②若采用恒压,当温度高于300℃后,H2S的转化率出现了断崖式下跌,原因可能是_______ 、_______ 。(写出任意两点即可)。
(3)增大c(H2S)/c(CO)的值,可以_______ (填“增大”或“减小”)CO的转化率。工业上H2S尾气的处理方法中,克劳斯法是将三分之一H2S氧化为SO2,再在转化炉中将剩下的H2S转化为S单质,写出转化炉中反应的化学方程式_______ 。实验室中H2S气体常用过量的氢氧化钠溶液吸收,写出反应的离子方程式_______ 。
 COS(g)+H2(g)。
COS(g)+H2(g)。(1)已知COS结构与CO2相似,COS的电子式为
a.增大压强,化学平衡正向移动
b.增大CO浓度,正反应速率增大,逆反应速率减小
c.反应前H2S的物质的量为7mol
d.达到平衡时CO的转化率为20%
(2)①在不同温度下达到化学平衡时,H2S的转化率如图所示,则该反应是

②若采用恒压,当温度高于300℃后,H2S的转化率出现了断崖式下跌,原因可能是
(3)增大c(H2S)/c(CO)的值,可以
您最近半年使用:0次
【推荐1】X、Y、Z、M、Q、R是元素周期表前四周期元素,且原子序数依次增大,其相关信息如下表:
请用化学用语填空:
(1)X元素位于元素周期表第___________ 周期___________ 族; R是___________ 区的元素。
(2)请写出Q元素基态原子的外围电子排布图:___________ 。
(3)X、Y、Z、M四种元素的原子半径由小到大的顺序是___________ (用元素符号表示)。
(4)R元素可形成R2+和R3+,其中较稳定的是R3+,原因是___________ 。
(5)与M元素成“对角线规则”关系的某短周期元素T的最高价氧化物的水化物具有两性,写出该两性物质与Z元素的最高价氧化物的水化物反应的化学方程式:___________ ;已知T元素和Q元素的电负性分别为1.5和3.0,则它们形成的化合物是___________ (填“离子化合物”或“共价化合物”)。
| 元素 | 相关信息 |
| X | 原子核外有6种不同运动状态的电子 |
| Y | 基态原子中s电子总数与p电子总数相等 |
| Z | 原子半径在同周期元素中最大 |
| M | 逐级电离能(kJ·mol-1)依次为 578、1 817、2 745、11 575、14 830、18 376 |
| Q | 基态原子的最外层p轨道上有两个电子的自旋方向与其他电子的自旋方向相反 |
| R | 基态原子核外有7个能级且能量最高的能级上有6个电子 |
(1)X元素位于元素周期表第
(2)请写出Q元素基态原子的外围电子排布图:
(3)X、Y、Z、M四种元素的原子半径由小到大的顺序是
(4)R元素可形成R2+和R3+,其中较稳定的是R3+,原因是
(5)与M元素成“对角线规则”关系的某短周期元素T的最高价氧化物的水化物具有两性,写出该两性物质与Z元素的最高价氧化物的水化物反应的化学方程式:
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】如图为元素周期表的一部分,请参照元素①~⑨在图中的位置,回答下列问题。
(1)第三周期元素中非金属性最强的元素的原子结构示意图是_________ 。
(2)①~⑨号元素中,原子半径最大的是:_________ (填元素符号),⑧和⑨的离子半径相比较小的是:_________ (填离子符号);
(3)下列可以判断⑤和⑥金属性强弱的是_________ (填序号)。
a.单质的熔点:⑤<⑥
b.化合价:⑤<⑥
c.单质与水反应的剧烈程度:⑤>⑥
d.最高价氧化物对应水化物的碱性:⑤>⑥
(4)元素⑤和元素⑥各自的最高价氧化物对应水化物相互反应的离子方程式为:_________ 。
(5)为验证第ⅦA族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:
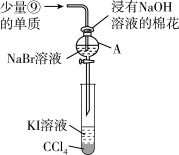
①仪器A的名称是_________ ,A中发生反应的离子方程式是_________ 。
②棉花中浸有 溶液的作用是
溶液的作用是_________ (用离子方程式表示)。
③验证溴与碘的非金属性强弱:通入少量⑨的单质,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到溶液分层,下层液体为紫红色。该实验必须控制⑨单质的加入量,否则得不出溴的非金属性比碘强的结论,理由是_________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(2)①~⑨号元素中,原子半径最大的是:
(3)下列可以判断⑤和⑥金属性强弱的是
a.单质的熔点:⑤<⑥
b.化合价:⑤<⑥
c.单质与水反应的剧烈程度:⑤>⑥
d.最高价氧化物对应水化物的碱性:⑤>⑥
(4)元素⑤和元素⑥各自的最高价氧化物对应水化物相互反应的离子方程式为:
(5)为验证第ⅦA族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:

①仪器A的名称是
②棉花中浸有
 溶液的作用是
溶液的作用是③验证溴与碘的非金属性强弱:通入少量⑨的单质,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到溶液分层,下层液体为紫红色。该实验必须控制⑨单质的加入量,否则得不出溴的非金属性比碘强的结论,理由是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】短周期主族元素W、X、Y、Z的原子序数依次增大,W的最简单氢化物甲是一种能使湿润的红色石蕊试纸变蓝的无色气体,常用作制冷剂,Y的金属性是所有短周期主族元素中最强的,Z与X属于同一主族,Z与Y属于同一周期。
(1)元素W在周期表中位置为_______________ 。
(2)元素W的另一常见氢化物乙是一种高能燃料,为18电子微粒,乙的结构式为___________ 。
(3)X、Y、Z的原子半径由小到大的顺序为_________________ 。
(4)若X与Z的最外层电子数之和是W核外电子数的2倍,甲可与Z单质发生置换反应,产物之一可作化肥,其反应的化学方程式为___________________ ,该产物化肥中含有的化学键有________________ 。
(5)若由X、Y和Z三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀析出,同时有刺激性气味气体产生。则元素Z是______ (填元素符号),反应的离子方程式为________________ 。
(1)元素W在周期表中位置为
(2)元素W的另一常见氢化物乙是一种高能燃料,为18电子微粒,乙的结构式为
(3)X、Y、Z的原子半径由小到大的顺序为
(4)若X与Z的最外层电子数之和是W核外电子数的2倍,甲可与Z单质发生置换反应,产物之一可作化肥,其反应的化学方程式为
(5)若由X、Y和Z三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀析出,同时有刺激性气味气体产生。则元素Z是
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】锌的化合物在生产生活中有广泛的应用。
(1)L-赖氨酸锌螯合物X (结构为如图)易被人体吸收。

①X中元素(除H外)的第一电离能由小到大的顺序为_______ ,加“*”氧原子的杂化方式为_______ 。
②X的晶体中存在的微粒间作用力有._______ 。
A.离子键 B. π键 C.金属键 D.配位键 E.非极性键
③L-赖氨酸易溶于水主要原因是_______ 。
(2)某锌铁氧体[化学式为ZnxFe(III)yOz]制成的磁芯被广泛用于电子行业。
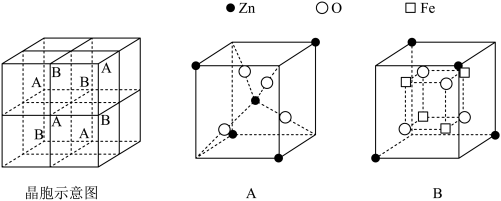
①组成微粒的原子(或离子)中存在未成对电子,该微粒具有顺磁性。指出锌铁氧体晶体中具有顺磁性的离子,并说明理由_______ 。
②锌铁氧体晶胞结构如图所示,该晶胞由4个A型和4个B型小立方体构成。锌铁氧体的化学式为_______ 。
(1)L-赖氨酸锌螯合物X (结构为如图)易被人体吸收。

①X中元素(除H外)的第一电离能由小到大的顺序为
②X的晶体中存在的微粒间作用力有.
A.离子键 B. π键 C.金属键 D.配位键 E.非极性键
③L-赖氨酸易溶于水主要原因是
(2)某锌铁氧体[化学式为ZnxFe(III)yOz]制成的磁芯被广泛用于电子行业。
①组成微粒的原子(或离子)中存在未成对电子,该微粒具有顺磁性。指出锌铁氧体晶体中具有顺磁性的离子,并说明理由
②锌铁氧体晶胞结构如图所示,该晶胞由4个A型和4个B型小立方体构成。锌铁氧体的化学式为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】B、N、F、Ga、As是新一代太阳能电池、半导体材料中含有的主要元素。回答下列问题:
(1)基态Ga原子的核外电子排布式是__________ ,基态Ga原子核外电子占据最高能级的电子云轮廓图为________ 。
(2)在第四周期中,与基态As原子核外未成对电子数目相同的元素为__________ 。
(3)NF3的立体构型为_______ 。N2F2分子中各原子都满足8电子结构,分子中σ键和π键的个数比为______ ,氮原子的杂化轨道类型为__________ 。
(4)B、Al、Ga单质的熔点依次为2300°C,660°C,29.8°C,解释熔点产生差异的原因______ 。
(5)由B、N、F组成的某离子化合物中,B、N、F的原子个数比为1:1:8,其阴、阳离子互为等电子体,该化合物中的阳离子、阴离子符号分别为__________ 。
(6)GaAs晶体结构如图所示。
①图中As原子的坐标参数为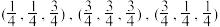 ,
,_______ 。
②已知晶胞中相邻且最近的Ga、As原子的核间距为acm,NA为阿伏加 德罗常数的值,晶体的密度为___________ g/cm3(填写表达式)。

(1)基态Ga原子的核外电子排布式是
(2)在第四周期中,与基态As原子核外未成对电子数目相同的元素为
(3)NF3的立体构型为
(4)B、Al、Ga单质的熔点依次为2300°C,660°C,29.8°C,解释熔点产生差异的原因
(5)由B、N、F组成的某离子化合物中,B、N、F的原子个数比为1:1:8,其阴、阳离子互为等电子体,该化合物中的阳离子、阴离子符号分别为
(6)GaAs晶体结构如图所示。
①图中As原子的坐标参数为
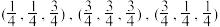 ,
,②已知晶胞中相邻且最近的Ga、As原子的核间距为acm,NA为阿伏加 德罗常数的值,晶体的密度为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】近日,科学家利用铁配合物催化氮气选择性转化成肼。铁配合物结构如图所示(Et为乙基:-CH2CH3)。

回答下列问题:
(1)基态 的价层电子排布式
的价层电子排布式___________ ,微粒半径Fe___________  。(填“大于”、“小于”或“等于”)
。(填“大于”、“小于”或“等于”)
(2) 所含元素中,电负性最大的元素是
所含元素中,电负性最大的元素是___________ 。P原子的杂化类型是___________ 。
(3) 和
和 的相对分子质量相同,但是常温常压下,
的相对分子质量相同,但是常温常压下, 呈液态,而
呈液态,而 呈气态,其主要原因是
呈气态,其主要原因是___________ 。
(4) 的VSEPR模型为
的VSEPR模型为___________ 。写出N2的一种等电子体___________ 。
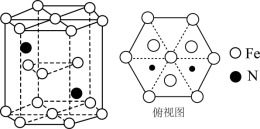
(5)某种磁性氮化铁的晶胞结构如图所示。已知: 为阿伏加德罗常数的值,六棱柱底边的边长为
为阿伏加德罗常数的值,六棱柱底边的边长为 ,高为
,高为 ,该晶体中Fe、N原子个数最简比为
,该晶体中Fe、N原子个数最简比为___________ 。该晶体的密度为___________  (只列计算式)。
(只列计算式)。

回答下列问题:
(1)基态
 的价层电子排布式
的价层电子排布式 。(填“大于”、“小于”或“等于”)
。(填“大于”、“小于”或“等于”)(2)
 所含元素中,电负性最大的元素是
所含元素中,电负性最大的元素是(3)
 和
和 的相对分子质量相同,但是常温常压下,
的相对分子质量相同,但是常温常压下, 呈液态,而
呈液态,而 呈气态,其主要原因是
呈气态,其主要原因是(4)
 的VSEPR模型为
的VSEPR模型为(5)某种磁性氮化铁的晶胞结构如图所示。已知:
 为阿伏加德罗常数的值,六棱柱底边的边长为
为阿伏加德罗常数的值,六棱柱底边的边长为 ,高为
,高为 ,该晶体中Fe、N原子个数最简比为
,该晶体中Fe、N原子个数最简比为 (只列计算式)。
(只列计算式)。
您最近半年使用:0次



