20-21高三下·浙江·阶段练习
1 . 硫酸在国民经济中占有极其重要的地位,工业上常用黄铁矿为原料接触法制硫酸。
(1)写出黄铁矿(FeS2)在沸腾炉中与氧气发生反应的化学方程式_______ 。
(2)硫酸的生产中,下列说法不正确的是_______ 。
A.把黄铁矿磨成细粉末在“沸腾”状态下燃烧,可以提高原料的利用率
B.气体在进接触室前要先净化,可防止催化剂中毒
C.接触室中反应采用400-500°C,主要是因为提高原料的平衡转化率
D.吸收塔中操作采取逆的形式,SO3从下而上,水从上而喷下
(3)分别将1mol的SO2(g)、1.45mol的O2(g)通入p1、p2和p3恒压容器中发生反应: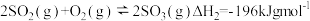 ,相同时间内测得SO2的转化率α随温度的变化如图所示。(对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数,记作Kp如p(B)=px(B),p为平衡总压强,x(B为平衡系统中B的物质的量分数)。
,相同时间内测得SO2的转化率α随温度的变化如图所示。(对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数,记作Kp如p(B)=px(B),p为平衡总压强,x(B为平衡系统中B的物质的量分数)。
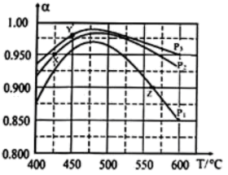
请回答:
①据图判断p1、p2、p3的大小关系_______ 。
②判断X、Y、Z中属于平衡点的是_______ (填“X”、 “Y”、 “Z”),并计算该温度下平衡的Kp=_______ 。(用含p1或p2或p3的式子表示)。
(4)为减少SO2的排放,工业上常将SO2转化为CaSO4固定,但存在CO又会同时发生以下两个反应:
①恒容、恒温(T1)条件下,反应体系中c(SO2)随时间t变化的总趋势如图。结合已知信息分析c(SO2)浓度随时间t变化的原因_______ 。
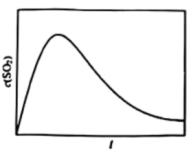
②恒容、恒温(T2,T2>T1)条件下,请在图中画出T2条件下c(SO2)浓度随时间t变化图_______ 。
(1)写出黄铁矿(FeS2)在沸腾炉中与氧气发生反应的化学方程式
(2)硫酸的生产中,下列说法不正确的是
A.把黄铁矿磨成细粉末在“沸腾”状态下燃烧,可以提高原料的利用率
B.气体在进接触室前要先净化,可防止催化剂中毒
C.接触室中反应采用400-500°C,主要是因为提高原料的平衡转化率
D.吸收塔中操作采取逆的形式,SO3从下而上,水从上而喷下
(3)分别将1mol的SO2(g)、1.45mol的O2(g)通入p1、p2和p3恒压容器中发生反应:
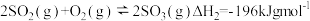 ,相同时间内测得SO2的转化率α随温度的变化如图所示。(对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数,记作Kp如p(B)=px(B),p为平衡总压强,x(B为平衡系统中B的物质的量分数)。
,相同时间内测得SO2的转化率α随温度的变化如图所示。(对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数,记作Kp如p(B)=px(B),p为平衡总压强,x(B为平衡系统中B的物质的量分数)。
请回答:
①据图判断p1、p2、p3的大小关系
②判断X、Y、Z中属于平衡点的是
(4)为减少SO2的排放,工业上常将SO2转化为CaSO4固定,但存在CO又会同时发生以下两个反应:
| 反应 | 活化能 | 平衡常数 | |
| I | 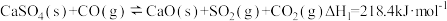 | EaI | KI |
| II | 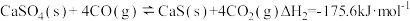 | EaII(EaII>EaI) | KII(KI>KII) |

②恒容、恒温(T2,T2>T1)条件下,请在图中画出T2条件下c(SO2)浓度随时间t变化图
您最近一年使用:0次
名校
2 . 请回答下列问题
(1)已知:25℃时,0.1 mol·L-1的HA溶液中c(H+)/c(OH-)=1010。
①HA是________ (填“强电解质”或“弱电解质”);
②在加水稀释HA溶液的过程中,随着水量的增加而减小的是________ (填字母)。
A.c(H+)/c(HA) B.c(HA)/ c (A-)
C.c(H+)与c(OH-)的乘积 D.c(OH-)
③若M溶液是由上述HA溶液V1 mL与pH = 12的NaOH溶液V2 mL混合充分反应而得,则下列说法中正确的是_______ (填字母)。
A.若溶液M呈中性,则溶液M中c(H+) + c(OH-) = 2.0×10-7 mol·L-1
B.若V1 =V2 ,则溶液M的pH一定等于7
C.若溶液M呈酸性,V1一定大于V2
D.若溶液M呈碱性,V1一定小于V2
(2)若已知在25℃,AgCl的Ksp = 1.8×10-10,现将足量AgCl分别放入:①100 mL 蒸馏水中;②100 mL 0.2mol·L-1 AgNO3溶液中;③100 mL 0.1mol·L-1 AlCl3溶液中;④100 mL 0.1mol·L-1盐酸中,充分搅拌后,相同温度下c(Ag+)由大到小的顺序是__________ (用序号连接)
(3)对于2NO2(g) N2O4(g) ΔH < 0反应,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。则下列说法正确的是
N2O4(g) ΔH < 0反应,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。则下列说法正确的是____ 。

①A、C两点的反应速率:A>C
②A、C两点气体的颜色:A深、C浅
③B、C两点的气体的平均分子质量:B<C
④由状态B到状态A,可以用加热方法
(1)已知:25℃时,0.1 mol·L-1的HA溶液中c(H+)/c(OH-)=1010。
①HA是
②在加水稀释HA溶液的过程中,随着水量的增加而减小的是
A.c(H+)/c(HA) B.c(HA)/ c (A-)
C.c(H+)与c(OH-)的乘积 D.c(OH-)
③若M溶液是由上述HA溶液V1 mL与pH = 12的NaOH溶液V2 mL混合充分反应而得,则下列说法中正确的是
A.若溶液M呈中性,则溶液M中c(H+) + c(OH-) = 2.0×10-7 mol·L-1
B.若V1 =V2 ,则溶液M的pH一定等于7
C.若溶液M呈酸性,V1一定大于V2
D.若溶液M呈碱性,V1一定小于V2
(2)若已知在25℃,AgCl的Ksp = 1.8×10-10,现将足量AgCl分别放入:①100 mL 蒸馏水中;②100 mL 0.2mol·L-1 AgNO3溶液中;③100 mL 0.1mol·L-1 AlCl3溶液中;④100 mL 0.1mol·L-1盐酸中,充分搅拌后,相同温度下c(Ag+)由大到小的顺序是
(3)对于2NO2(g)
 N2O4(g) ΔH < 0反应,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。则下列说法正确的是
N2O4(g) ΔH < 0反应,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。则下列说法正确的是
①A、C两点的反应速率:A>C
②A、C两点气体的颜色:A深、C浅
③B、C两点的气体的平均分子质量:B<C
④由状态B到状态A,可以用加热方法
您最近一年使用:0次
2016-12-09更新
|
248次组卷
|
3卷引用:江西省吉安市永新中学2021-2022学年高二上学期期中考试化学(理科)试题



