名校
1 . 用下列实验装置进行相应实验,能达到实验目的的是
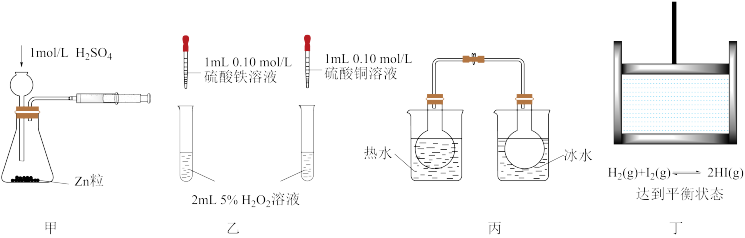

| A.利用装置甲测定化学反应速率 |
| B.利用装置乙证明对H2O2分解反应Fe3+催化效果好于Cu2+ |
| C.利用装置丙探究温度对平衡2NO2(g)⇌N2O4(g)的影响 |
| D.利用装置丁探究压强对平衡H2(g)+I2(g)⇌2HI(g)的影响 |
您最近一年使用:0次
2022-09-19更新
|
465次组卷
|
3卷引用:山东省济南市莱芜凤城高级中学2021-2022学年高二上学期期中考试化学试题
名校
解题方法
2 . 下列由实验现象所得结论正确的是
| A.向H2S气体中通入SO2气体,瓶壁上产生淡黄色固体,证明SO2具有氧化性 |
| B.压缩二氧化氮气体时,气体颜色加深,证明加压时N2O4与NO2的混合气体中NO2的含量增大 |
| C.向Fe(NO3)2溶液中滴加稀硫酸,溶液变为黄色,证明稀硫酸可将Fe2+氧化为Fe3+ |
| D.常温下,向铁质容器中注入浓硫酸,无明显现象,证明铁在常温下不与浓硫酸反应 |
您最近一年使用:0次
2021-12-25更新
|
300次组卷
|
5卷引用:重庆市2021-2022学年高三12月联考化学试题
重庆市2021-2022学年高三12月联考化学试题河北省保定市2021-2022学年高三上学期期末考试化学试题(已下线)卷04 元素及其化合物-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)河北省唐山市开滦第一中学2022-2023学年高三上学期期末考试化学试题课时3影响化学平衡的因素随堂练习
名校
解题方法
3 . 下列各实验装置、目的或结论全都正确的是
| 选项 | A | B | C | D |
| 实验装置 |  | 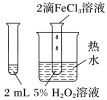 | 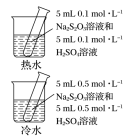 | 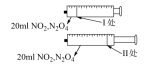 |
| 目的或结论 | 测定锌与稀硫酸反应生成氢气的速率 | 验证 对 对 分解反应有催化作用 分解反应有催化作用 | 依据出现浑浊的快慢比较温度对反应速率的影响 | 活塞I处→II处压强减小,颜色变化可证明平衡移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . NO与CO是燃油汽车尾气中的两种有害气体,常温常压下它们之间的反应: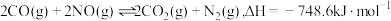 ,
, ,反应速率较小,有关该反应的说法正确的是
,反应速率较小,有关该反应的说法正确的是
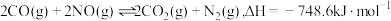 ,
, ,反应速率较小,有关该反应的说法正确的是
,反应速率较小,有关该反应的说法正确的是| A.K很大,说明NO与CO在排入大气之前就已反应完全 |
B.增大压强,反应速率增大,平衡将向右移动,K>2.5 106 106 |
| C.升高温度,既加快反应速率又可以提高有害气体的平衡转化率 |
| D.选用适宜催化剂可以使尾气排放达到标准 |
您最近一年使用:0次
2023-12-22更新
|
73次组卷
|
3卷引用:广东省广州真光中学2021-2022学年高二上学期期中考试化学试题
名校
5 . T1时,在1L恒容密闭容器中充入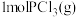 和
和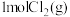 ,发生反应:
,发生反应: ,
, ,达平衡时升温至T2,实验测得:
,达平衡时升温至T2,实验测得: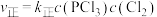 、
、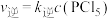 ,
, ,
, 为速率常数,只与温度有关。下列说法不正确的是
为速率常数,只与温度有关。下列说法不正确的是
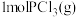 和
和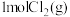 ,发生反应:
,发生反应: ,
, ,达平衡时升温至T2,实验测得:
,达平衡时升温至T2,实验测得: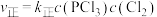 、
、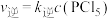 ,
, ,
, 为速率常数,只与温度有关。下列说法不正确的是
为速率常数,只与温度有关。下列说法不正确的是A.当 且不变时,该反应达到平衡状态 且不变时,该反应达到平衡状态 |
B.该反应的平衡常数可表示为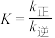 , ,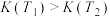 |
C.向T1温度下的平衡体系再充入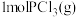 ,平衡正向移动,产物 ,平衡正向移动,产物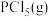 的体积分数变大 的体积分数变大 |
D.T1时,在一恒压密闭容器中充入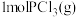 和 和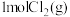 ,发生上述反应, ,发生上述反应, 的转化率变大 的转化率变大 |
您最近一年使用:0次
2023-08-23更新
|
468次组卷
|
4卷引用:云南省保山市2020-2021学年高二下学期期末考试化学试题
6 . 一定温度下的平衡体系: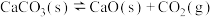 中仅含有
中仅含有 、CaO及
、CaO及 气体。此时压强为p,体积为2V。在t0时刻,将容器容积压缩到V且保持不变。测得体系中压强与时间关系如图所示(忽略固体所占体积)。下列说法错误的是
气体。此时压强为p,体积为2V。在t0时刻,将容器容积压缩到V且保持不变。测得体系中压强与时间关系如图所示(忽略固体所占体积)。下列说法错误的是

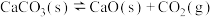 中仅含有
中仅含有 、CaO及
、CaO及 气体。此时压强为p,体积为2V。在t0时刻,将容器容积压缩到V且保持不变。测得体系中压强与时间关系如图所示(忽略固体所占体积)。下列说法错误的是
气体。此时压强为p,体积为2V。在t0时刻,将容器容积压缩到V且保持不变。测得体系中压强与时间关系如图所示(忽略固体所占体积)。下列说法错误的是
A.容器容积缩小, 浓度增大,平衡向左移动 浓度增大,平衡向左移动 |
| B.t1时,CaO几乎反应完全 |
| C.t1时,若再加入足量的CaO,达到新平衡时体系的压强大于p |
D.若t₀时,向体系中增加少量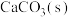 ,反应速率不变 ,反应速率不变 |
您最近一年使用:0次
名校
7 . 甲醇脱氢可制取甲醛,反应原理为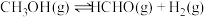 ,甲醇的平衡转化率随温度的变化曲线如图所示(已知反应在1L的密闭容器中进行,甲醇的初始物质的量为1mol)。下列有关说法正确的是
,甲醇的平衡转化率随温度的变化曲线如图所示(已知反应在1L的密闭容器中进行,甲醇的初始物质的量为1mol)。下列有关说法正确的是

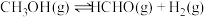 ,甲醇的平衡转化率随温度的变化曲线如图所示(已知反应在1L的密闭容器中进行,甲醇的初始物质的量为1mol)。下列有关说法正确的是
,甲醇的平衡转化率随温度的变化曲线如图所示(已知反应在1L的密闭容器中进行,甲醇的初始物质的量为1mol)。下列有关说法正确的是
A.脱氢反应的 |
B.600K时,Y点: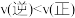 |
| C.要实现从Y点到Z点的变化可通过增大压强的方法 |
D.在 时,该反应的平衡常数为8.1 时,该反应的平衡常数为8.1 |
您最近一年使用:0次
2022-02-27更新
|
82次组卷
|
2卷引用:辽宁省渤海大学附属高级中学2021-2022学年高二上学期第二次月考化学试题
8 . 在一定条件下,碳与水蒸气可发生的化学反应为:C(s)+H2O(g)  CO(g)+H2(g) ΔH>0。下列有关说法正确的是
CO(g)+H2(g) ΔH>0。下列有关说法正确的是
 CO(g)+H2(g) ΔH>0。下列有关说法正确的是
CO(g)+H2(g) ΔH>0。下列有关说法正确的是| A.当反应达平衡时,恒温恒压条件下通入Ar,H2O的转化率不变 |
| B.在一定条件下达平衡时,使用催化剂能加快反应速率,增加生成物的产量 |
| C.当反应达平衡时,其他条件不变,降低温度可使该反应的平衡常数减小 |
| D.其它条件不变时,升高温度,正反应速率增大、逆反应速率减小,平衡正向移动 |
您最近一年使用:0次
名校
9 . 如图表示合成氨反应过程中的能量变化。关于合成氨反应 ,下列说法
,下列说法不 正确的是
 ,下列说法
,下列说法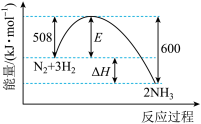
A.升高温度有利于提高 的平衡转化率 的平衡转化率 |
B.提高 与 与 的投料比可增大 的投料比可增大 的转化率 的转化率 |
C.增大压强能提高 的反应速率和转化率 的反应速率和转化率 |
| D.使用催化剂能缩短该反应到达平衡的时间 |
您最近一年使用:0次
2022-11-18更新
|
293次组卷
|
8卷引用:江苏省扬州市2020-2021学年高二下学期期末考试化学(选修)试题
江苏省扬州市2020-2021学年高二下学期期末考试化学(选修)试题(已下线)第二章 第三节化学平衡(第2课时 化学平衡的影响因素)(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)(原卷版)(已下线)第2章 化学反应速率和化学平衡(提分小卷)-【单元测试】2021-2022学年高二化学尖子生选拔卷(人教版选修4)云南昆明师范专科学校附属中学2021-2022学年高二上学期期中考试化学试题(已下线)2.4 化学反应的调控(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)第二章 化学反应速率与化学平衡(B卷·能力提升练)【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)江苏省马坝高级中学2022-2023学年高二上学期期中考试化学试题江苏省南京市五校(秦淮中学,溧水二高,江浦文昌)2023-2024学年高二下学期期中联考化学试题
10 . 二氧化碳到淀粉的人工合成第一步为用无机催化剂将二氧化碳还原为甲醇,反应方程式为3H2(g)+CO2(g) CH3OH(g)+H2O(g)。一定温度下,恒容密闭容器中按照投料比
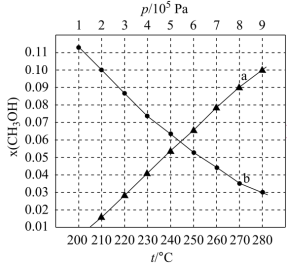
CH3OH(g)+H2O(g)。一定温度下,恒容密闭容器中按照投料比 =3充入H2与CO2,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x(CH3OH),在T=250℃下的x(CH3OH)~p、在p=5×105Pa下的x(CH3OH)~T如图所示。下列说法不正确的是
=3充入H2与CO2,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x(CH3OH),在T=250℃下的x(CH3OH)~p、在p=5×105Pa下的x(CH3OH)~T如图所示。下列说法不正确的是
 CH3OH(g)+H2O(g)。一定温度下,恒容密闭容器中按照投料比
CH3OH(g)+H2O(g)。一定温度下,恒容密闭容器中按照投料比 =3充入H2与CO2,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x(CH3OH),在T=250℃下的x(CH3OH)~p、在p=5×105Pa下的x(CH3OH)~T如图所示。下列说法不正确的是
=3充入H2与CO2,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x(CH3OH),在T=250℃下的x(CH3OH)~p、在p=5×105Pa下的x(CH3OH)~T如图所示。下列说法不正确的是
| A.当体系中c(CH3OH)与c(H2)比值不变,可说明此时该反应达到平衡状态 |
| B.曲线b表示的是压强相同时,温度升高该反应逆向移动,说明正反应放热 |
| C.在原p=5×105Pa,210℃的条件下,向该恒容密闭容器中继续通入3molH2与1molCO2,达到新的平衡后,x(CH3OH)<0.10 |
| D.当x(CH3OH)=0.10时,反应条件可能为p=5×105Pa,210℃或p=9×105Pa,250℃ |
您最近一年使用:0次
2021-12-15更新
|
436次组卷
|
3卷引用:浙江省普通高中强基联盟2022届高三上学期12月统测化学试题
浙江省普通高中强基联盟2022届高三上学期12月统测化学试题(已下线)解密09 化学反应速率与化学平衡(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)北京市海淀区教师进修学校2022-2023学年高三下学期开学检测化学试题



