下列各实验装置、目的或结论全都正确的是
| 选项 | A | B | C | D |
| 实验装置 |  | 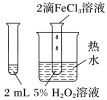 | 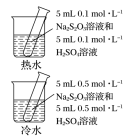 | 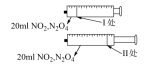 |
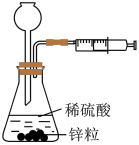
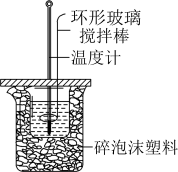
| 目的或结论 | 测定锌与稀硫酸反应生成氢气的速率 | 验证 对 对 分解反应有催化作用 分解反应有催化作用 | 依据出现浑浊的快慢比较温度对反应速率的影响 | 活塞I处→II处压强减小,颜色变化可证明平衡移动 |
| A.A | B.B | C.C | D.D |
更新时间:2021-10-13 17:22:32
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】下列装置或操作能达到实验目的的是
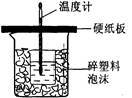

A.中和热测定 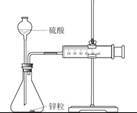 |
B.测定H2反应速率(mL•s—1) 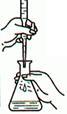 |
C.高锰酸钾滴定草酸 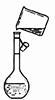 |
| D.定容 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列说法不正确的是
| A.新制氯水具有漂白性,故无法测定其pH值 |
| B.中和热测定实验中,应迅速将稀的NaOH溶液和稀的盐酸在测定装置中混合 |
| C.探究催化剂对H2O2分解速率的影响:在相同条件下,向一支试管中加入2mL5%H2O2和1mLH2O,向另一支试管中加入2ml 5% H2O2和lmL FeCl3溶液,观察并比较实验现象 |
| D.已知4H++4I-+O2=2I2+2H2O,为了利用该反应探究反应速率与温度的关系,所用试剂除1 mol·L-1 KI溶液、0.1 mol·L-1稀硫酸外,还需要用到淀粉溶液 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】升高温度,下列数据不一定增大的是
| A.化学平衡常数 K | B.水的离子积 Kw |
| C.化学反应速率 | D.醋酸的电离平衡常数 Ka |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列关于化学反应速率的说法正确的是
| A.0.1 mol·L-1盐酸和0.1 mol·L-1硝酸与相同形状和大小的大理石反应的速率相同 |
| B.化学反应速率为0.8 mol·L-1·s-1,其含义是时间为1s时,某物质的浓度是0.8 mol·L-1 |
| C.2mol/L盐酸与锌反应时,加入4mol/L的氯化钠溶液,生成氢气的速率加快 |
| D.工业上合成氨是放热反应,升高温度,正反应速率减慢 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】化学是以实验为基础的科学。下列实验操作或做法能达到目的的是
| 选项 | 操作或做法 | 目的 |
| A | 在过氧化氢溶液中加入少量 | 加快 的生成速率 的生成速率 |
| B | 用铂丝蘸取某溶液进行焰色反应,火焰呈黄色 | 证明该溶液溶质为钠盐 |
| C | 向稀盐酸中加入锌粒,将生成的气体通过浓硫酸 | 制取纯净的 |
| D | 用湿润的淀粉碘化钾试纸检验某气体,试纸变蓝 | 证明该气体为 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】据文献显示: 催化合成DMC的一种反应机理如图所示。下列叙述正确的是
催化合成DMC的一种反应机理如图所示。下列叙述正确的是

 催化合成DMC的一种反应机理如图所示。下列叙述正确的是
催化合成DMC的一种反应机理如图所示。下列叙述正确的是
| A.①②的反应类型不同 |
B. 能提高反应物的平衡转化率 能提高反应物的平衡转化率 |
| C.DMC是乙酸的同系物 |
| D.上述合成DMC的反应属于真正的“绿色化学”,实现了原子利用率100% |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
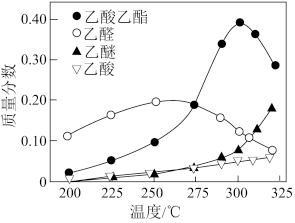
【推荐1】科学家研究了乙醇催化合成乙酸乙酯2C2H5OH(g) CH3COOC2H5(g)+2H2(g)的新方法。在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。下列推测合理的是
CH3COOC2H5(g)+2H2(g)的新方法。在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。下列推测合理的是
 CH3COOC2H5(g)+2H2(g)的新方法。在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。下列推测合理的是
CH3COOC2H5(g)+2H2(g)的新方法。在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。下列推测合理的是
| A.乙醛是该反应的催化剂 |
| B.加压有利于提高乙酸乙酯的产率 |
| C.提高催化剂的活性和选择性,减少乙醚等副产物是工艺的关键 |
| D.随着温度的升高,乙酸乙酯的质量分数先增大后减小,说明该反应是吸热反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列事实不能用勒夏特列原理(平衡移动原理)解释的是
①溴水中存在化学平衡:Br2+H2O HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
②铁在潮湿的空气中易生锈
③二氧化氮与四氧化二氮的平衡体系,增大压强后颜色加深
④合成氨反应,为提高氨的产率,理论上应采取降低温度的措施
⑤钠与氯化钾共融制备钾:Na(l)+KCl(l) K(g)+NaCl(l)
K(g)+NaCl(l)
①溴水中存在化学平衡:Br2+H2O
 HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅②铁在潮湿的空气中易生锈
③二氧化氮与四氧化二氮的平衡体系,增大压强后颜色加深
④合成氨反应,为提高氨的产率,理论上应采取降低温度的措施
⑤钠与氯化钾共融制备钾:Na(l)+KCl(l)
 K(g)+NaCl(l)
K(g)+NaCl(l)| A.①④ | B.③④ | C.②⑤ | D.②③ |
您最近一年使用:0次

 CO(g)+ H2(g),增加碳的量,平衡向正反应方向移动。
CO(g)+ H2(g),增加碳的量,平衡向正反应方向移动。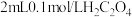 溶液的试管中分别加入
溶液的试管中分别加入 和
和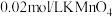 溶液,比较溶液褪色快慢
溶液,比较溶液褪色快慢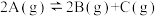 -Q;达平衡时,要使c(A)增大,应采取的措施是
-Q;达平衡时,要使c(A)增大,应采取的措施是

